Uždaviniai ir jų sprendimas
1. Kai nebūtina reakcijos lygtis
1.3. Mišinių ir junginių sudėtis
Uždavinys Nr.1
Apskaičiuokite K2Cr2O7 junginyje elementų sudėtį masės %.
Uždavinio sprendimas:
Kiekvieno elemento masės dalis % junginyje apskaičiuojama:
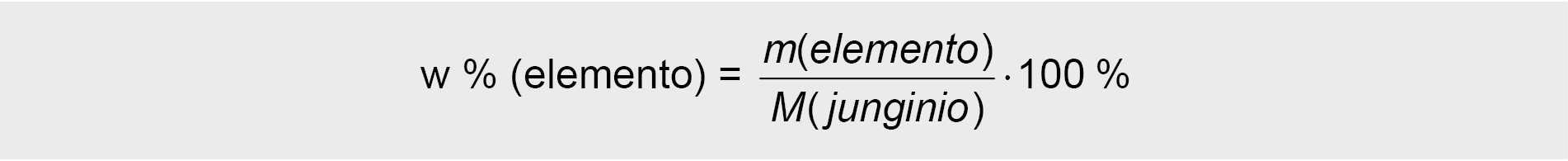
2. Apskaičiuojame kiekvieno elemento masės dalį %:

3. Pasitikriname, ar teisingai suskaičiuota – visų elementų % suma tyri būti lygi 100 %:
Uždavinys Nr. 2
Junginyje yra 34,6% natrio, 23,3% fosforo ir 42,1% deguonies. Suraskite junginio formulę?
Uždavinio sprendimas:
1. Pirmiausia pasitikriname, ar sudėjus visas elementų procentines dalis gausime 100 %:
![]()
Vadinasi 100 g junginio yra 34,6 g natrio, 23,3 g fosforo ir 42,1 g deguonies.
2. Randame elementų molinį santykį:
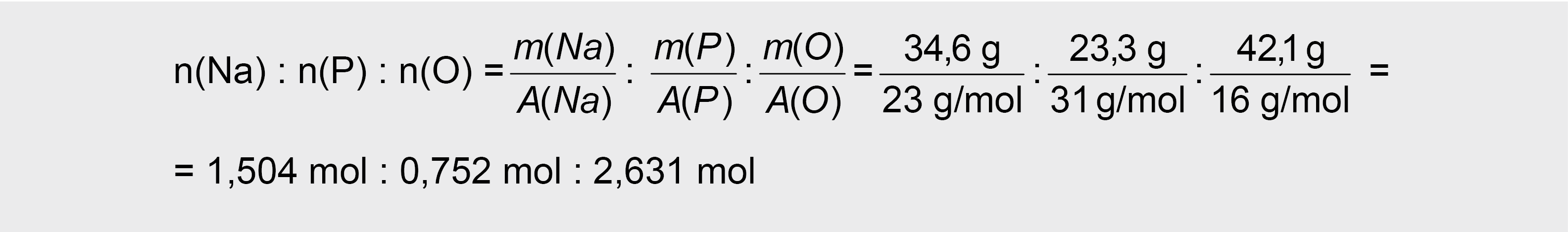
3. Visus skaičius reikia padalinti iš mažiausio (šiuo atveju 0,752), tuomet gauname:
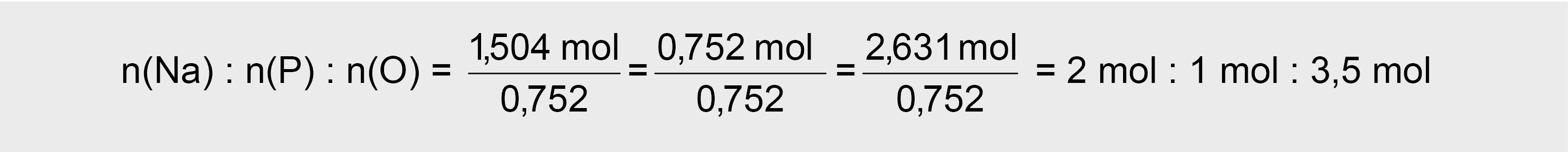
4. Kadangi vienas molinio santykio skaitmuo yra 3,5, tai visus padauginame iš 2, kad būtų sveikieji skaitmenys:
![]()
Tuomet junginio formulė bus Na4P2O7
Uždavinys Nr. 3
Junginyje yra 77,4% anglies, 7,5% vandenilio ir 15,1% azoto. Junginio garų santykinis tankis oro atžvilgiu – 3,2. Kokia junginio formulė?
Uždavinio sprendimas:
1. Pirmiausia pasitikriname, ar sudėjus visas elementų procentines dalis gausime 100 %:
![]()
Vadinasi 100 g junginio yra 77,4 g anglies, 7,5 g vandenilio ir 15,1 g azoto.
2. Randame elementų molinį santykį:

3. Visus skaičius reikia padalinti iš mažiausio (šiuo atveju 1,08), tuomet gauname:
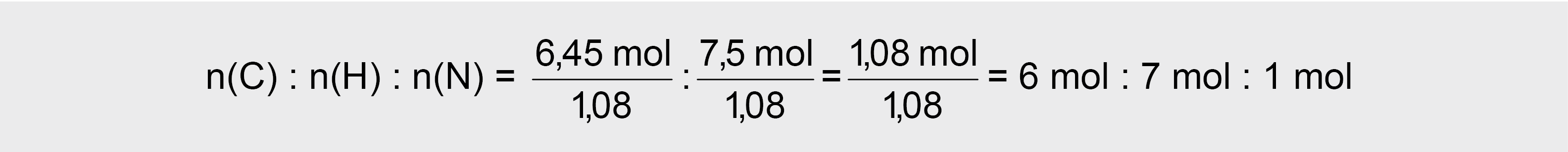
4. Empyrinė junginio formulė C6H7N
5. Apskaičiuojame tikrąją junginio molinę masę:

6. Apskaičiuojame empyrinio junginio molinę masę:
![]()
7. Kadangi empyrinio junginio molio masė yra lygi tikrojo junginio masei, tai junginys yra
C6H7N arba C6H5NH2 - fenilaminas
