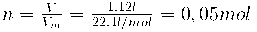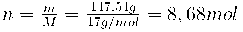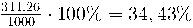Uždaviniai ir jų sprendimas
| Site: | KTU Open Courses |
| Course: | ★ CHEMIJA išlyginamieji mokymai |
| Book: | Uždaviniai ir jų sprendimas |
| Printed by: | Guest user |
| Date: | Saturday, 30 May 2026, 2:02 PM |
1. Kai nebūtina reakcijos lygtis
Šiame skyriuje rasite uždavinių sprendimo pavyzdžių, kuriuose reikia:
- įvertinti dujinių ir kietųjų medžiagų tirpumą vandenyje;
- skaičiuoti procentinę (masės dalies) ir molinės koncentracijas;
- nustatyti mišinių ir junginių sudėtį.
1.1. Kai reikia įvertinti dujų tirpumą
Kai kurių dujų tirpumo vandenyje priklausomybės nuo temperatūros (kai p=101,325 kPa)
Dažniausiai įvairių dujų tirpumo vandenyje priklausomybės nuo temperatūros yra atvaizduojamos grafiškai. Tačiau tikslias dujų tirpumo vertes galima rasti žinynų lentelės.Atkreipkite dėmesį: didėjant temperatūrai daugumos dujų tirpumas vandenyje mažėja!!! Ypač menkai tirpių dujų tirpumas vandenyje beveik nekinta didėjant temperatūrai.
Pagrindinių orą sudarančių dujų (N2, O2) tirpumas vandenyje yra gan mažas. Vandenilio bei visų inertinių dujų tirpumas vandenyje yra ypač mažas.
CO2 ir H2S tirpumas yra gerokai didesnis nei pagrindinių orą sudarančių dujų.
Tačiau tokių dujų, kurios ištirpę vandenyje gana gerai jonizuojasi (NH3, SO2, HCl), tirpumas vandenyje yra ypač didelis.
1 pav. Azoto (N2), deguonies (O2) ir vandenilio (H2) dujų tirpumo vandenyje priklausomybė nuo temperatūros (kai p=101,325 kPa)
2 pav. CO2 ir H2S dujų tirpumo vandenyje priklausomybė nuo temperatūros (kai p=101,325 kPa)
3 pav. NH3, SO2 ir HCl dujų tirpumo vandenyje priklausomybė nuo temperatūros (kai p = 101,325 kPa)
Uždavinys Nr.1
Kiek litrų reikia paimti 50 ºC temperatūros vandens, norint ištirpinti 1,12 l deguonies dujų?
Uždavinio sprendimas:
1. Iš 1 pav. pavaizduotų tirpumo kreivių surandame deguonies dujų tirpumą 50 ºC temperatūros vandenyje.
50 ºC temperatūros vandenyje gali ištirpti 3 mg deguonies dujų 100 g vandens.
2. Apskaičiuojame, kiek molių sudaro 1,12 l deguonies dujų:
3. Apskaičiuojame deguonies dujų masę:
m = n · M = 0,05 mol · 32 g/mol = 1,6 g
4. Apskaičiuojame, kiek litrų reikia paimti vandens, norint ištirpinti 1,6 g deguonies dujų:
3 mg – 100 g (vandens)
1600 mg – x g (vandens)
x = 53333 g = 53,333 kg
V = m / ρ = 53333 / 1 g/ml = 53333 ml = 53,333 l
Atsakymas: reikia 53,333 litrų vandens.
Uždavinys Nr.2
Apskaičiuokite, koks tūris amoniako dujų išsiskirs šildant 1 kg sotųjį amoniako tirpalą nuo 20 ºC iki 40 ºC temperatūros. Kokia bus amoniako masės dalis 20 ºC ir 40 ºC temperatūros tirpaluose?Uždavinio sprendimas:
1. Iš 3 pav. pavaizduotų tirpumo kreivių surandame amoniako dujų tirpumą 20 ºC ir 40 ºC temperatūros vandenyje.
20 ºC temperatūros vandenyje gali ištirpti 52,5 g amoniako dujų 100 g vandens.
40 ºC temperatūros vandenyje gali ištirpti 30 g amoniako dujų 100 g vandens.2. Apskaičiuojame, kiek gramų amoniako ir vandens (tirpiklio) yra 20 ºC temperatūros 1 kg sotaus tirpalo:
m(tirpalo) = 100 g (vandens) + 52,5 g (NH3) = 152,5 g
152,5 g (tirpalo) – 52,5 g (NH3)
1000 g (tirpalo) – x g (NH3)
x = 344,26 g (NH3)
m (H2O) = 1000 g – 344,26 g = 655,74 g
3. Apskaičiuojame kiek gramų amoniako gali ištirpti 40 ºC temperatūros vandenyje (655,4 g):
100 g (vandens) – 30 g (NH3)
655,4 g (vandens) - x g (NH3)
x = 196,72 g
4. Apskaičiuojame koks tūris amoniako dujų išsiskirs šildant tirpalą nuo 20 ºC iki 40 ºC:
m(NH3)išsiskirs = 344,26 g – 196,72 g = 147,54 g
Norint masę paversti į tūrį, reikia susirasti molius:
V = n · Vm = 8,68 mol · 22,4 l/mol = 194,4 l100 g (tirpalo) – x g (NH3)
x = 34,43 %
6. Apskaičiuojame 40 ºC temperatūros amoniako masės dalį tirpale:
m(tirpalo) = 655,74 g + 196,72 g = 852,46 g
852,46 g (tirpalo) – 196,72 g (NH3)
100 g (tirpalo) – x g (NH3)
x = 23,08 %1.2. Kai reikia įvertinti kietųjų medžiagų tirpumą
Kai kurių kietųjų medžiagų tirpumo vandenyje priklausomybės nuo temperatūros
Tirpalai – tai vienalyčiai mišiniai. Jie yra skirstomi į:
- Nesočiuosius (tam tikroje temperatūroje, į tirpalą pridėjus dar medžiagos, ji ištirpsta).
- Sočiuosius (tam tikroje temperatūroje, į tirpalą pridėjus dar medžiagos, ji nebetirpsta).
- Persotintuosius (tam tikroje temperatūroje ištirpusios medžiagos yra daugiau, negu jos gali būti sočiajame tirpale).
Bet kuris tirpumo kreivės taškas rodo, kiek medžiagos tam tikroje temperatūroje maksimaliai ištirpsta 100 g vandens, susidarant sočiajam tirpalui.
- Iš nesotaus sotųjį tirpalą galima gauti ištirpinus tam tikrą kiekį medžiagos arba tirpalą atšaldžius.
- Iš sotaus tirpalo nesotųjį galima gauti tirpalą pašildžius arba įpylus daugiau tirpiklio.
- Persotintas tirpalas susidaro lėtai šaldant sotųjį tirpalą. Jeigu šaldant iškrenta kristalai, gauname sotųjį tirpalą žemesnėje temperatūroje. Persotintieji tirpalai yra labai nepatvarūs, atsiradus kristalizacijos centrui – jie išsikristalizuoja.
1 pav. Kai kurių natrio druskų tirpumo vandenyje priklausomybė nuo temperatūros
2 pav. Kai kurių kalio druskų tirpumo vandenyje priklausomybė nuo temperatūros
3 pav. Kai kurių hidroksidų tirpumo vandenyje priklausomybė nuo temperatūros
4 pav. Kalcio hidroksido tirpumo vandenyje priklausomybė nuo temperatūros
Uždavinys Nr. 1
Kokia natrio karbonato masės dalis (procentais) sočiajame tirpale 30 °C temperatūroje?
Uždavinio sprendimas:
1. Iš 1 pav. pavaizduotų tirpumo kreivių surandame Na2CO3 tirpumą 30 ºC temperatūros vandenyje.
30 ºC temperatūros vandenyje Na2CO3 tirpumas yra 40 g/100 g vandens.
2. Apskaičiuojame tirpalo masę:
m (tirpalo) = 100 g (vandens) + 40 g (Na2CO3) = 140 g
3. Apskaičiuojame natrio karbonato masės dalis (procentais) sočiajame tirpale 30 °C temperatūroje:
140 g (tirpalo) – 40 g (Na2CO3)
100 g (tirpalo) – x g (Na2CO3)
x = 28,57 % (Na2CO3)
Atsakymas: 28,57 %
Uždavinys Nr. 2
500 g 40 °C temperatūros sočiojo KNO3 tirpalo buvo pašildyta iki 100 °C. Apskaičiuokite, kiek gramų KNO3 reikia pridėti, kad gautas 100 °C temperatūros tirpalas vėl taptų sotusis.Uždavinio sprendimas:
1. Iš 2 pav. pavaizduotų tirpumo kreivių surandame KNO3 tirpumą 40 ºC ir 100 ºC temperatūros vandenyje.
40 ºC temperatūros vandenyje KNO3 tirpumas yra 65 g/100 g vandens.
100 ºC temperatūros vandenyje KNO3 tirpumas yra 245 g/100 g vandens.2. Apskaičiuojame, kiek gramų kalio nitrato ir vandens (tirpiklio) yra 40 ºC temperatūros 500 g sotaus KNO3 tirpalo:
m(tirpalo) = 100 g (vandens) + 65 g (KNO3 ) = 165 g
165 g (tirpalo) – 65 g (KNO3)
500 g (tirpalo) – x g (KNO3)
x = 196,97 g (KNO3)
m(H2O) = 500 g – 196,97 g = 303,03 g
3. Apskaičiuojame kiek gramų 100 ºC temperatūros 303,03 g vandens galima ištirpinti kalio nitrato, kad tirpalas būtų sotusis:
100 g (vandens) – 245 g (KNO3)
303,03 g (vandens) – x g (KNO3)
x = 742,42 g (KNO3)3. Apskaičiuojame kiek papildomai reikia įdėti kalio nitrato, kad tirpalas būtų sotusis:
m(KNO3) = 742,42 g – 196,97 g = 545,45 g
Atsakymas: 545,45 g
Uždavinys Nr. 3
Į tris chemines stiklines buvo įpilta po 100 g vandens ir ištirpinta po 30 g KCl, KNO3 ir NaNO3
druskos. Naudodamiesi tirpumo kreivėmis, nustatykite, kuris iš pateiktų teiginių yra teisingas:
a) esant 0 °C temperatūrai, visi tirpalai buvo nesotieji;
b) esant 10 °C temperatūrai, KCl masės dalis tirpale buvo mažiausia;
c) esant 20 °C temperatūrai, visi tirpalai buvo sotieji;
d) esant 30 °C temperatūrai, visuose tirpaluose druskos masės dalis buvo tokia pati.
Uždavinio sprendimas:
Iš 1 ir 2 pav. pateiktų kreivių nustatome, kad teisingas atsakymas yra d)
1.3. Mišinių ir junginių sudėtis
Uždavinys Nr.1
Apskaičiuokite K2Cr2O7 junginyje elementų sudėtį masės %.
Uždavinio sprendimas:
Kiekvieno elemento masės dalis % junginyje apskaičiuojama:
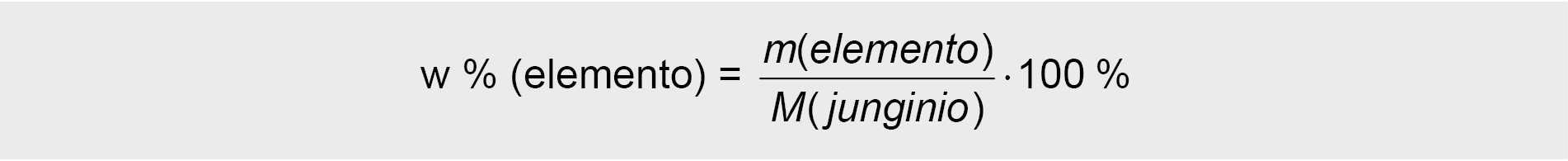
2. Apskaičiuojame kiekvieno elemento masės dalį %:

3. Pasitikriname, ar teisingai suskaičiuota – visų elementų % suma tyri būti lygi 100 %:
Uždavinys Nr. 2
Junginyje yra 34,6% natrio, 23,3% fosforo ir 42,1% deguonies. Suraskite junginio formulę?
Uždavinio sprendimas:
1. Pirmiausia pasitikriname, ar sudėjus visas elementų procentines dalis gausime 100 %:
![]()
Vadinasi 100 g junginio yra 34,6 g natrio, 23,3 g fosforo ir 42,1 g deguonies.
2. Randame elementų molinį santykį:
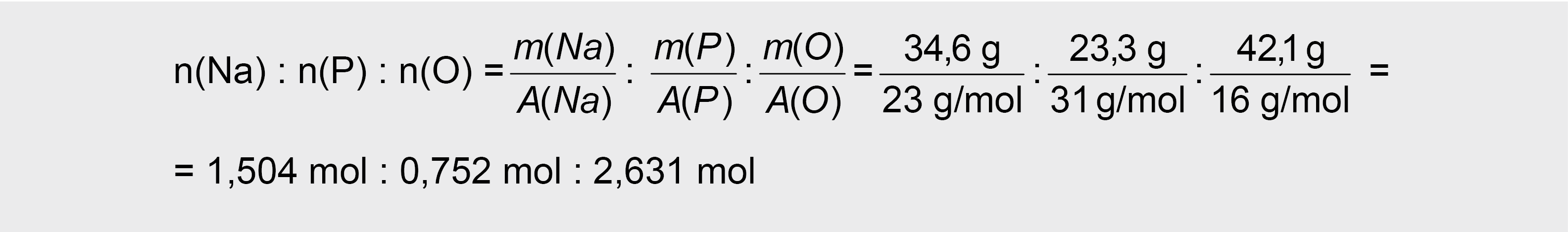
3. Visus skaičius reikia padalinti iš mažiausio (šiuo atveju 0,752), tuomet gauname:
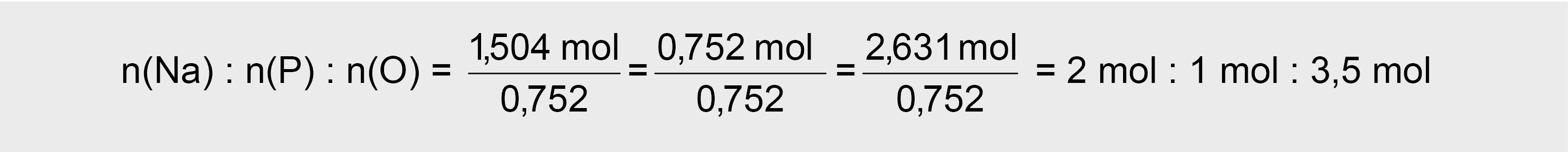
4. Kadangi vienas molinio santykio skaitmuo yra 3,5, tai visus padauginame iš 2, kad būtų sveikieji skaitmenys:
![]()
Tuomet junginio formulė bus Na4P2O7
Uždavinys Nr. 3
Junginyje yra 77,4% anglies, 7,5% vandenilio ir 15,1% azoto. Junginio garų santykinis tankis oro atžvilgiu – 3,2. Kokia junginio formulė?
Uždavinio sprendimas:
1. Pirmiausia pasitikriname, ar sudėjus visas elementų procentines dalis gausime 100 %:
![]()
Vadinasi 100 g junginio yra 77,4 g anglies, 7,5 g vandenilio ir 15,1 g azoto.
2. Randame elementų molinį santykį:

3. Visus skaičius reikia padalinti iš mažiausio (šiuo atveju 1,08), tuomet gauname:
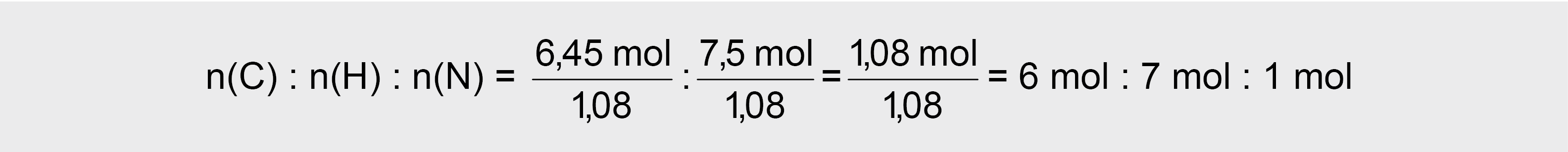
4. Empyrinė junginio formulė C6H7N
5. Apskaičiuojame tikrąją junginio molinę masę:

6. Apskaičiuojame empyrinio junginio molinę masę:
![]()
7. Kadangi empyrinio junginio molio masė yra lygi tikrojo junginio masei, tai junginys yra
C6H7N arba C6H5NH2 - fenilaminas
1.4. Tirpalų procentinė ir molinė koncentracijos
Uždavinys Nr.1
Gaminant praskiestos sulfato(VI) rūgšties H2SO4 tirpalą į 1 litrą distiliuoto vandens buvo įpiltas 1 litras koncentruotos 88 % H2SO4 tirpalo. Apskaičiuokite pagaminto praskiestos sulfato(VI) rūgšties H2SO4 tirpalo procentinę (masės dalies) ir molinę koncentracijas bei tikrąjį tūrį. Distiliuoto vandens, koncentruotos ir praskiestos sulfato(VI) rūgšties H2SO4 tirpalų tankius suraskite iš žemiau pateikto grafiko.
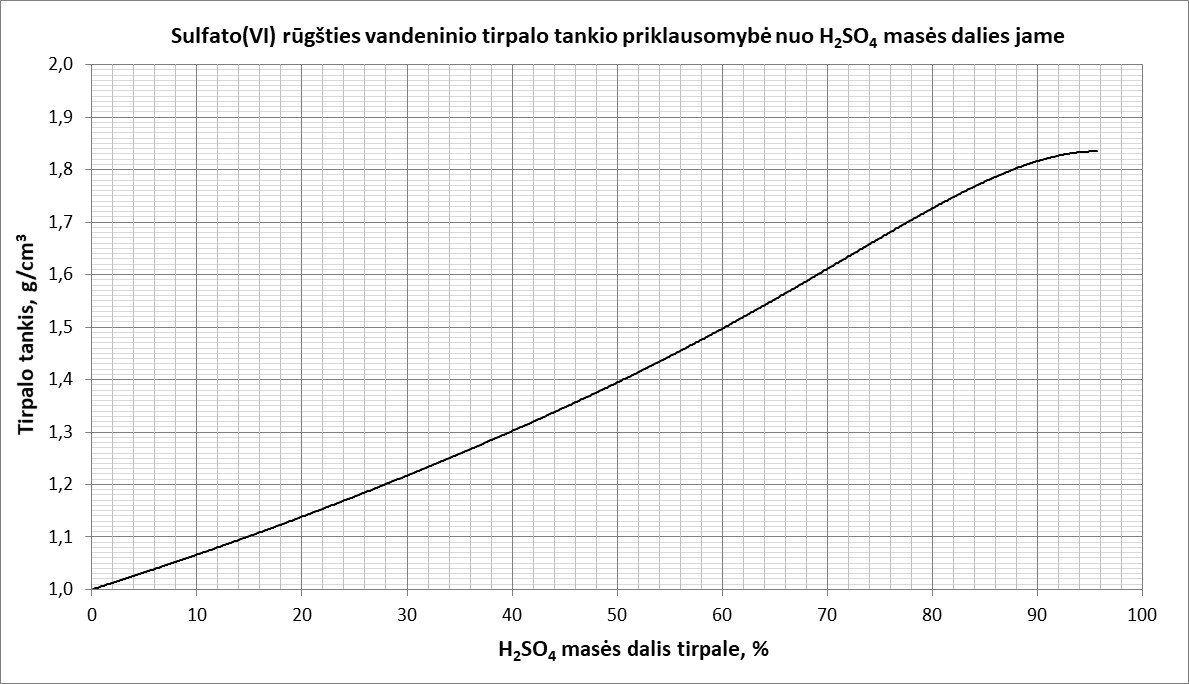
Uždavinio sprendimas:
1. Pirmiausiai iš grafiko surandami distiliuoto vandens ir 88 % koncentracijos H2SO4 tirpalo tankiai:- distiliuoto vandens tankis ρ (H2O) = 1,00 g/cm3 – šiuo atveju jis atitinka H2SO4 tirpalo, kuriame H2SO4 masės dalis tirpale yra lygi 0 %, tankį;
- 88 % koncentracijos H2SO4 tirpalo tankis ρ(88 % H2SO4) = 1,80 g/cm3
2. Po to, taikant tirpalo tankio formulę, apskaičiuojamos 1 litro (1000 cm3) distiliuoto vandens ir 1 litro (1000 cm3) 88 % koncentracijos H2SO4 tirpalo masės:
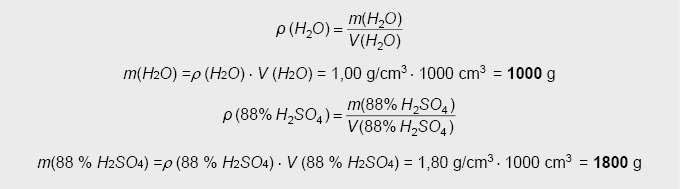
3. Apskaičiuojama grynos H2SO4 masė skiedžiamame 88 % koncentracijos H2SO4 tirpale:

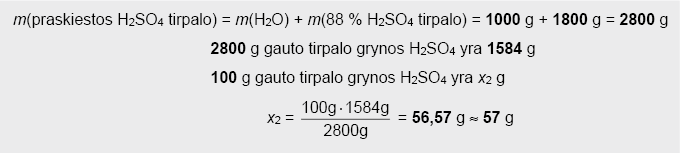
Kadangi tai yra grynos H2SO4 masė, esanti 100 g tirpalo, jos skaitinė verte atitinka praskiestos H2SO4 tirpalo procentinę (masės dalies) koncentraciją, t.y. w = 57 %
5. Gauto praskiestos H2SO4 tirpalo tūris apskaičiuojamas taikant tirpalo tankio formulę, prieš tai iš grafiko suradus 57 % koncentracijos H2SO4 tirpalo tankį: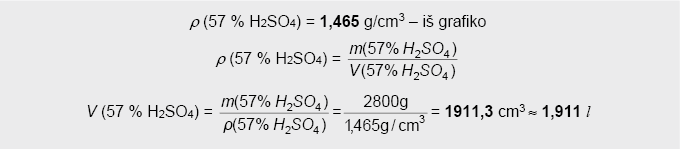

6. Apskaičiuojamas praskiestos H2SO4 tirpalo molinė koncentracija (mol/l) taikant jos apskaičiavimo formulę:
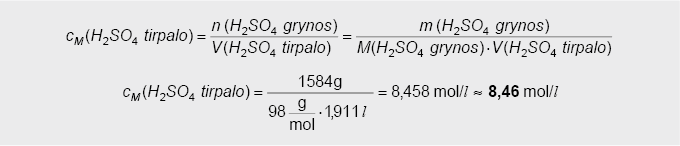
Uždavinys Nr.2
Vario sulfatas naudojamas mikroelementiniam (Cu) tręšimui bei pagrindinių grybinių ligų prevencijai. Tręšimui naudojamas 1 % vario sulfato tirpalas Pradžioje Linas 100 ml vandens ištirpino 10 g vario sulfato pentahidrato duskos. Iš šio tirpalo Linas turi paruošti reikiamos koncentracijos vario sulfato tirpalą. Kokia vario sulfato procentinė koncentracija šiame tirpale ? Kiek reikia Linui įpilti vandens, į pradinį tirpalą, kad paruoštų 1% tirpalą?
Uždavinio sprendimas:
1. Apskaičiuojame vario sulfato ir varios sulfato pentahidrato molines mases:
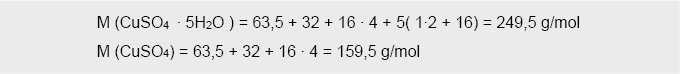
2. Apskaičiuojame, kiek CuSO4 g yra 10 g CuSO4 ∙ 5H2O:
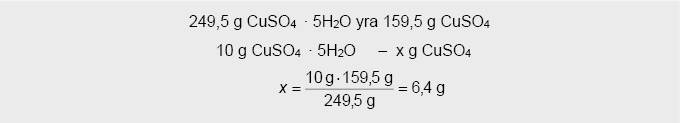
3. Skaičiuojame tirpalo masę:
![]()
4. Skaičiuojame vario sulfato procentinę koncentraciją šiame tirpale:

5. Skaičiuojame, kiek reikia įpilti vandens, į pradinį tirpalą, kad paruoštų 1% tirpalą:

Paruošim 640 g tirpalo, tai H2O reikia įpilti
![]()
Atsakymas: vario sulfato procentinė koncentracija šiame tirpale yra 5,82% ir Linui, į pradinį tirpalą, kad paruoštų 1% tirpalą, reikia įpilti 530 g (ml) vandens.
2. Kai vyksta tik viena reakcija
Uždavinys
Kiek gramų nuosėdų susidarys reaguojant 200 cm3 0,65 mol/l K3PO4 tirpalo su 115 ml 25 % MgCl2 tirpalo, kurio tankis yra 1,082 g/cm3?
Uždavinio sprendimas:
1. Pirmiausia užrašome ir išlyginame reakcijos lygtį:
![]()
2. Virš reakcijos lygties susirašome kas duota ir ką reikia rasti:
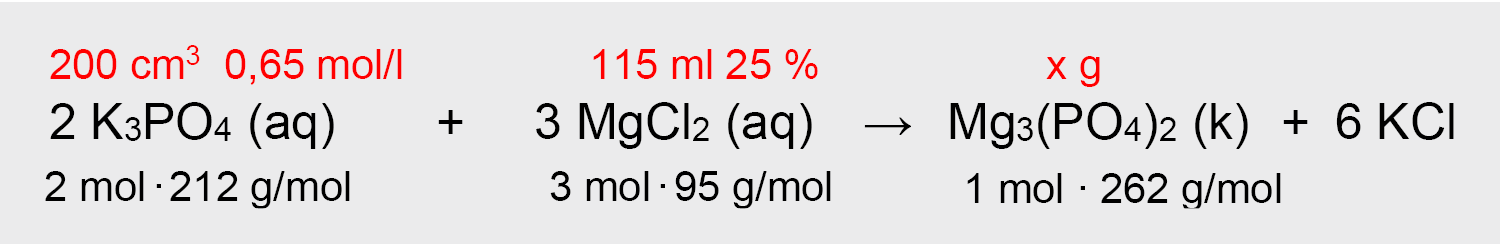
3. Suskaičiuojame molines mases:
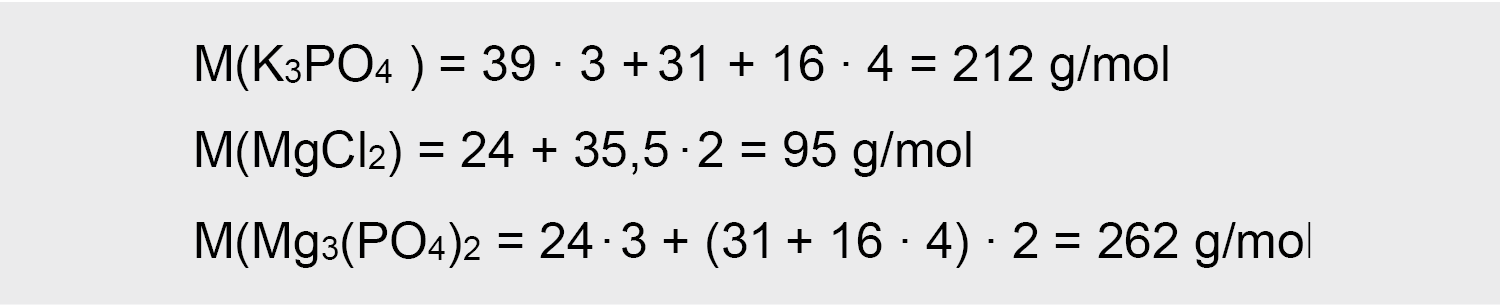
4. Apskaičiuojame kiek gramų gryno K3PO4 ir MgCl2 buvo paimta:

Pagal proporciją suskaičiuojam kiek gryno MgCl2 yra:

5. Skaičiuojame, kurios medžiagos yra perteklius. MgCl2 pasižymime x:

Kadangi mes MgCl2 turime 31,11 g, o mums reikia 18,525 g, tai vadinasi jo yra perteklius.
6. Skaičiuojame kiek susidarė nuosėdų:
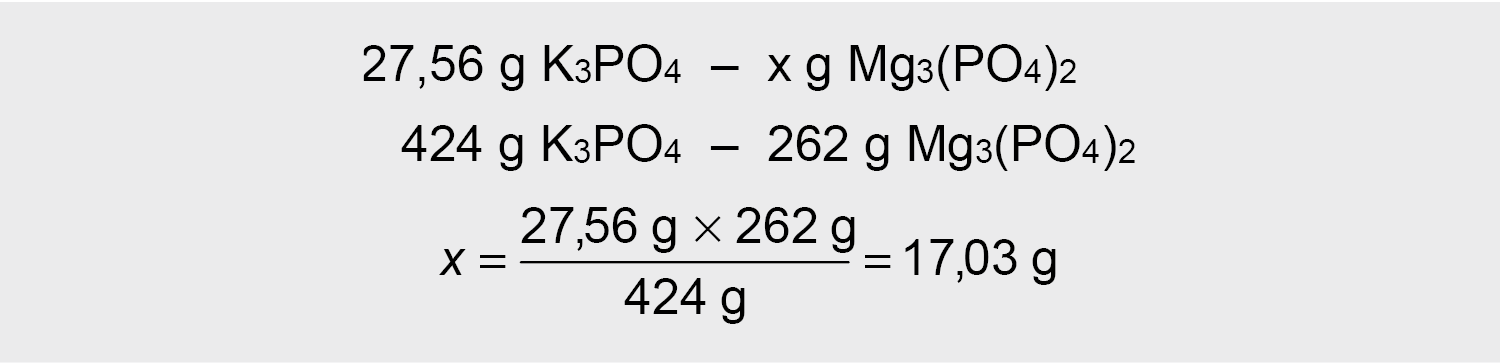
3. Kai vyksta kelios reakcijos lygiagrečiai
Uždavinys
15,5 g Al, Mg ir Cu miltelių mišinio buvo paveikta praskiestos druskos rūgšties – 5 % koncentracijos vandeninio HCl tirpalo – pertekliumi. Reakcijos metu išsiskyrė 7,84 litrai (n.s.) bespalvių ir bekvapių dujų. Neištirpęs metalų mišinio likutis buvo paveiktas koncentruotos nitrato(V) rūgšties – 65 % koncentracijos vandeninio HNO3 tirpalo – pertekliumi. Šios reakcijos metu išsiskyrė 5,6 litro (n.s.) rusvos spalvos, aštraus specifinio kvapo dujų. Apskaičiuokite kiekvieno metalo miltelių masę jų mišinyje.
Uždavinio sprendimas:
1. Pirmiausiai užrašomos ir išlyginamos miltelių mišinį sudarančių metalų reakcijų su parskiesta druskos rūgštimi HCl lygtys: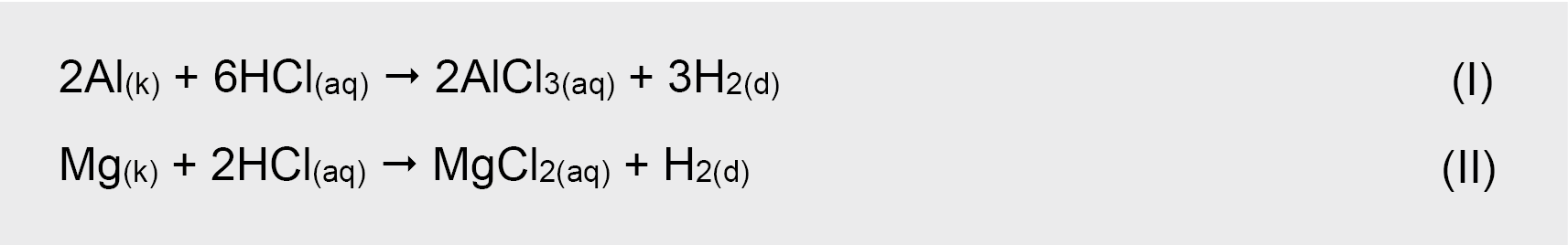
![]() → reakcija nevyksta, nes Cu yra neaktyvus metalas - aktyvumo eilėje Cu yra „už vandenilio“
→ reakcija nevyksta, nes Cu yra neaktyvus metalas - aktyvumo eilėje Cu yra „už vandenilio“
Vykstant reakcijoms (I) ir (II) išsiskiria bespalvės ir bekvapės vandenilio H2 dujos.
2. Po to užrašoma ir išlyginama su druskos rūgštimi nereagavusios miltelių dalies – Cu miltelių – reakcijos su koncentruota nitrato(V) rūgštimi HNO3 lygtis:
![]()
Vykstant reakcijai (III) išsiskyrė rusvos, aštraus specifinio kvapo NO2 dujos
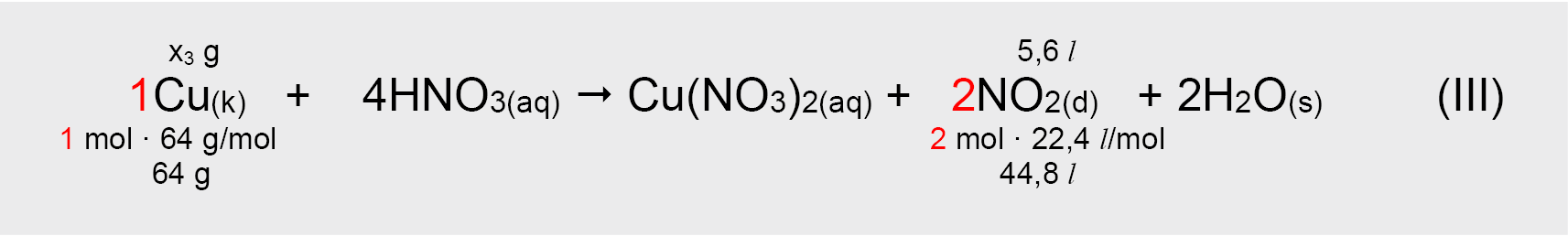
 – taip išreiškiama reakcijos (III) metu sureagavusių Cu miltelių masė.
– taip išreiškiama reakcijos (III) metu sureagavusių Cu miltelių masė.
4. Toliau surandama miltelių mišinyje esančių Al ir Mg miltelių bendra masė:

5. Bendrą Al ir Mg miltelių masę pažymėjus x1 + x2 = 7,5 g, remiantis reakcijų (I) ir (II) lygtimis apskaičiuojamos Al ir Mg miltelių masės x1 ir x2:
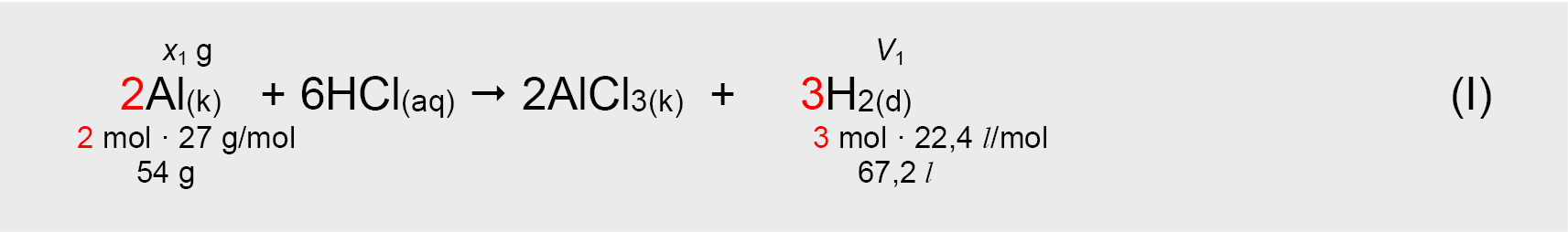
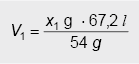 – taip išreiškiamas reakcijos (I) metu išsiskyrusių H2 dujų tūris.
– taip išreiškiamas reakcijos (I) metu išsiskyrusių H2 dujų tūris.

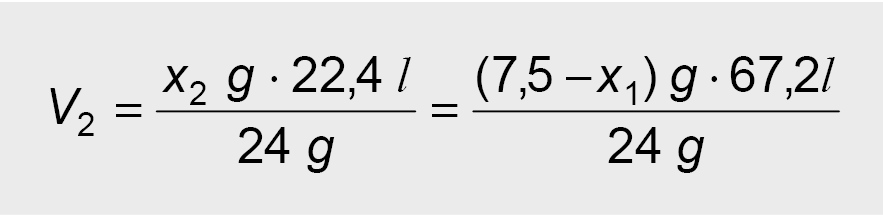 – taip išreiškiamas reakcijos (II) metu išsiskyrusių H2 dujų tūris.
– taip išreiškiamas reakcijos (II) metu išsiskyrusių H2 dujų tūris.
Bendras reakcijų (I) ir (II) metu išsiskyrusių H2 dujų tūris yra:
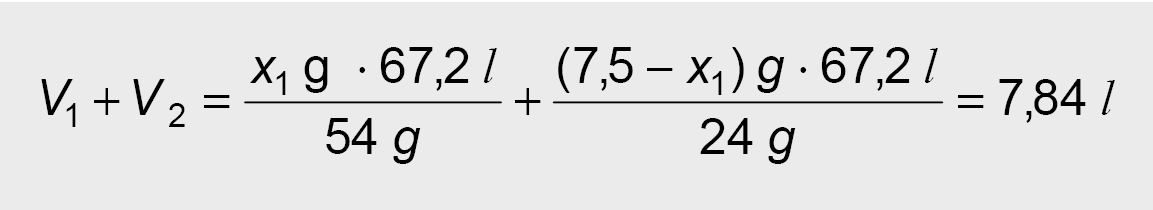
Išsprendus šią lygtį, surandama Al miltelių masė ![]()
Mg miltelių masė x2 apskaičiuojama taip:
![]()
Atsakymas: metalų miltelių mišinyje yra 2,7 g Al, 4,8 g Mg ir 8,0 g Cu.
4. Kai vyksta kelios reakcijos nuosekliai
Uždavinys
Sudeginus (iškaitinu) ore nežinomą masę cinko(II) sulfido ZnS, išsiskyrė specifinio aštraus kvapo bespalvės dujos. Šios dujos, praturtintos deguonimi, buvo praleistos virš įkaitinto V2O5 katalizatoriaus. Virš jo praėjusių karštų dujų mišinys – katalizinės reakcijos produktas su nesureagavusio deguonies pertekliumi – buvo praleistas pro vandenį. Gautas rūgštinis tirpalas, kurio neutralizacijai buvo sunaudota 20 ml 1,0 mol/l koncentracijos NaOH tirpalo. Apskaičiuokite sudeginto ore ZnS masę.
Uždavinio sprendimas:
1. Pirmiausiai užrašomos ir išlyginamos visų nuosekliai vykstančių reakcijų lygtys:

2. Toliau apskaičiuojama paskutinėje, (IV) reakcijoje dalyvavusio NaOH kiekis moliais:
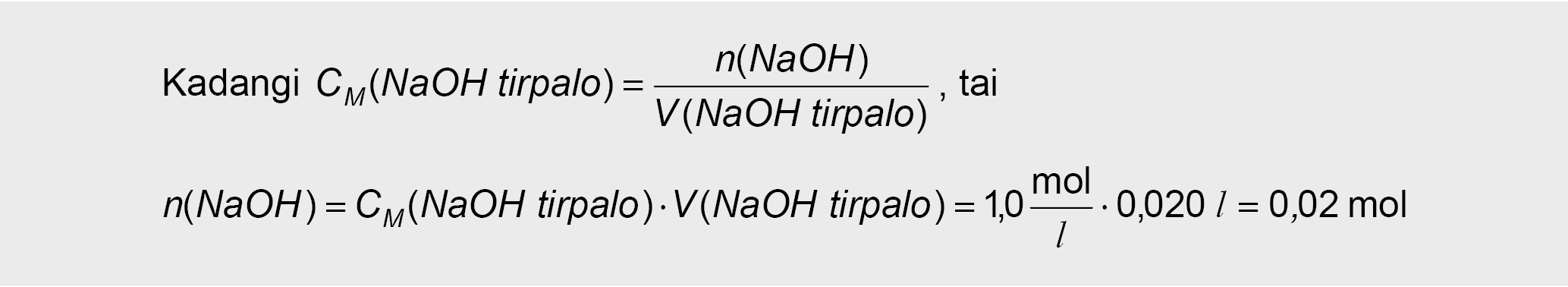
3. Pradedant (VI) ir baigiant (I) reakcijos lygtimi, nuosekliai yra skaičiuojama:
(VI) reakcijoje su NaOH sureagavusios H2SO4 kiekis n4, kuris taip pat yra lygus (III) reakcijoje susidariusios H2SO4 kiekiui

(III) reakcijoje sureagavusios SO3 kiekis n3, kuris taip pat yra lygus (II) reakcijoje susidariusio SO3 kiekiui
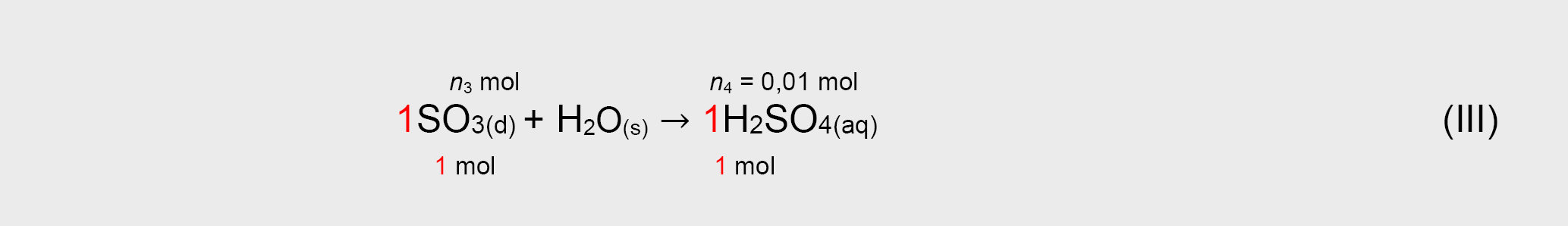
(II) reakcijoje sureagavusios SO2 kiekis n2, kuris taip pat yra lygus (I) reakcijoje susidariusio SO2 kiekiui
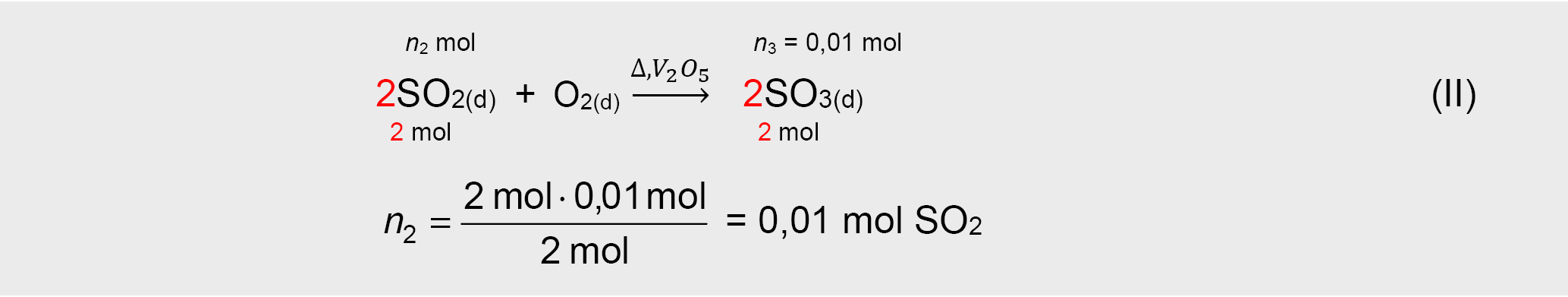
(I) reakcijoje sureagavusio ZnS kiekis n1
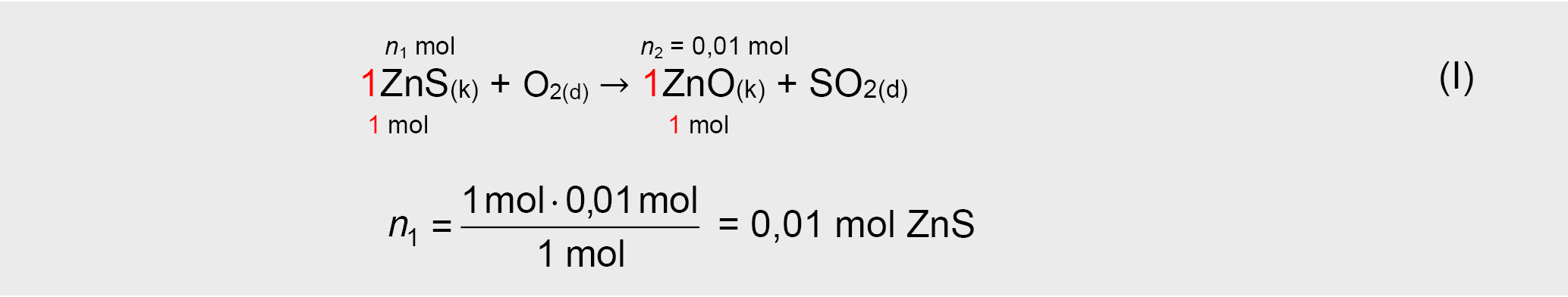
4. Apskaičiuojama (I) reakcijoje reagavusio ZnS masė:

Atsakymas: sudeginto (iškaitinto) ore ZnS masė yra 0,97 g
5. Kai vyksta kelios reakcijos lygiagrečiai ir nuosekliai
Uždavinys
Sudeginus 5 litru (n.s.) dujų mišinio, kurį sudaro 40 % (tūrio) metano ir 60 % (tūrio) propano dujos, gauti degimo produktai buvo praleisti pro perteklių Ba(OH)2 tirpalo. Reakcijos metu tirpalas drumstė, jame susidarė baltų nuosėdų. Kokios medžiagos nuosėdos ir kokia jų masė susidarė?
Uždavinio sprendimas:
1. Pirmiausiai užrašomos ir išlyginamos metano CH4 ir propano C3H8 degimo reakcijų lygtys:
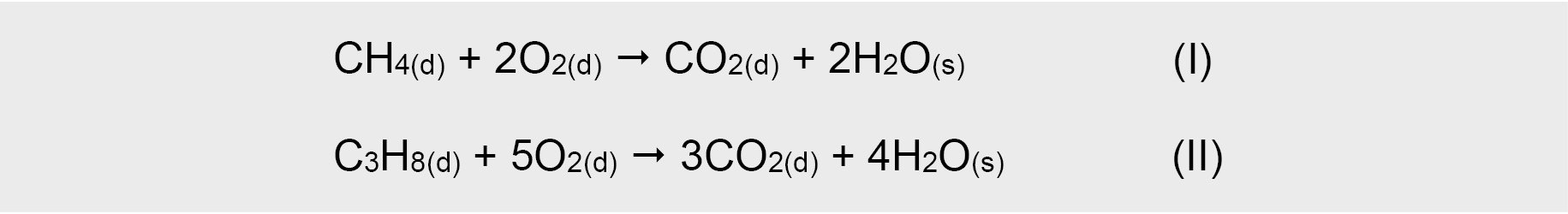
2. Apskaičiuojami metano ir propano dujų tūriai mišinyje:
- Kadangi metanas dujų mišinyje sudaro 40 % (tūrio), tai reiškia:
100 litrų dujų mišinio yra 40 litrų CH4
5 litruose dujų mišinio yra x1 litrų CH4
Iš proporcijos apskaičiuojamas CH4 dujų tūris
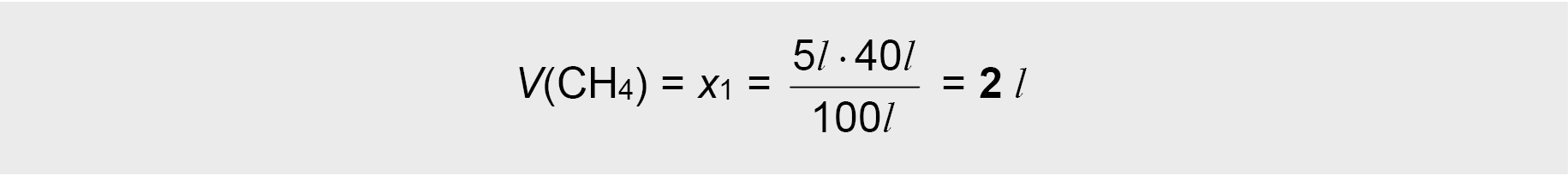
- Kadangi propanas dujų mišinyje sudaro 60 % (tūrio), tai reiškia:
100 litrų dujų mišinio yra 60 litrų C3H8
5 litruose dujų mišinio yra x2 litrų C3H8
Iš proporcijos apskaičiuojamas C3H8 dujų tūris
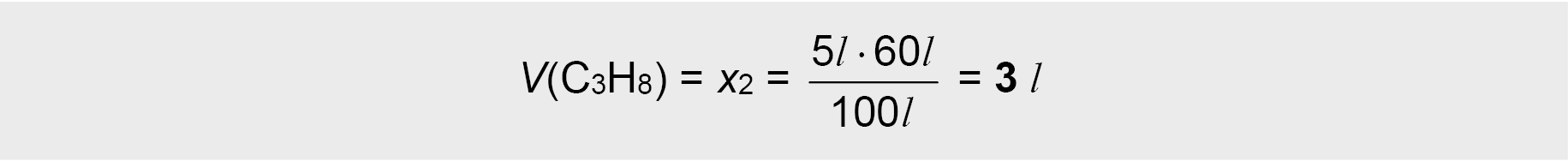
- C3H8 dujų tūris gali būti apskaičiuojamas ir taip:
3. Apskaičiuojami metano ir propano dujų kiekiai mišinyje:

4. Apskaičiuojamas kiekvienos degimo reakcijos metu susidariusių CO2 dujų kiekis:
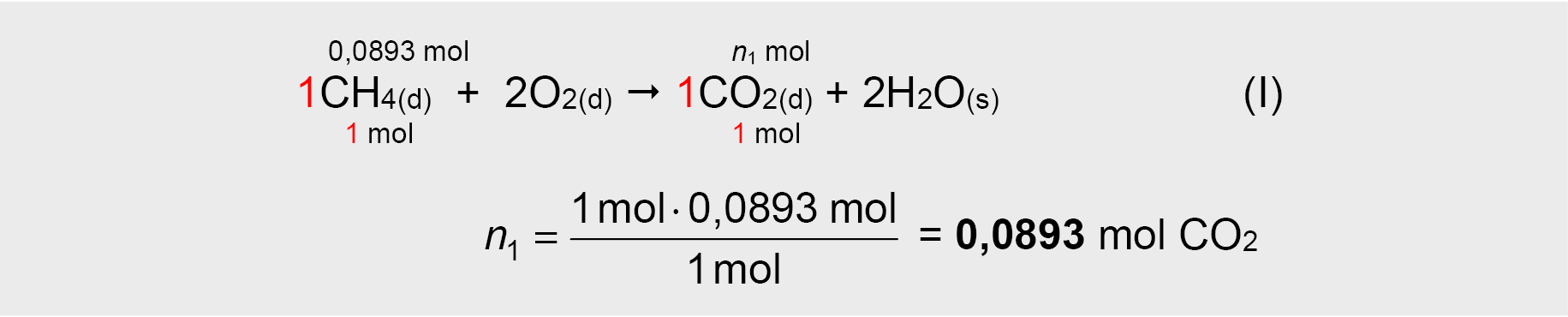
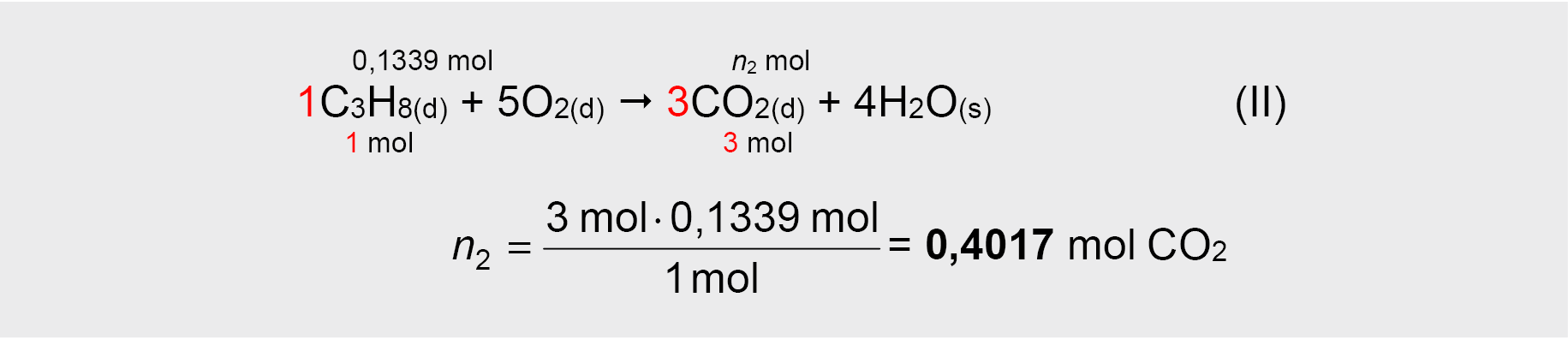
5. Apskaičiuojamas bendras abiejų degimo reakcijų metu susidariusių CO2 dujų kiekis:
![]()
6. Užrašoma ir išlyginama degimo produkto CO2 reakcijos su Ba(OH)2 lygtis ir pagal ją apskaičiuojama tirpale susidariusio netirpaus bario karbonato BaCO3 (baltų nuosėdų) kiekis, o po to – masė:
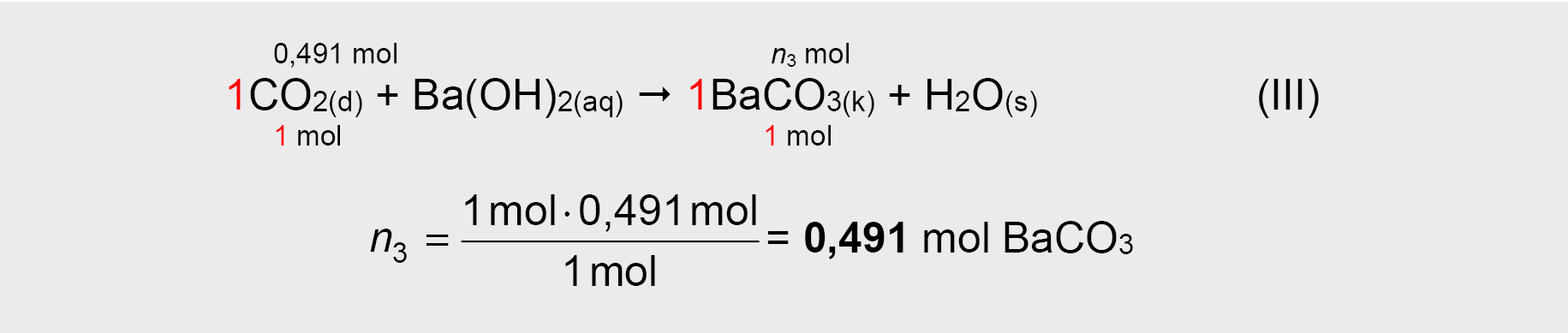
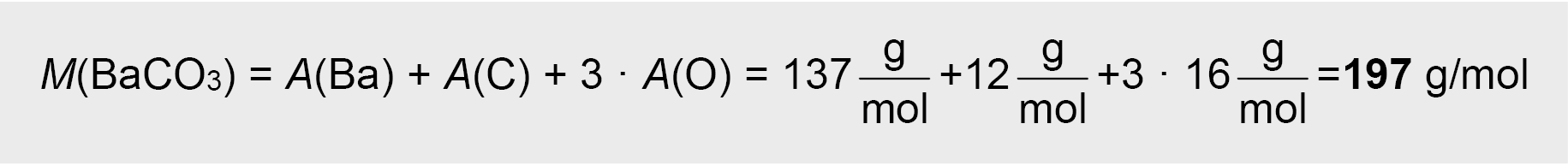
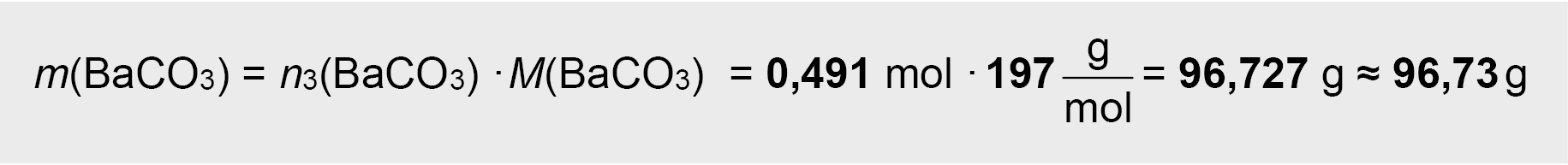
Atsakymas: susidarė 96,73 g BaCO3 nuosėdų.
6. Kai reikia įvertinti reakcijų išeigas
Apibrėžimas ir paaiškinimai
Išeiga – tai chemijoje bei įvairiose gamybos srityse vartojamas terminas, apibūdinantis iš pradinių medžiagų, reagentų, žaliavų ir pan., gaunamo produkto kiekį, masę ar tūrį.
- Atskiros reakcijos išeiga yra jos metu praktiškai gauto produkto kiekio, masės arba tūrio santykis su teoriškai pagal reakcijos lygtį apskaičiuotu to produkto kiekiu, mase arba tūriu, išreikštas procentais;
- Kartais išeiga gali būti išreiškiama gauto produkto ir jo gavimui sunaudotos medžiagos (žaliavos) masių santykiu, išreikštu procentais;
- Išeiga dažnai žymima simboliu η (gr. „eta“).
Uždavinys Nr. 1
Perdirbant naftą yra gaunama labai daug įvairių jos perdirbimo produktų. Tačiau didžiausią dalį sudaro degalai – benzinas ir dyzelinas. Benzinas – tai degus skystis, priskiriamas lengvajai arba lakiajai naftos distiliacijos frakcijai ir daugiausiai susidedantis iš angliavandenilių, kurių molekulės turi nuo 6 iki 8 anglies atomų, mišinio. Dyzelinas – tai degus, tačiau mažiau lakus nei benzinas, skystis, priskiriamas vidutinei naftos distiliacijos frakcijai ir daugiausiai susidedantis iš angliavandenilių, kurių molekulės turi nuo 9 iki 20 anglies atomų, mišinio. Apskaičiuokite benzino ir dyzelino išeigas, jeigu žinoma, jog naftos perdirbimo gamykla per parą perdirba 15000 tonų naftos ir pagamina 4600 tonų benzino ir 8700 tonų dyzelino.
Uždavinio sprendimas:
1. Pirmiausiai užrašomos benzino ir dyzelino išeigų apskaičiavimui naudojamos matematinės formulės:

2. Pagal užrašytas matematines formules apskaičiuojamos benzino ir dyzelino išeigos, paimant per vieną parą perdirbamos naftos ir gaunamo benzino ir dyzelino mases:

Atsakymas: iš perdirbamos naftos gaunamo benzino išeiga – 30,67 %, o dyzelino išeiga – 58,00 %.
Uždavinys Nr. 2
Ore sudeginus 5,0 g baltojo fosforo, jo degimo produktas buvo ištirpintas 100 g vandens. Kurios medžiagos ir kokios procentinės koncentracijos tirpalas buvo gautas, jeigu baltojo fosforo degimo produkto išeiga h = 90 % ?
Uždavinio sprendimas:
1. Pirmiausiai užrašomos visų vykusių reakcijų lygtys:
P4(k) + 5O2(d) → 2P2O5(k) baltojo fosforo P4 degimas (oksidacija)
P2O5(k) + 3H2O(s) → 2H3PO4(aq) ortofosfato(V) rūgšties susidarymas
2. Pagal pirmąją reakcijos lygtį apskaičiuojama teorinė susidariusio fosforo(V) oksido masė x1:
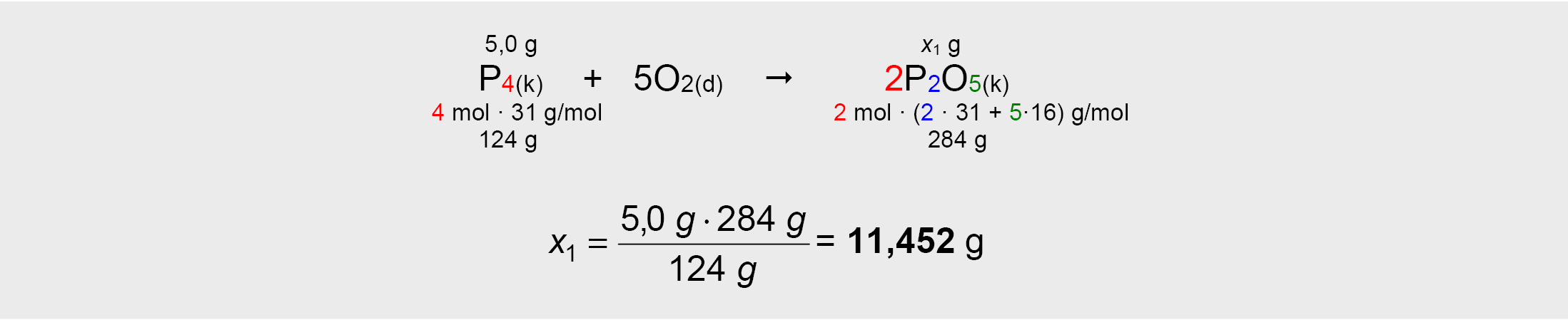
Tai teorinė susidariusio fosforo(V) oksido P2O5 masė.
3. Įvertinus fosforo(V) oksido P2O5 susidarymo reakcijos išeigą, apskaičiuojama tikroji fosforo(V) oksido P2O5 masė x2:
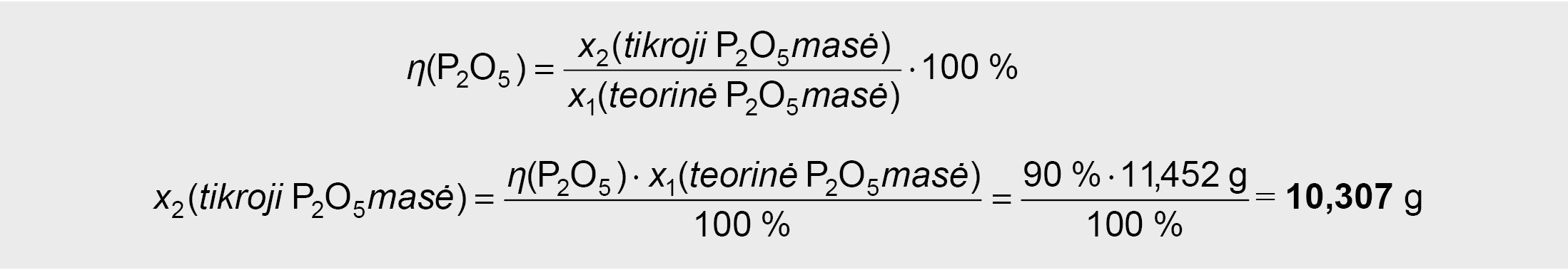
4. Pagal antrąją reakcijos lygtį, imant tikrąją fosforo(V) oksido P2O5 masę x2, apskaičiuojama susidariusios ortofosfato(V) rūgšties masė x3. Kadangi sąlygoje antrosios reakcijos išeiga neminima, todėl laikoma, kad ji yra lygi 100 %, t.y. praktinė susidariusios ortofosfato(V) rūgšties masė yra lygi teorinei masei x3:
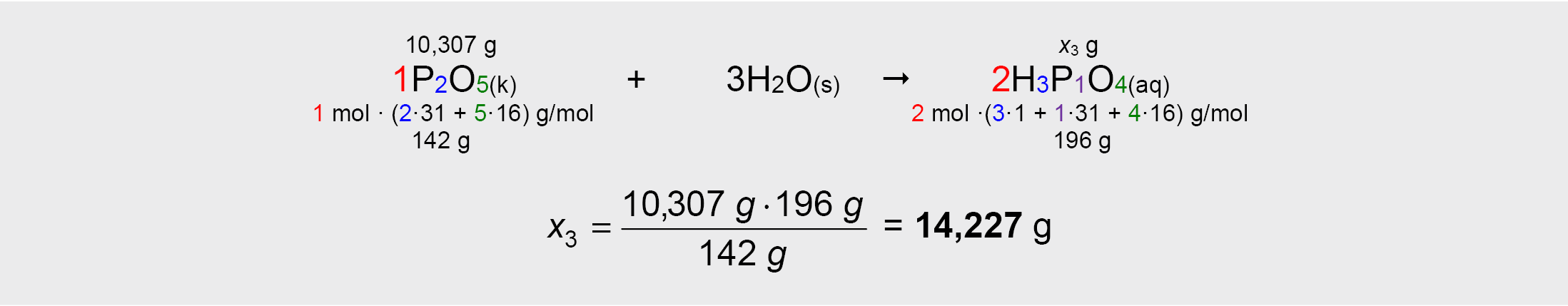
Tai teorinė susidariusio ortofosfato(V) rūgšties H3PO4 masė, sutampanti su praktine jos mase.
5. Apskaičiuojama gauto ortofosfato(V) rūgšties H3PO4 tirpalo masė:
![]()
Atkreipkite dėmesį: dalis vandens sureagavo su fosforo(V) oksidu P2O5 susidarant ortofosfato(V) rūgščiai H3PO4, o likęs vanduo yra tirpiklis, kuriame ši rūgštis ištirpsta susidarant jos tirpalui.
6. Apskaičiuojama ortofosfato(V) rūgšties H3PO4 procentinė (masės dalies) koncentracija gautame tirpale:
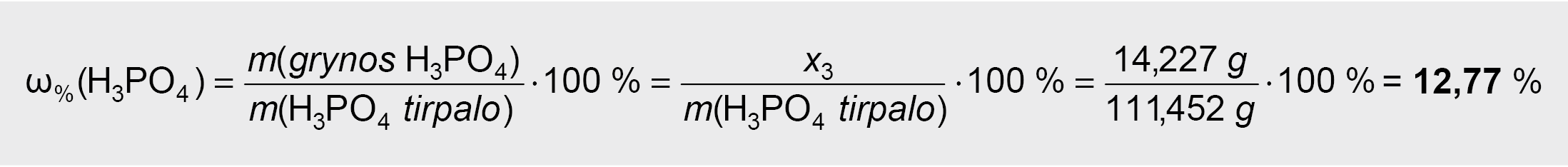
Atsakymas: buvo gautas 12,77 %, koncentracijos ortofosfato(V) rūgšties H3PO4 tirpalas.
Uždavinys Nr. 3
Vykdant amoniako sintezę iš N2 ir H2 dujų, optimaliomis sąlygomis grįžtamosios reakcijos metu susidarančio NH3 išeiga siekia 72 %. Apskaičiuokite, kokio tūrio (n.s.) N2 ir H2 reikia, norint gauti 1 m3 (n.s.) amoniako NH3.
Uždavinio sprendimas:
1. Pirmiausiai užrašomo amoniako sintezės reakcijos lygtis:
![]()
2. Kadangi sąlygoje nurodytas 1 m3 (n.s.) amoniako NH3 tūris yra norimo gauti amoniako tūris arba praktinis tūris, todėl apskaičiuojamas teorinis amoniako NH3 tūris (n.s.), kuris būtų gautas idealiu atveju, t.y. kai reakcijos išeiga būtų lygi 100 %:

3. Pagal reakcijos lygtį apskaičiuojami H2 ir N2 dujų tūriai (n.s.), imant iš jų gaunamo amoniako NH3 teorinį tūrį, t.y. tokį tūrį, kuris būtų gautas idealiu atveju, kai amoniako sintezė vyksta be nuostolių:
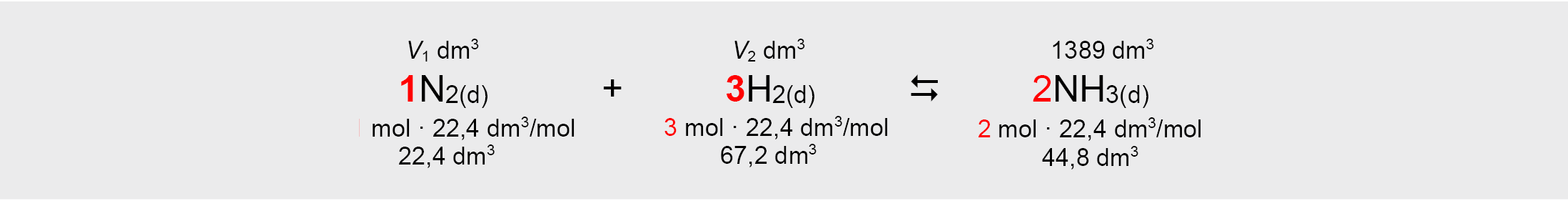

Tai reikalingas N2 dujų tūris (n.s.)

Tai reikalingas H2 dujų tūris (n.s.)
Atkreipkite dėmesį: apskaičiuotas N2 ir H2 dujų tūrių (n.s.) santykis yra toks pat, kaip reakcijoje dalyvaujančių N2 ir H2 molekulių (molių) skaičiaus santykis, t.y.:

Atsakymas: norint gauti 1 m3 (n.s.) amoniako NH3 reikia 694,5 dm3 (n.s.) N2 ir 2083,5 dm3 (n.s.) H2 dujų.