Uždaviniai ir jų sprendimas
6. Kai reikia įvertinti reakcijų išeigas
Apibrėžimas ir paaiškinimai
Išeiga – tai chemijoje bei įvairiose gamybos srityse vartojamas terminas, apibūdinantis iš pradinių medžiagų, reagentų, žaliavų ir pan., gaunamo produkto kiekį, masę ar tūrį.
- Atskiros reakcijos išeiga yra jos metu praktiškai gauto produkto kiekio, masės arba tūrio santykis su teoriškai pagal reakcijos lygtį apskaičiuotu to produkto kiekiu, mase arba tūriu, išreikštas procentais;
- Kartais išeiga gali būti išreiškiama gauto produkto ir jo gavimui sunaudotos medžiagos (žaliavos) masių santykiu, išreikštu procentais;
- Išeiga dažnai žymima simboliu η (gr. „eta“).
Uždavinys Nr. 1
Perdirbant naftą yra gaunama labai daug įvairių jos perdirbimo produktų. Tačiau didžiausią dalį sudaro degalai – benzinas ir dyzelinas. Benzinas – tai degus skystis, priskiriamas lengvajai arba lakiajai naftos distiliacijos frakcijai ir daugiausiai susidedantis iš angliavandenilių, kurių molekulės turi nuo 6 iki 8 anglies atomų, mišinio. Dyzelinas – tai degus, tačiau mažiau lakus nei benzinas, skystis, priskiriamas vidutinei naftos distiliacijos frakcijai ir daugiausiai susidedantis iš angliavandenilių, kurių molekulės turi nuo 9 iki 20 anglies atomų, mišinio. Apskaičiuokite benzino ir dyzelino išeigas, jeigu žinoma, jog naftos perdirbimo gamykla per parą perdirba 15000 tonų naftos ir pagamina 4600 tonų benzino ir 8700 tonų dyzelino.
Uždavinio sprendimas:
1. Pirmiausiai užrašomos benzino ir dyzelino išeigų apskaičiavimui naudojamos matematinės formulės:

2. Pagal užrašytas matematines formules apskaičiuojamos benzino ir dyzelino išeigos, paimant per vieną parą perdirbamos naftos ir gaunamo benzino ir dyzelino mases:

Atsakymas: iš perdirbamos naftos gaunamo benzino išeiga – 30,67 %, o dyzelino išeiga – 58,00 %.
Uždavinys Nr. 2
Ore sudeginus 5,0 g baltojo fosforo, jo degimo produktas buvo ištirpintas 100 g vandens. Kurios medžiagos ir kokios procentinės koncentracijos tirpalas buvo gautas, jeigu baltojo fosforo degimo produkto išeiga h = 90 % ?
Uždavinio sprendimas:
1. Pirmiausiai užrašomos visų vykusių reakcijų lygtys:
P4(k) + 5O2(d) → 2P2O5(k) baltojo fosforo P4 degimas (oksidacija)
P2O5(k) + 3H2O(s) → 2H3PO4(aq) ortofosfato(V) rūgšties susidarymas
2. Pagal pirmąją reakcijos lygtį apskaičiuojama teorinė susidariusio fosforo(V) oksido masė x1:
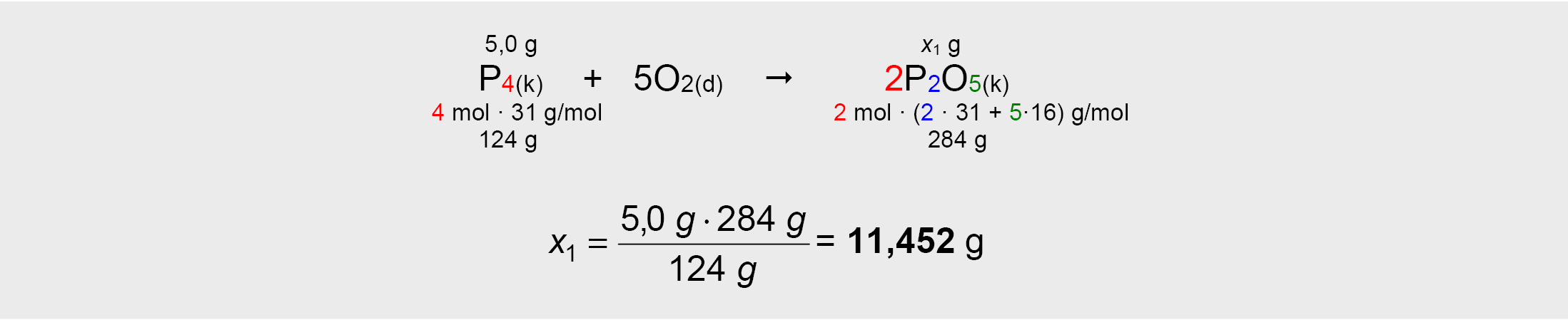
Tai teorinė susidariusio fosforo(V) oksido P2O5 masė.
3. Įvertinus fosforo(V) oksido P2O5 susidarymo reakcijos išeigą, apskaičiuojama tikroji fosforo(V) oksido P2O5 masė x2:
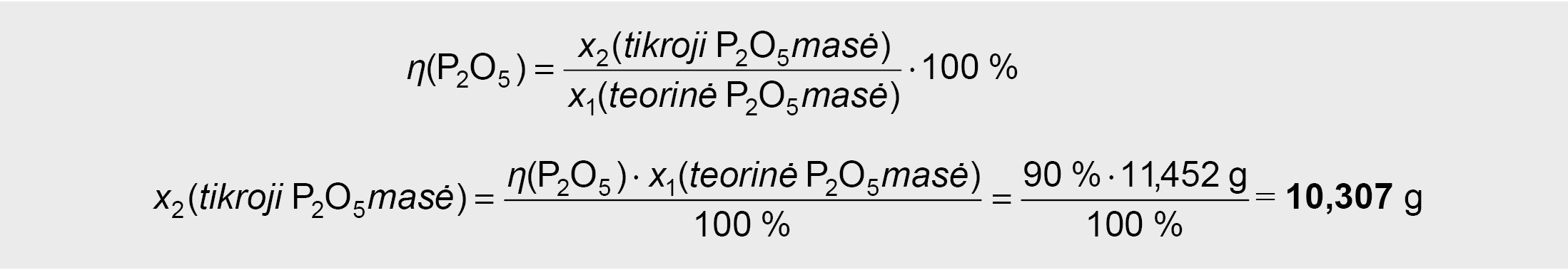
4. Pagal antrąją reakcijos lygtį, imant tikrąją fosforo(V) oksido P2O5 masę x2, apskaičiuojama susidariusios ortofosfato(V) rūgšties masė x3. Kadangi sąlygoje antrosios reakcijos išeiga neminima, todėl laikoma, kad ji yra lygi 100 %, t.y. praktinė susidariusios ortofosfato(V) rūgšties masė yra lygi teorinei masei x3:
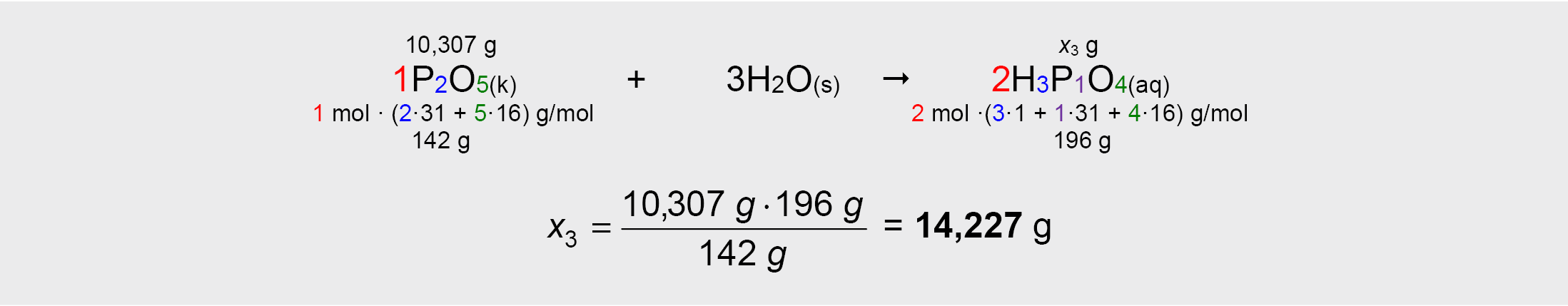
Tai teorinė susidariusio ortofosfato(V) rūgšties H3PO4 masė, sutampanti su praktine jos mase.
5. Apskaičiuojama gauto ortofosfato(V) rūgšties H3PO4 tirpalo masė:
![]()
Atkreipkite dėmesį: dalis vandens sureagavo su fosforo(V) oksidu P2O5 susidarant ortofosfato(V) rūgščiai H3PO4, o likęs vanduo yra tirpiklis, kuriame ši rūgštis ištirpsta susidarant jos tirpalui.
6. Apskaičiuojama ortofosfato(V) rūgšties H3PO4 procentinė (masės dalies) koncentracija gautame tirpale:
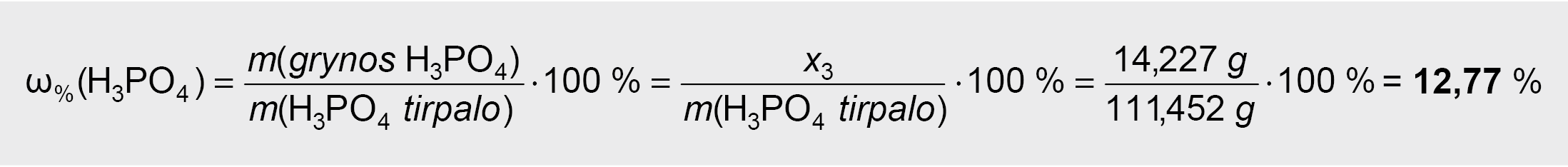
Atsakymas: buvo gautas 12,77 %, koncentracijos ortofosfato(V) rūgšties H3PO4 tirpalas.
Uždavinys Nr. 3
Vykdant amoniako sintezę iš N2 ir H2 dujų, optimaliomis sąlygomis grįžtamosios reakcijos metu susidarančio NH3 išeiga siekia 72 %. Apskaičiuokite, kokio tūrio (n.s.) N2 ir H2 reikia, norint gauti 1 m3 (n.s.) amoniako NH3.
Uždavinio sprendimas:
1. Pirmiausiai užrašomo amoniako sintezės reakcijos lygtis:
![]()
2. Kadangi sąlygoje nurodytas 1 m3 (n.s.) amoniako NH3 tūris yra norimo gauti amoniako tūris arba praktinis tūris, todėl apskaičiuojamas teorinis amoniako NH3 tūris (n.s.), kuris būtų gautas idealiu atveju, t.y. kai reakcijos išeiga būtų lygi 100 %:

3. Pagal reakcijos lygtį apskaičiuojami H2 ir N2 dujų tūriai (n.s.), imant iš jų gaunamo amoniako NH3 teorinį tūrį, t.y. tokį tūrį, kuris būtų gautas idealiu atveju, kai amoniako sintezė vyksta be nuostolių:
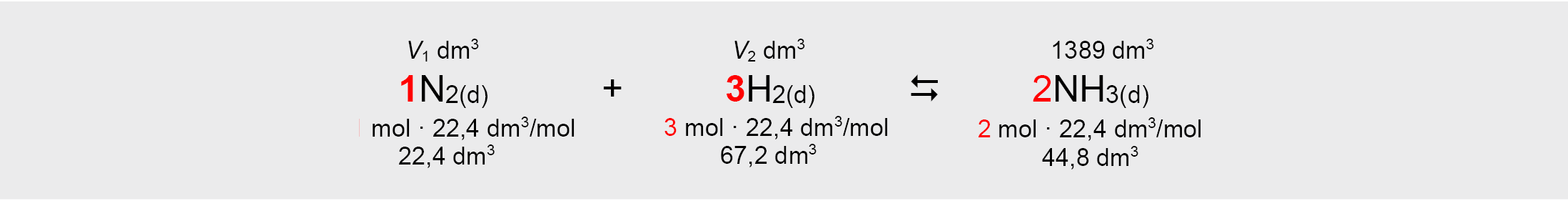

Tai reikalingas N2 dujų tūris (n.s.)

Tai reikalingas H2 dujų tūris (n.s.)
Atkreipkite dėmesį: apskaičiuotas N2 ir H2 dujų tūrių (n.s.) santykis yra toks pat, kaip reakcijoje dalyvaujančių N2 ir H2 molekulių (molių) skaičiaus santykis, t.y.:

Atsakymas: norint gauti 1 m3 (n.s.) amoniako NH3 reikia 694,5 dm3 (n.s.) N2 ir 2083,5 dm3 (n.s.) H2 dujų.
