Uždaviniai ir jų sprendimas
4. Kai vyksta kelios reakcijos nuosekliai
Uždavinys
Sudeginus (iškaitinu) ore nežinomą masę cinko(II) sulfido ZnS, išsiskyrė specifinio aštraus kvapo bespalvės dujos. Šios dujos, praturtintos deguonimi, buvo praleistos virš įkaitinto V2O5 katalizatoriaus. Virš jo praėjusių karštų dujų mišinys – katalizinės reakcijos produktas su nesureagavusio deguonies pertekliumi – buvo praleistas pro vandenį. Gautas rūgštinis tirpalas, kurio neutralizacijai buvo sunaudota 20 ml 1,0 mol/l koncentracijos NaOH tirpalo. Apskaičiuokite sudeginto ore ZnS masę.
Uždavinio sprendimas:
1. Pirmiausiai užrašomos ir išlyginamos visų nuosekliai vykstančių reakcijų lygtys:

2. Toliau apskaičiuojama paskutinėje, (IV) reakcijoje dalyvavusio NaOH kiekis moliais:
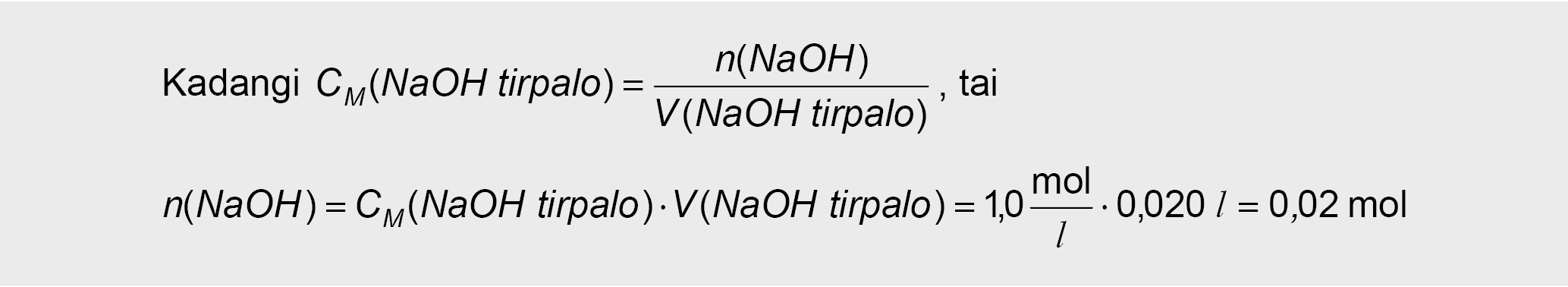
3. Pradedant (VI) ir baigiant (I) reakcijos lygtimi, nuosekliai yra skaičiuojama:
(VI) reakcijoje su NaOH sureagavusios H2SO4 kiekis n4, kuris taip pat yra lygus (III) reakcijoje susidariusios H2SO4 kiekiui

(III) reakcijoje sureagavusios SO3 kiekis n3, kuris taip pat yra lygus (II) reakcijoje susidariusio SO3 kiekiui
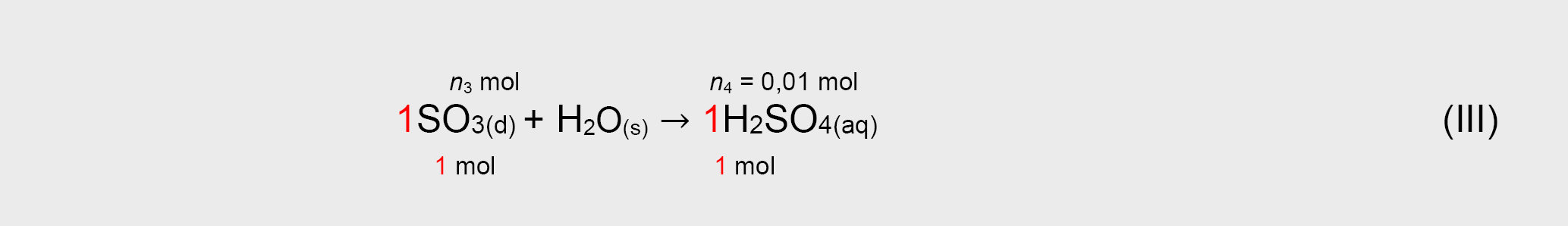
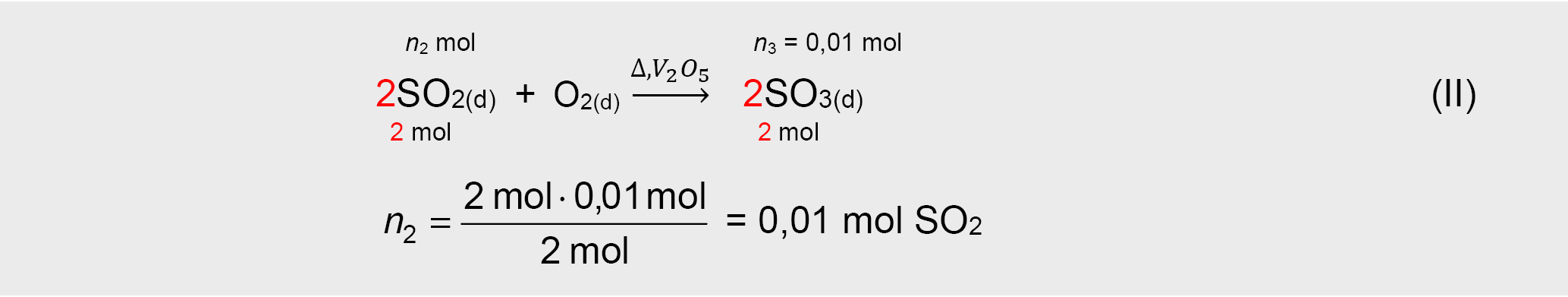
(II) reakcijoje sureagavusios SO2 kiekis n2, kuris taip pat yra lygus (I) reakcijoje susidariusio SO2 kiekiui
(I) reakcijoje sureagavusio ZnS kiekis n1
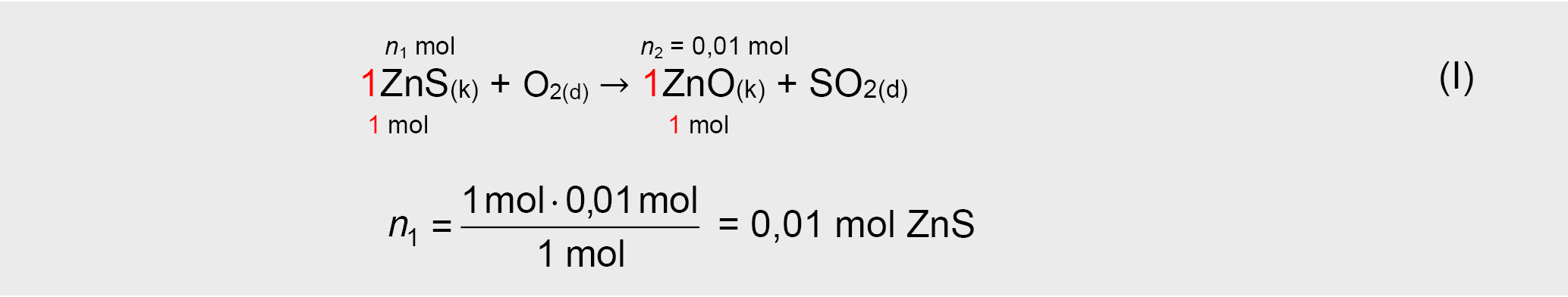
4. Apskaičiuojama (I) reakcijoje reagavusio ZnS masė:

Atsakymas: sudeginto (iškaitinto) ore ZnS masė yra 0,97 g
