Teorinė medžiaga
7.2. Oras
7.2.3. Atmosferos ozono sluoksnis
Ozonas – tai alotropinė deguonies atmaina. Ozono molekules sudaro trys O atomai. Ozono cheminė formulė yra O3.
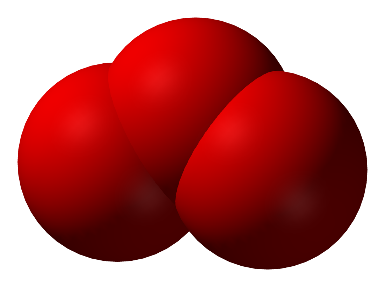
O3 molekulės rutulinis modelis
Grynas O3 yra melsvos, aštraus dirginančio kvapo dujos (tvir.=-112 oC; tlyd.= -192,2 oC). Skystas O3 yra tamsiai mėlynas, o kietas – tamsiai violetinis. Ozonas susidaro iš dviatomių deguonies molekulių O2 , jas veikiant ultravioletine spinduliuote (UV), elektros išlydžiu.
UV
3O2(d) → 2O3(d)
Ozono sluoksnį atmosferoje sudaro O3, esantis stratosferoje 10-50 km aukštyje ir apsaugantis Žemę nuo žalingų ultravioletinių (UV) spindulių, sklindančių iš Saulės, poveikio. Stratosferoje yra susikaupę ~90% viso atmosferoje esančio O3. Ozono sluoksnio storis matuojamas santykiniais Dobsono vienetais (žymima DV).
1 DV atitinka 0,01 mm ozono sluoksnio storį esant 0 oC temperatūrai ir 101,325 kPa slėgiui. Vidutinis ozono sluoksnio storis Žemės atmosferoje yra apie 300 DV. Tai reiškia, jeigu sugebėtume visą O3 „suspausti“ į vieną sluoksnį, jo storis esant 0 oC temperatūrai ir 760 mmHg slėgiui būtų apie 3 mm.
Kadangi O3 yra labai reaktyvus, su juo reaguoti ir taip ardyti ozono sluoksnį gali daugelis į stratosferą patenkančių medžiagų. Ypač pavojingi junginiai ir radikalai (dalelės, kurių atomai turi nesuporuotų elektronų), katalizuojantys O3 skilimo reakciją. Tai azoto oksidai NO ir N2O, hidroksilas (hidroksilo radikalas) HO·, chloro atomas (radikalas) Cl·. Ypač reakcingi ardant O3 yra chloro atomai, kurie susidaro iš į atmosferą „išmestų“ halogenintų, t.y. fluoro, chloro ir bromo atomų turinčių angliavandenilių, populiariai vadinamų freonų. Tai paprasčiausių angliavandenilių – metano (CH4) ir etano (C2H6) – molekulių dariniai, gauti visus arba dalį H atomų šiose molekulėse pakeitus F, Cl ir Br atomais. Šie junginiai yra labai inertiški. Ilgą laiką šaldytuvų, oro kondicionierių, aerozolių balionėlių gamyboje buvo naudojami du ypatingu cheminiu inertiškumu pasižymintys „kietieji“ freonai: trichlorfluormetanas CFCl3 (žymimas CFC-11) ir dichlordifluormetanas CF2Cl2 (žymimas CFC-12).
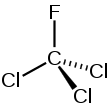
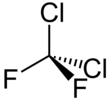

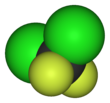
CFCl3 ir CF2Cl2 molekulių struktūrinės formulės (aukščiau) ir rutuliniai modeliai (žemiau)
Patekę į atmosferą, jie pasiekia stratosferą, kur veikiami ultravioletinių spindulių suskyla į laisvuosius radikalus. Ypač aktyvūs chloro radikalai Cl· reaguoja su O3 molekulėmis ir taip ardo ozono sluoksnį:
UV
CFCl3(d) → ·CFCl2(d) + Cl·(d)
Cl·(d) + O3(d) → O2(d) + ClO·(d)
ClO·(d) + O3(d) → 2O2(d) + Cl·(d)
