Teorinė medžiaga
| Надруковано: | Misafir kullanıcı |
| Дата: | суботу 30 травня 2026 14:03 PM |
7. Aplinkos chemija
Aplinkos chemija – tai mokslas apie įvairiausios kilmės medžiagų šaltinius, pernašą, chemines reakcijas bei kitokius virsmus aplinkoje. Aplinkos chemija susideda iš tarpusavyje labai glaudžiai susijusių dalių:
- Oro arba atmosferos chemijos
- Vandens arba hidrosferos chemijos
- Dirvožemio arba litosferos chemijos
- Gyvūnijos ir augmenijos arba biosferos chemijos (biochemijos)
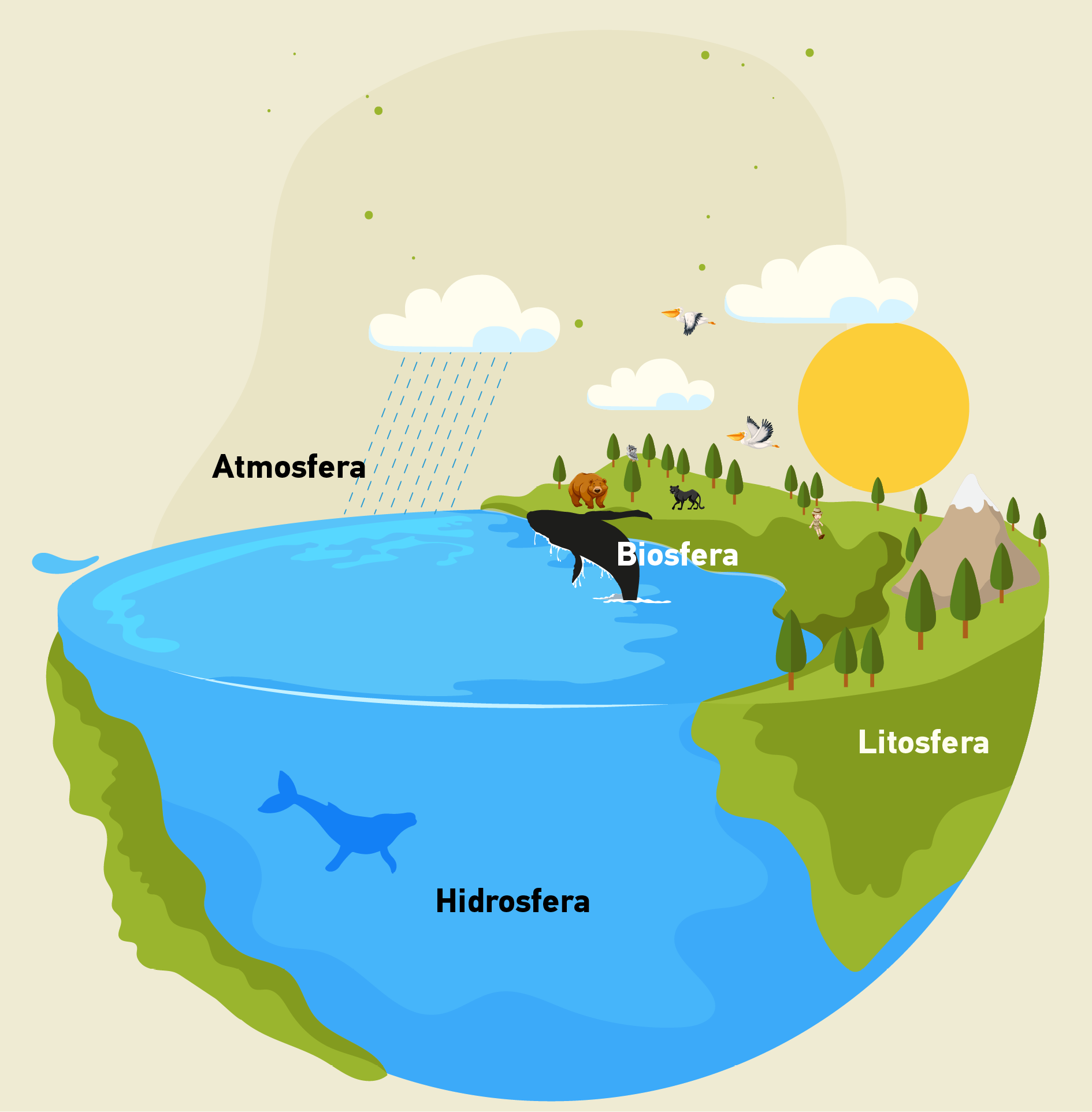
7.1. Aplinka ir jos komponentai
Aplinka – tai gamtoje funkcionuojanti sistema, sudaryta iš tarpusavyje susijusių natūraliųjų arba gamtinių bei žmogaus sukurtų komponentų.
Natūralieji arba gamtiniai komponentai dar skirstomi į negyvuosius ir gyvuosius. Pagrindiniai negyvieji aplinkos komponentai yra oras (Žemę gaubiantis dujų sluoksnis – atmosfera), vanduo (Žemės hidrosferoje, o taip pat atmosferoje esantis vanduo) ir dirvožemis (viršutinis, purus Žemės plutos sluoksnis), o gyvieji – augalija ir gyvūnija (iš pastarosios kartais dar yra išskiriama žmonija).
Pagrindiniai žmogaus sukurti aplinkos komponentai yra įvairūs statiniai (gyvenamieji, visuomeniniai bei gamybiniai pastatai, paminklai) ir įrenginiai (keliai, elektros ir ryšių linijos, vandentiekio, nuotekų ir kt. sistemos) bei transporto priemonės (riedančios, plaukiančios, skrendančios).
Visi šie paminėti aplinkos komponentai yra glaudžiai tarpusavyje susiję ir vieni kitus betarpiškai veikia tiek fiziškai, tiek chemiškai. Ypač didelį poveikį visiems kitiems aplinkos komponentams daro žmonija, vykdydama savo ūkinę ir gamybinę veiklą bei tenkindama kitus savo poreikius. Tai pirmiausiai pasireiškia nuolatos augančiu gamtos išteklių naudojimu. Gamtos ištekliai skirstomi į:
- Atsikuriančius arba biologinius, kurie atsikuria patys arba žmogui padedant;
- Neatsikuriančius, kurių kiekis gamtoje yra ribotas, o jų atsikūrimo greitis, palyginus su naudojimo tempais, yra labai lėtas.
Augantis gamtos išteklių naudojimas didina žmonijos neigiamą poveikį aplinkai, kuris pirmiausiai pasireiškia aplinkos tarša. Aplinkos tarša – tai cheminių, fizinių bei biologinių teršalų, kurie neigiamai veikia žmoniją, kitus gyvuosius organizmus ir negyvuosius aplinkos komponentus bei keičia cheminius ir fizinius aplinkos parametrus, patekimas į aplinką. Paprasčiau tariant, aplinkos tarša yra dėl gamtos išteklių naudojimo susidariusių buitinių ir gamybinių atliekų bei cheminių teršalų patekimas į aplinką. Cheminiai teršalai – tai cheminės medžiagos, jų junginiai ir mišiniai, kurie viršijus tam tikrą koncentraciją bei poveikio trukmę, daro neigiamą įtaką žmonėms (jų sveikatai ir gyvybei), kitiems gyviems organizmams bei negyviems aplinkos komponentams.
7.2. Oras
Oras – tai įvairių dujų mišinys, sudarantis Žemės atmosferą.
 |
 |
|---|
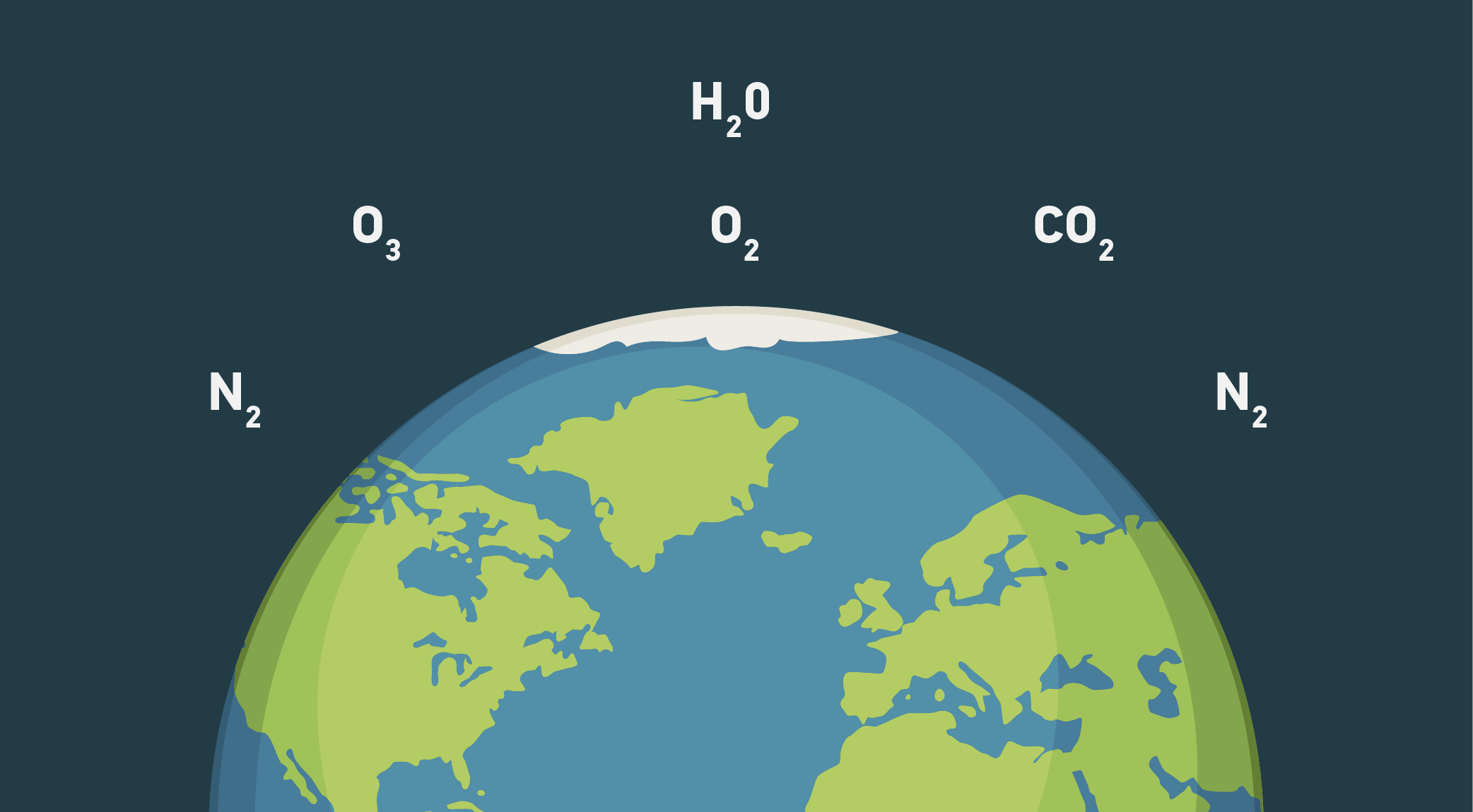
Sausą orą (be vandens garų) sudaro:
- azotas N2 – 78,1 % (tūrio);
- deguonis O2 – 20,9 % (tūrio),
- anglies dioksidas CO2 – 0,04 % (tūrio)
- argonas Ar – 0,93 % (tūrio)
- vandenilis H2, helis He, neonas Ne ir kitos dujos – 0,03 % (tūrio).
Orą sudarančių dujų tūrinių koncentracijų santykis sausame ore iki 80 km aukščio nuo žemės paviršiaus yra beveik pastovus ir vienodas bet kurioje pasaulio dalyje. Tačiau ore visada yra vandens garų (oro drėgmės), dulkių ir kitų dujinių teršalų, kurių koncentracija ore priklauso nuo vietovės.
Oro tankis, kai temperatūra 0 °C, o slėgis 101,325 kPa, yra apie 1,29 g/dm3. Oro molinė masė apytiksliai lygi 29 g/mol.
Svarbiusios oro dujos, kurios reikalingos gyvybei palaikyti Žemėje, yra deguonis O2 ir anglies dioksidas CO2 .
Dujinis azotas N2 yra chemiškai inertiškas ir atmosferoje gali reaguoti su kitu jos komponentu deguonimi O2 tik esant labai aukštai temperatūrai, pvz. žaibuojant ar degant kurui.
7.2.1. Oro tarša
Oro tarša – tai kenksmingų žmonėms bei kitiems organizmams arba pažeidžiančių aplinką medžiagų (dažniausiai dujinių) išmetimas į atmosferą. Pagrindiniai oro teršalai yra:
Anglies oksidai – anglies(II) oksidas (anglies monoksidas, smalkės) CO ir anglies(IV) oksidas (anglies dioksidas) CO2.
CO yra bespalvės, bekvapės, lengvesnės už orą (tankis 1,14 g/dm3, kai temperatūra 0 °C ir slėgis 101,325 kPa), nuodingos dujos. CO dujos susidaro anglies turinčio kuro nevisiško arba nepilno degimo metu, kai nepakanka deguonies O2, bei aukštoje temperatūroje reaguojant angliai C su anglies dioksidu CO2:
|
CH4(d) |
+ |
O2(d) |
→ |
CO(d) |
+ |
H2O(s) |
|
2C(k) |
+ |
O2(d) |
→ |
2CO(d) |
|
|
|
C(k) |
+ |
CO2(d) |
→ |
2CO(d) |
|
|
Norint išvengti CO susidarymo bei apsinuodijimo (ypač uždarose patalpose), būtina užtikrinti pakankamą oro deguonies tiekimą degančiam kurui bei gerai vėdinti patalpas.
Gerokai didesnė nei vidutinė CO2 koncentracija ore paprastai būna arti šiluminių elektrinių, katilinių, gamyklų, transporto magistralių, vandens ir oro uostų. Čia į orą „išmetami“ ypač dideli CO2 kiekiai degant įvairiausiam anglies turinčiam kurui, t.y. akmens anglims, medienai, durpėms, gamtinėms dujoms, perdirbtos naftos produktams (benzinui, dyzelinui, aviaciniam kurui, mazutui) bei anglies monoksidui CO.
|
CH4(d) |
+ |
2O2(d) |
→ |
CO2(d) |
+ 2H2O(s) |
|
|
C(k) |
+ |
O2(d) |
→ |
CO2(d) |
|
|
|
C9H20(s) |
+ |
14O2(d) |
→ |
9CO2(d) |
+ 10H2O(s) |
|
|
2CO(d) |
+ |
O2(d) |
→ |
2CO2(d) |
|
|
Sieros oksidai – sieros(IV) oksidas (sieros dioksidas) SO2 ir sieros(VI) oksidas (sieros trioksidas) SO3.
SO2 į atmosferą patenka deginant sieringą kurą (akmens anglyse, naftoje būna 2–3 % S, mazute iki 3,5 % S) bei metalurgijos gamyklose perdirbant (apdeginant ore) metalų sulfidų rūdas (mineralus):
|
S(k) |
+ |
O2(d) |
→ |
SO2(d) |
|
|
|
ZnS(k) |
+ |
3O2(d) |
→ |
ZnO(k) |
+ |
SO2(d) |
|
4FeS2(k) |
+ |
11O2(d) |
→ |
2Fe2O3(k) |
+ |
8SO2(d) |
Dalis į atmosferą patekusio SO2 yra oksiduojama oro deguonies iki SO3:
|
2SO2(d) |
+ |
O2(d) |
→ |
2SO3(s) |
|
|
Siekiant sumažinti oro taršą sieros oksidais, naftos perdirbimo metu iš jos yra šalinama siera ir gaminami mažo sieringumo degalai (dyzelinas, aviacinis kuras). Metalurgijos gamyklose susidarantis SO2 ten pat panaudojamas sieros rūgšties H2SO4 gamybai.
Azoto oksidai – azoto monoksidas NO, diazoto trioksidas N2O3, azoto dioksidas NO2 (bendrai žymimi formule NOx).
Šie oksidai yra fiziologiškai veiklios medžiagos, nepatvarūs ir nuodingi. Orą teršiančių NOx daugiausia susidaro degant bet kokiam kurui, kai aukštoje temperatūroje, o vidaus degimo ir reaktyviniuose varikliuose dar ir esant aukštam slėgiui, oro azotas N2 reaguoja su oro deguonimi O2. Natūraliai atmosferoje perkūnijos metu taip pat susidaro azoto monoksidas NO, kuris veikiamas oro deguonies virsta NO2.
|
N2(d) |
+ |
O2(d) |
→ |
NO(d) |
|
|
|
2NO(d) |
+ |
O2(d) |
→ |
2NO2(d) |
|
|
Šiuolaikinio transporto, varomo vidaus degimo varikliais ir naudojančio benziną bei dyzeliną, išmetamosiose dujose susidarę NOx yra nukenksminami dujų išmetimo sistemoje įrengtuose kataliziniuose konverteriuose Kadangi vidaus degimo varikliuose vyksta labai greitos kuro degimo (sprogimo) reakcijos, dalis kuro nepilnai sudega ir išmetamosiose dujose taip pat būna maži kiekiai anglies monoksido CO bei mažos molekulinės masė angliavandenilių (pvz. etano, eteno, propano, propeno), kurie bendrai žymimi CHx. Kataliziniame konverteryje aukštoje temperatūroje, ant specialiame filtre esančių tauriųjų metalų-katalizatorių platinos Pt, paladžio Pd, rodžio Rh mikro- ir nanodalelių paviršiaus vyksta pagreitintos NOx, CO ir CHx oksidacijos-redukcijos reakcijos:
Pt/Rh
NOx(d) → N2(d) + xO2(d)
Pt/Pd
2CO(d) + O2(d) → 2CO2(d)
Pt/Pd
C2H4(d) + 3O2(d) → 2CO2(d)
+ 2H2O(s)
https://www.youtube.com/watch?v=O1iSgouiEPk
Tokiu būdu iš katalizinio konverterio išeina visiškai nekenksmingų azoto N2 dujų, vandens garų H2O bei anglies dioksido CO2 dujų mišinys, kuris gerokai mažiau teršia orą. Deja, bet tokių katalizinių konverterių techniškai neįmanoma įrengti lėktuvų reaktyvinių variklių išmetamųjų dujų nukenksminimui, todėl aviacija išlieka labiausiai azoto oksidais orą teršiančiu transportu.
Apskritai, dėl į orą patenkančių didelių kiekių sieros ir azoto oksidų atmosferoje vyksta „rūgščiųjų kritulių“ susidarymo procesas. Apie šį reiškinį daugiau sužinosite skyriuje „Rūgštieji krituliai“.
Kietosios dalelės – dulkės, suodžiai ir kt.
Dujiniai bei lakieji organiniai ir neorganiniai junginiai: metanas CH4 ir kiti angliavandeniliai, žemą virimo temperatūrą turintys organiniai junginiai (pvz., įvairūs tirpikliai, freonai ir kt.), amoniakas NH3, vandenilio sulfidas H2S.
7.2.2. Rūgštieji krituliai
Rūgštieji krituliai – tai reiškinys, kai atmosferos krituliai (lietus, sniegas) parūgštėja (pH<5) dėl oro taršos rūgštiniais oksidais (SO2, NOx) bei šių oksidų tolesnės oksidacijos ir reakcijos su vandeniu metu susidarančių produktų – sulfato (sieros) rūgšties H2SO4 ir nitrato (azoto) rūgšties HNO3. Kartais šis reiškinys vadinamas rūgščiuoju lietumi. Apie šių oksidų susidarymą ir patekimą į orą (atmosferą) aprašyta ankstesniame skyriuje.
Į orą išmestas sieros(IV) oksidas SO2 veikiamas oro deguonimi (ypač deguonies atomais O) lengvai oksiduojasi iki sieros(IV) oksido SO3, o šis oksidas, reaguodamas su kritulių vandeniu, sudaro stiprią sulfato (sieros) rūgštį H2SO4:
UV
O2(d) → 2O(d)
SO2(d) + O(d) → SO3(s)
SO3(s) + H2O(s) → H2SO4(aq)Tiek natūraliai (pvz. žaibuojant), tiek dėl oro taršos susidarę azoto oksidai NOx taip pat reaguoja su oro deguonimi bei kritulių vandeniu ir sudaro stiprią nitrato (azoto) rūgštį HNO3. Reakcijų metu taip pat gali susidaryti nestabilios nitrito rūgšties HNO2, kuri labai greita suskyla į kitus azoto junginius:
2NO(d) + O2(d) → 2NO2(d)
NO(d) + NO2(d) ↔ N2O3(d)
2NO2(d) + H2O(s) → HNO3(aq) + HNO2(aq)
N2O3(d) + H2O(s) → 2HNO2(aq)
3HNO2(aq) → HNO3(aq) + 2NO(d) + H2O(s)
Jeigu gryno vandens pH yra apie 7, tai lietaus pH yra apie 5,6. Tokį lietaus pH sumažėjimą lemia natūraliai atmosferoje esančio CO2 nedidelis kiekis. Jam ištirpus vandenyje susidaro silpnoji karbonato (anglies) rūgštis:
CO2(d) + H2O (s) ↔ H2CO3(aq)
H2CO3(aq) ↔ H+(aq) + HCO3-(aq)
Dėl oro taršos rūgštiniais oksidais kritulių pH gali sumažėti net 2–3 pH vienetais ir svyruoti nuo 2 iki 4.
Rūgštieji krituliai – viena didžiausių aplinkos taršos problemų. Iškritę rūgštieji krituliai yra žalingi ekosistemoms dėl paviršinių vandens telkinių ir dirvožemio parūgštėjimo bei tiesioginio poveikio augalams. Rūgštiesiems krituliams ypač jautrūs spygliuočiai. Nuo ilgalaikio poveikio jų spygliai ima ruduoti ir kristi, medžiai ima džiūti. Žiemos mėnesiais, kai dėl intensyviai deginamo iškastinio kuro ore būna didžiausia SO2 koncentracija, sniego paviršiuje gali susikaupti rūgštiniai sieros junginiai. Pavasarį tirpstant tokiam sniegui staiga padidėja vandens telkinių rūgštingumas ir dėl to labai nukenčia žuvų mailius.

https://www.wonderwhizkids.com/acid-rain
Rūgštieji krituliai taip pat skatina metalų koroziją, ardo įvairias statybines medžiagas (marmurą, smiltainį, klintis, dolomitą). Rūgštieji krituliai sukelia dirvožemio parūgštėjimą, pagreitina kai kurių karbonatinių uolienų (pvz. kreidos, kalkmenio, dolomito) dūlėjimą:
|
CaCO3(k) |
+2HNO3(aq) |
→ |
Ca(NO3)2(aq) |
+ CO2(d) |
+ H2O(s) |
|
|
CaCO3∙MgCO3(k) |
+ 2H2SO4(d) |
→ |
CaSO4(aq) |
+ MgSO4(aq) |
+ 2CO2(d) |
+ 2H2O(s) |

https://en.wikipedia.org/wiki/Acid_rain https://en.wikipedia.org/wiki/Rust
7.2.3. Atmosferos ozono sluoksnis
Ozonas – tai alotropinė deguonies atmaina. Ozono molekules sudaro trys O atomai. Ozono cheminė formulė yra O3.
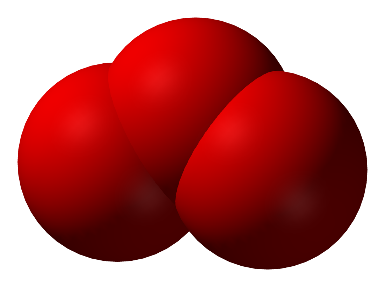
O3 molekulės rutulinis modelis
Grynas O3 yra melsvos, aštraus dirginančio kvapo dujos (tvir.=-112 oC; tlyd.= -192,2 oC). Skystas O3 yra tamsiai mėlynas, o kietas – tamsiai violetinis. Ozonas susidaro iš dviatomių deguonies molekulių O2 , jas veikiant ultravioletine spinduliuote (UV), elektros išlydžiu.
UV
3O2(d) → 2O3(d)
Ozono sluoksnį atmosferoje sudaro O3, esantis stratosferoje 10-50 km aukštyje ir apsaugantis Žemę nuo žalingų ultravioletinių (UV) spindulių, sklindančių iš Saulės, poveikio. Stratosferoje yra susikaupę ~90% viso atmosferoje esančio O3. Ozono sluoksnio storis matuojamas santykiniais Dobsono vienetais (žymima DV).
1 DV atitinka 0,01 mm ozono sluoksnio storį esant 0 oC temperatūrai ir 101,325 kPa slėgiui. Vidutinis ozono sluoksnio storis Žemės atmosferoje yra apie 300 DV. Tai reiškia, jeigu sugebėtume visą O3 „suspausti“ į vieną sluoksnį, jo storis esant 0 oC temperatūrai ir 760 mmHg slėgiui būtų apie 3 mm.
Kadangi O3 yra labai reaktyvus, su juo reaguoti ir taip ardyti ozono sluoksnį gali daugelis į stratosferą patenkančių medžiagų. Ypač pavojingi junginiai ir radikalai (dalelės, kurių atomai turi nesuporuotų elektronų), katalizuojantys O3 skilimo reakciją. Tai azoto oksidai NO ir N2O, hidroksilas (hidroksilo radikalas) HO·, chloro atomas (radikalas) Cl·. Ypač reakcingi ardant O3 yra chloro atomai, kurie susidaro iš į atmosferą „išmestų“ halogenintų, t.y. fluoro, chloro ir bromo atomų turinčių angliavandenilių, populiariai vadinamų freonų. Tai paprasčiausių angliavandenilių – metano (CH4) ir etano (C2H6) – molekulių dariniai, gauti visus arba dalį H atomų šiose molekulėse pakeitus F, Cl ir Br atomais. Šie junginiai yra labai inertiški. Ilgą laiką šaldytuvų, oro kondicionierių, aerozolių balionėlių gamyboje buvo naudojami du ypatingu cheminiu inertiškumu pasižymintys „kietieji“ freonai: trichlorfluormetanas CFCl3 (žymimas CFC-11) ir dichlordifluormetanas CF2Cl2 (žymimas CFC-12).
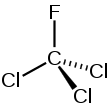
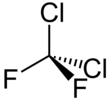

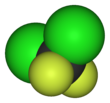
CFCl3 ir CF2Cl2 molekulių struktūrinės formulės (aukščiau) ir rutuliniai modeliai (žemiau)
Patekę į atmosferą, jie pasiekia stratosferą, kur veikiami ultravioletinių spindulių suskyla į laisvuosius radikalus. Ypač aktyvūs chloro radikalai Cl· reaguoja su O3 molekulėmis ir taip ardo ozono sluoksnį:
UV
CFCl3(d) → ·CFCl2(d) + Cl·(d)
Cl·(d) + O3(d) → O2(d) + ClO·(d)
ClO·(d) + O3(d) → 2O2(d) + Cl·(d)
7.2.4. Šiltnamio efektas
Šiltnamio efektas – tai reiškinys, dėl kurio Žemės paviršiaus temperatūra yra daug aukštesnė, nei turėtų būti pagal iš Saulės gaunamos energijos ir be trukdžių į kosmosą išspinduliuojamos energijos balansą. Šį efektą lemia atmosferoje esantys H2O garai ir dujos (anglies dioksidas CO2, metanas CH4, ozonas O3, azoto oksidai NOx, freonai ir kt.), kurios praleidžia Saulės trumpesnių elektromagnetinių bangų regimąją spinduliuotę, tačiau sulaiko nuo mūsų planetos paviršiaus atsispindėjusią ilgesnių elektromagnetinių bangų šiluminę (infraraudonąją) spinduliuotę. Tokiomis savybėmis pasižyminčios atmosferoje esančios (į ją patenkančios) dujos yra vadinamos šiltnamio dujomis.
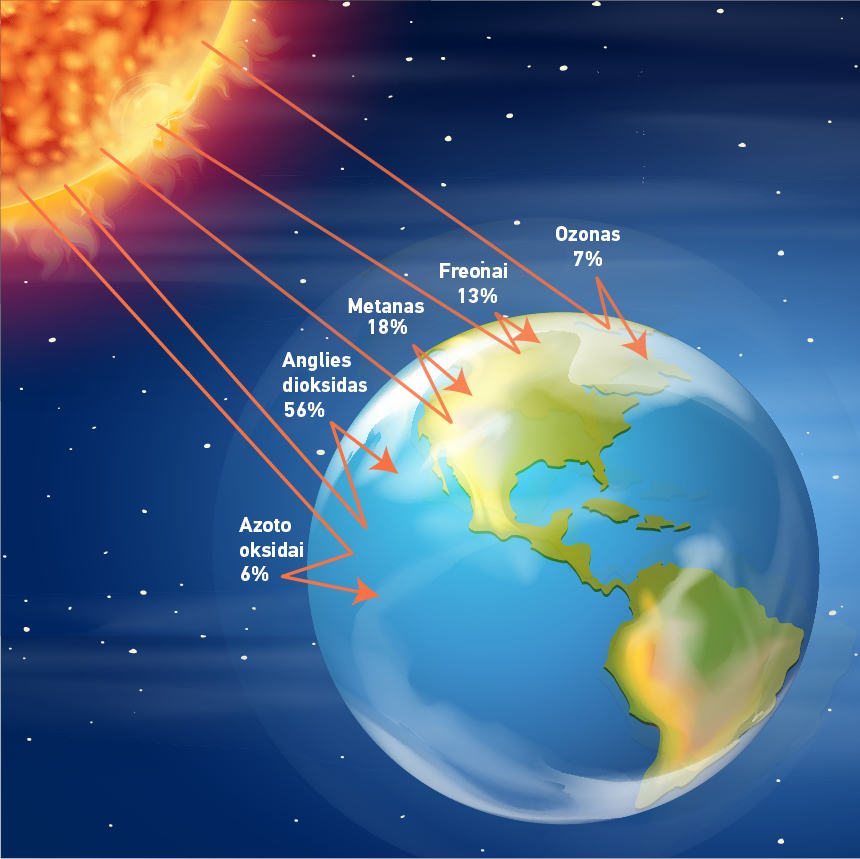
Skaičiai paveiksle parodo, kokią šiluminės spinduliuotės dalį atspindi atitinkamos atmosferos dujos.
https://www.youtube.com/watch?v=VYMjSule0Bw
https://www.youtube.com/watch?v=NvPqSGUIXtg
Apskaičiuota, jog Žemės paviršiaus vidutinė temperatūra yra apie 15 °C. Jei nebūtų šiltnamio efekto, ši temperatūra būtų apie -18°C. Šis 33-jų laipsnių skirtumas yra parametras, leidžiantis įvertinti šiltnamio efektą. Didžiausią įtaką žemės šiltnamio efektui turi:
H2O garai – nuo 36 iki 80 %
CO2 – nuo 9 iki 26 %
CH4 – nuo 4 iki 9 %
O3 – nuo 4 iki 9 %
Kiekvienoms dujoms negalima priskirti konkrečios įtakos šiltnamio efektui procentinės dalies, nes šių dujų šiluminės spinduliuotės spektrų kai kurios absorbcijos ir emisijos juostos sutampa (persikloja). Debesys (H2O garai) taip pat sugeria, atspindi bei išspinduliuoja dalį šiluminės spinduliuotės ir taip veikia visos atmosferos spinduliuotės balansą.
Per pastaruosius 200-250 m., dėl žmonijos intensyvios pramoninės veiklos pradėjus deginti vis daugiau iškastinio anglies turinčio kuro (akmens anglių, gamtinių dujų, perdirbtos naftos produktų), CO2 ir CH4 koncentracijos atmosferoje padidėjo atitinkamai 1,35 ir 2,5 karto. Šių dujų koncentracijos padidėjimas sparčiausiai vyko XX amžiaus antroje pusėje. Prognozuojama, kad per XXI amžių dėl oro taršos ir su tuo susijusių atmosferos sudėties pokyčių Žemės paviršiaus temperatūra gali pakilti nuo 2 iki 4 °C. Tai gali smarkiai paveikti pasaulinį klimatą ir turėti sunkių padarinių žmonijai. Norint sušvelninti šiuos padarinius, reikia kardinaliai sumažinti šiltnamio efektą sukeliančių dujų išmetimą į atmosferą sumažinat iškastinio kuro naudojimą šiluminei ir elektros energijai gauti bei transporte. Tai galima pasiekti vis daugiau energijos gaunat iš atsinaujinančių šaltinių (saulės, vėjo, energetinių augalų)
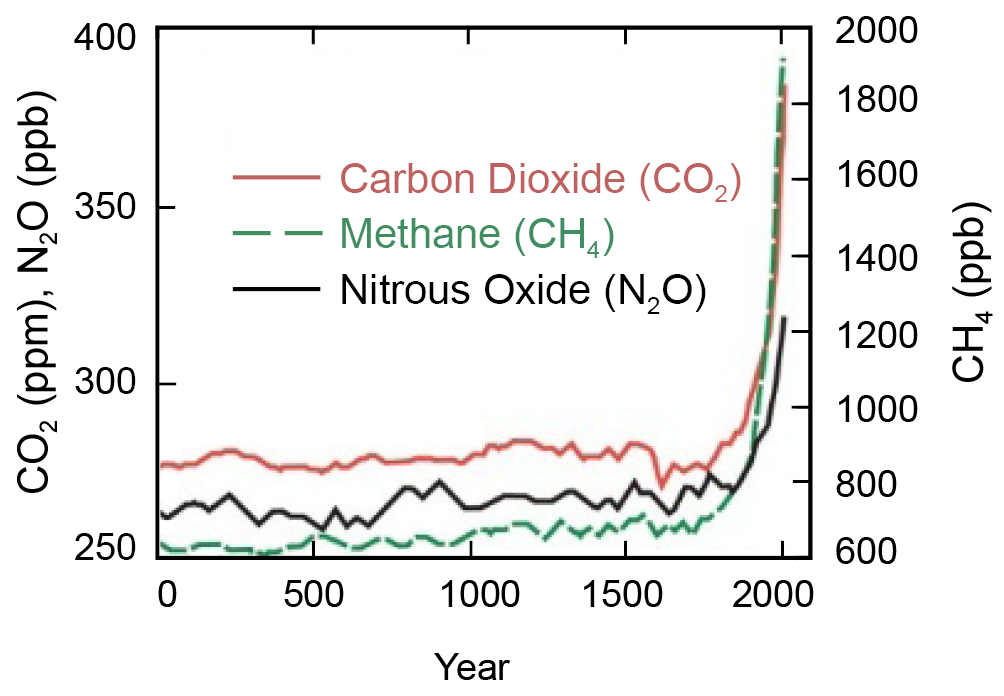
https://rtpi.org/the-weather-channel-and-climate-change-ignorance
Grafike pateikti dujų koncentracijos atmosferoje matavimo vienetai yra: ppm – milijoninė dalis, ppb – milijardinė dalis
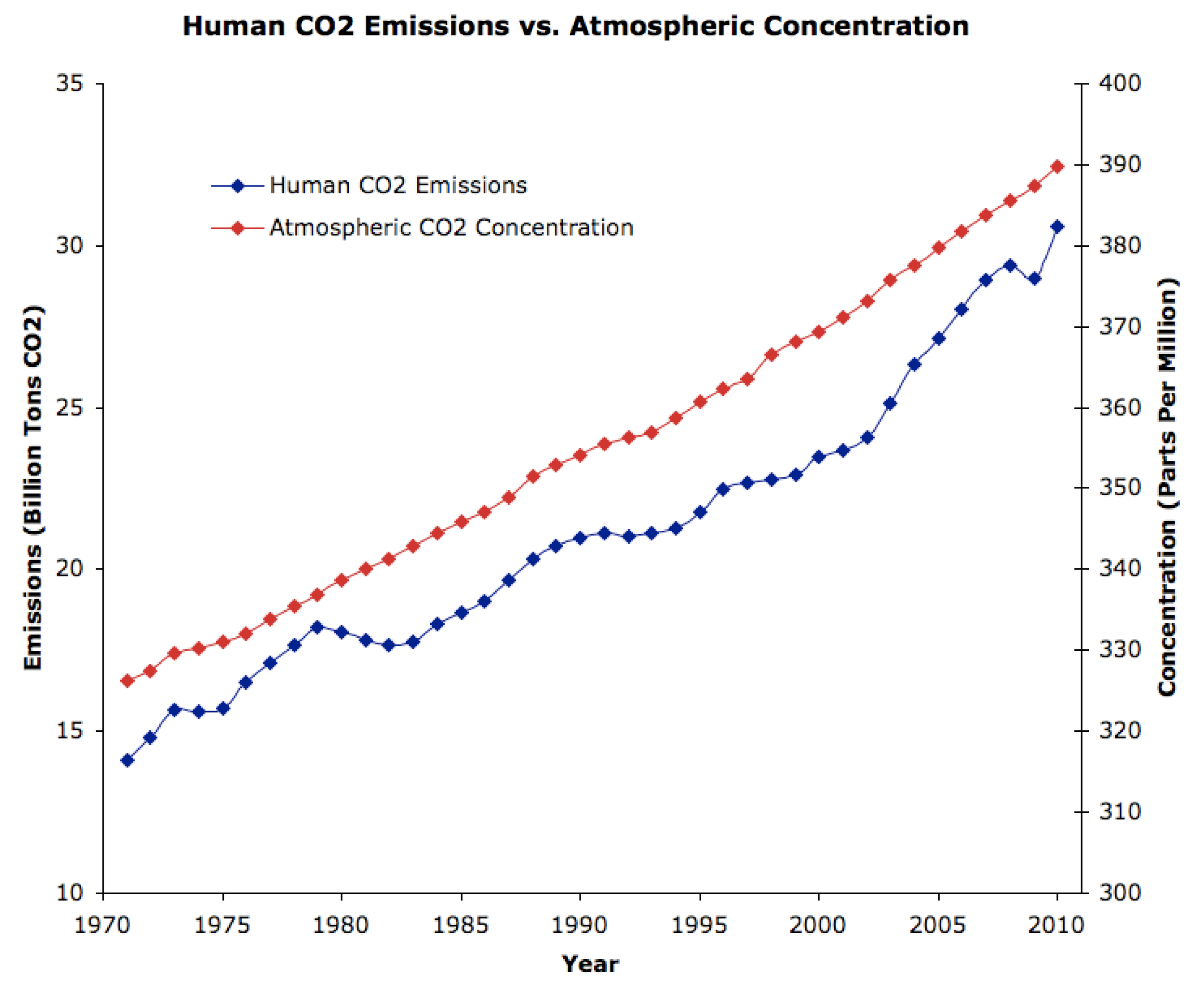
https://www.groasis.com/pt/downloads/faca-o-download-gratuito-do-livro-the-treesolution
7.3. Vanduo
Vanduo – vienas labiausiai mūsų planetoje Žemėje paplitusių junginių. Vandenynai ir jūros bei kiti paviršiniai vandens telkiniai (ežrai, upės, tvenkiniai, ledynai) dengia daugiau kaip 2/3 žemės paviršiaus. Taip pat didelė dalis vandens yra susikaupusi po žeme. Šis vanduo yra vadinamas požeminiu. Bendrai visas Žemėje esantis vanduo sudaro hidrosferą. Atmosferoje vandens yra tik labai nedidelė dalis (apie 0,001 %).
Vanduo sudaro nuo 50 iki 95 % daugelio augalų ir gyvūnų masės. Žmogaus organizme jo yra beveik 70 %, o vient tik kraujyje bei linfoje - per 90 %. Akivaizdu, jog be vandens Žemėje gyvybė negalėtų egzistuoti. Tačiau augmenijai ir gyvūnijai tinkamo, o taip pat žmonijos ūkinei bei buitinei veiklai tinkamo gėlo vandens, kuriame ištirpusių druskų koncentracija neviršija 0,1 %, mūsų planetoje yra tik apie 3,5 %. Kadangi gėlo vandens ištekliai Žemėje pasiskirstę netolygiai (apie 2/3 gėlo vandens yra susikapupę ašigalių ledynuose ir yra sunkiai panaudojami), daugelis šalių susiduria su apsirūpinimo gėlu vandeniu problema.
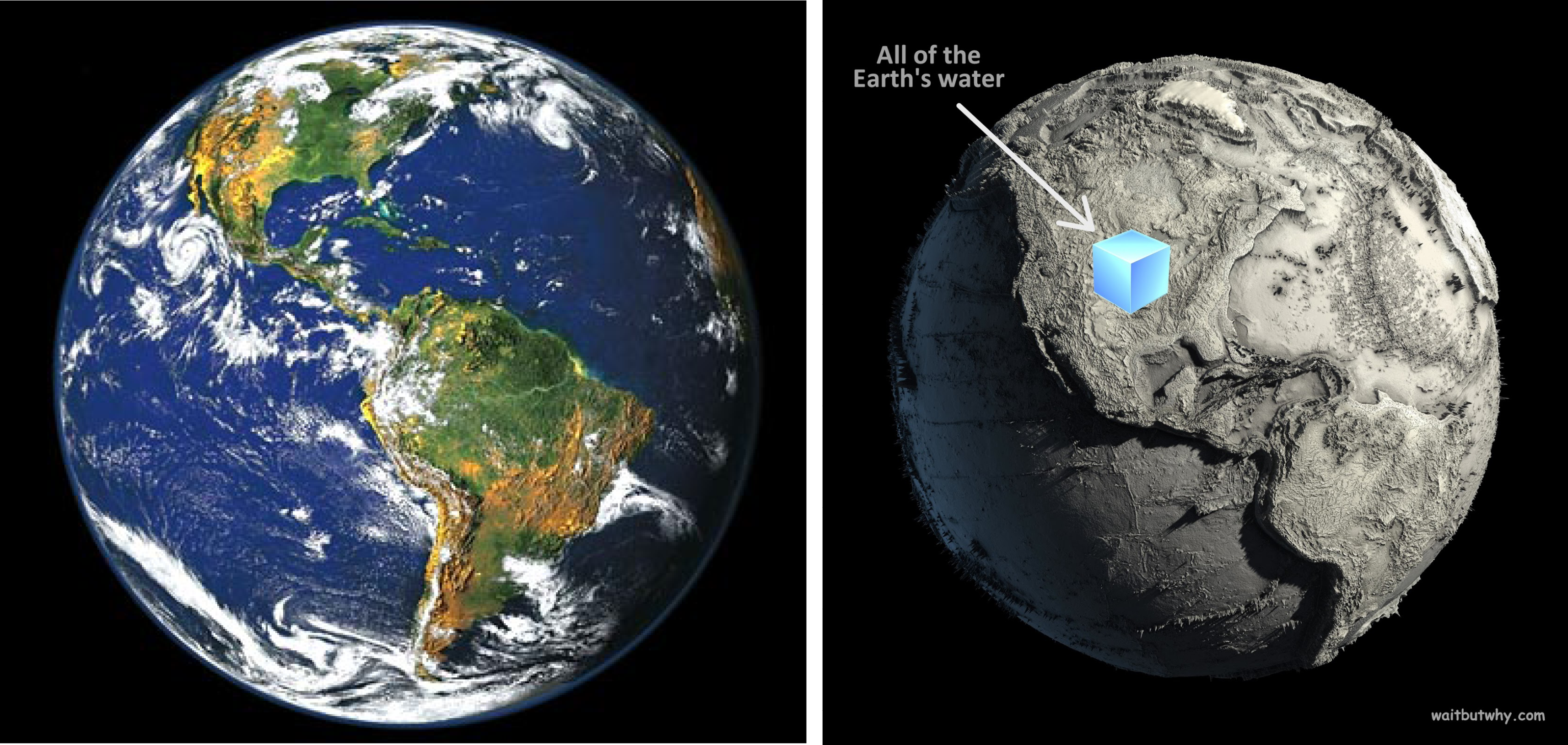
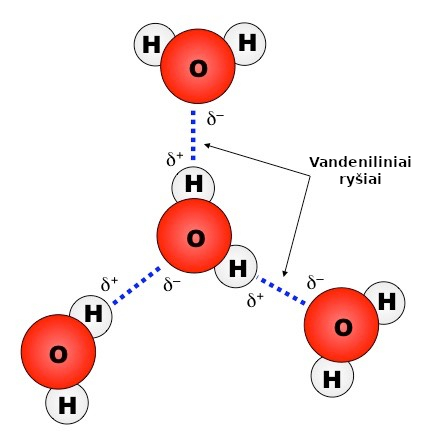
Vanduo, kaip cheminis junginys H2O, yra labai unikalių savybių medžiaga. Dėl kovalentinio ryšio elektronų pasislinkimo nuo H atomų link O atomo, pastarasis H2O molekulėje įgyja dalinį neigiamą, o H atomai – dalinį teigiamą krūvį. Dėl tokio krūvio pasiskirstymo H2O molekulės yra polinės ir tarpusavyje sudaro vandenilinį ryšį. Šis ryšys nulemia daugelį kitų vandens savybių, pvz. gan aukštas stingimo (užšalimo) ir virimo temperatūras, didelį paviršiaus įtempį. Dėl vandenilionio ryšio skystos būsenos H2O tankis, esant 4 oC temperatūrai, yra didžiausias, o kietos būsenos H2O (ledo) tankis, esant 0 oC ir žemesnei temperatūrai, yra mažesnis.
 |
t(stingimo) = 0 oC, esant 101,325 kPa slėgiui t(virimo) = 100 oC, esant 101,325 kPa slėgiui d(kieto H2O) = 916,7 kg/m3, esant 0 oC temperatūrai ir 101,325 kPa slėgiui d(skysto H2O) = 999,85 kg/m3, esant 0,1 oC temperatūrai ir 101,325 kPa slėgiui d(skysto H2O) = 999,97 kg/m3, esant 4 oC temperatūrai ir 101,325 kPa slėgiui d(skysto H2O) = 997,057 kg/m3, esant 25 oC temperatūrai ir 101,325 kPa slėgiui |
|---|
7.3.1 Vandens tarša
Dėl didelio H2O molekulių poliškumo vanduo yra geras tirpiklis, jis reaguoja su daugeliu medžiagų, susidarant kitoms, vandenyje tirpioms medžiagoms. Ypač gerai vandenyje tirpsta daugelis druskų ir rūgščių (neorganinių ir organinių), kai kurios bazės (tirpieji hidroksidai, amoniakas NH3), įvairios organinė medžiagos (angliavandeniai, alkoholiai, aminai ir kt.). Dėl to vanduo linkęs labai lengvai „užsiteršti“. Augant temperatūrai daugelio skystųjų ir kietųjų medžiagų tirpumas H2O didėja, o dujų – mažėja, ir tai sukelia rimtas aplinkosaugos problemas. Kadangi vandens augmenija ir gyvūnija kvėpavimui naudoja vandenyje ištirpusį deguonį, todėl šiltuoju metų laiku sumažėjus vandenyje ištirpusio O2 koncentracijai, vandens augalai ir gyvūnai patiria deguonies trūkumą. Visa tai sustiprina vandens eutrofikacija. Eutrofikacija – vandens ekosistemos kitimas, sukeltas cheminių maisto medžiagų, dažniausiai tirpių azoto ir fosforo junginių, pertekliaus. Eutrofikacija yra natūralus procesas, tačiau ją neretai paspartina žmonijos ūkinė veikla:
- nesaikingas tręšimas, kai žemės ūkyje naudojamos trąšos (ypač nitratai NO3- ir fosfatai PO43-) išplaunamos iš dirvožemio patenka į vandens telkinius;
- pramoninė oro tarša, kai į atmosferą išmetamos dujinės cheminės medžiagos (NOx, NH3), kurios kartu su krituliais sugrįžta į dirvožemį bei patenka į vandens telkinius;
- tiesioginė vandens tarša, kai į vandens telkinius išleidžiamas nepakankamai išvalytos ar visai nevalytos buitinės, pramoninės ir žemės ūkio (pvz. gyvulių fermų) nuotekos. Iš buitinių nuotekų yra gan sudėtinga pašalinti su skalbimo priemonėmis į jas patenkančius tirpiuosius fosfatų PO43-.
Todėl siekiant mažinti eutrofikaciją, būtinas buitinių ir pramoninių nuotekų valymas (biocheminis ir cheminis), trąšų ir oro taršos kontrolė. Tačiau tirpiųjų fosfatų PO43- koncentracijos sumažinimas buitinėse nuotekose yra efektyvus tik naudojant mažiau fosfatų turinčias arba visai jų neturinčias skalbimo priemones.

https://www.treehugger.com/clean-technology/finally-detergent-industry-puts-voluntary-ban-on-phosphates-in-household-dishwasher-detergents.html
https://www.ecogreen.ca/about/environment/phosphate-free/
Pastaraisiais dešimtmečiais išaugus įvairių plastikų gamybai bei jų panaudojimui buityje (įvairios plastikinės pakuotės, indai, buteliai ir kt.) bei žmonijos ūkinėje veikloje (plėvelės, putplasčiai, virvės, žvejybos tinklai ir kt.), taip pat išaugo ir vandens telkinių tarša plastikų šiukšlėmis. Ši problema ypač pastebima milijardines populiacijas gyventojų turinčiose valstybėse (Indijoje, Kinijoje), bei mažiau ekonomiškai įsivysčiusiose šalyse, kur menkai rūpinamasi atliekų surinkimu, rūšiavimu ir perdirbimu. Plastikinės šiukšlės, patekusios į upes, plukdomos į jūras ir vandenynus. Skaičiuojama, kad kasmet į vandenynus patenka iki 8 milijonų tonų plastiko atliekų. Dėl to jau eilę metų stebimas vis didėjantis plastiko „šiukšlynas“ Ramiajame vandenyne. Bangų mūša dalį šių šiukšlių „sugražina“ į pakrantes.

https://phys.org/news/2018-03-pacific-plastic-dump-larger.html https://en.wikipedia.org/wiki/File:Litter_on_Singapore%27s_East_Coast_Park.jpg
7.4. Dirvožemis ir jo tarša
Dirvožemis – tai viršutinis, purusis Žemės putos sluoksnis, susidaręs iš dirvodarinė uolienos, kuriame auga sausumos augmenija. Tinkami dirvožemio plotai yra naudojami žemės ūkinei veiklai, siekiant gauti specialiai jame auginamų augalų derlių. Jame taip pat auga ir natūraliai užsisėjusi augmenija (pvz. miškai). Dirvožemio susidarymas yra ilgai trunkantis bei sudėtingas procesas, kurį lemia tokie gamtiniai veiksniai:
- fiziniai (vėjas, krituliai, temperatūros svyravimai)
- cheminiai (tirpimas, hidrolizė, hidratacija, oksidacija-redukcija ir kt.)
- biologiniai (augmenija bei mikroorganizmų, bestuburių, aukštesniųjų gyvūnų veikla)
Be kietosios dirvožemio fazės (mineralinių ir organinių medžiagų), jį taip pat sudaro skystoji (H2O su jame ištirpusiomis mineralinėmis ir organinėmis medžiagomis) fazė, dujinė (dirvožemio poras užpildantis oras) fazė ir gyvoji (mikroorganizmai, bestuburiai, augmenijos šaknys) fazė. Dirvožemyje įvairių junginių pavidalu randama didžioji dalis cheminių elementų. Daugiausia yra deguonies, silicio, aliuminio, geležies, kalcio junginių (mineralų). Jame nuolatos vyksta cheminių elementų greitesnis ar lėtesnis koncentracijos kitimas (išplovimas, migracija, akumuliacija). Tai labiausiai priklauso nuo:
- cheminių junginių patekimo iš atmosferos (pvz. vykstant oro taršai), nuotekų, buitinių ir pramoninių atliekų (tiek atsitiktinėse vietose išmestų, tiek kaupiamų ir saugomų sąvartynuose);
- žemdirbystėje naudojamų cheminių medžiagų, tokių kaip trąšos, dirvožemio rūgštingumą mažinančios medžiagos (klintys (CaCO3), dolomitas (CaCO3∙MgCO3), gesintos kalkės (Ca(OH)2), augalų apsaugai nuo kenkėjų bei neapgeidautinų augalų naikinimui naudojamų pesticidų (insekticidų, fungicidų, herbicidų);
- stambiose gyvulių ir paukščių fermose susidarančių atliekų (mėšlo ir srutų, kuriuose gausu azoto junginių, taip pat yra fosforo junginių, antibiotikų);
- gyvūnijos ir augmenijos organinių liekanų natūralios mineralizacijos;
- požeminio (gruntinio) vandens tekėjimo;
Žemdirbystėje intensyviai naudojant mineralines trąšas, taip pat dėl rūgščiųjų kritulių padidėja dirvožemio rūgštingumas, jame sparčiau vyksta maistinių medžiagų (azoto, fosforo, kalio ir kitų cheminių elementų) išsiplovimas. Dėl to mažėja dirvožemio derlingumas. Suintensyvėjus maistinių medžiagų išsiplovimui, taip pat padidėja požeminių (gruntinio) ir paviršinių vandens telkinių tarša bei eutrofikacija.
Nesakingai tręšiant dirvožemį mėšlu ir srutomis, kuriuose gausu junginių, turinčių amonio (NH4+), nitrito (NO2-), nitrato (NO3-) bei fosfato (PO43–) jonų, dalis jų patenka į požeminius ir paviršinius vandens telkinius ir juos stipriai užteršia. Be to, tokiuose dirvožemiuose augančiuose augaluose (žemės ūkio kultūrose) kaupiasi neleistini nitritų ir nitratų kiekiai. Šie junginiai yra nuodingi, ypač esant didelėms jų koncentracijoms.
|
|
|
|
|
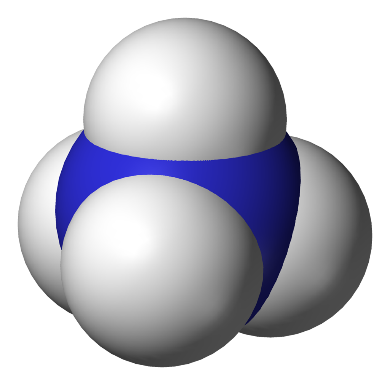
NH4+ jono rutulinis modelis |
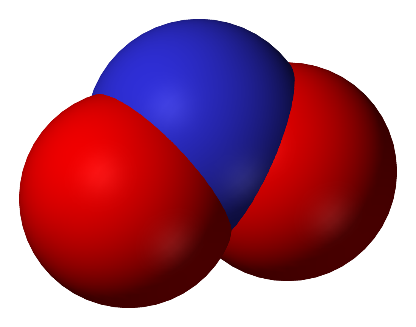
NO2– jono rutulinis modelis |
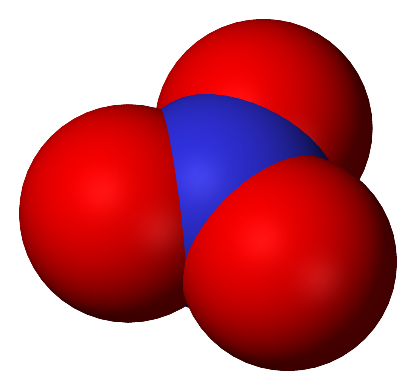
NO3– jono rutulinis modelis |
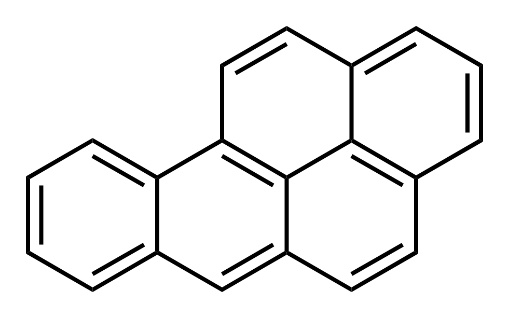
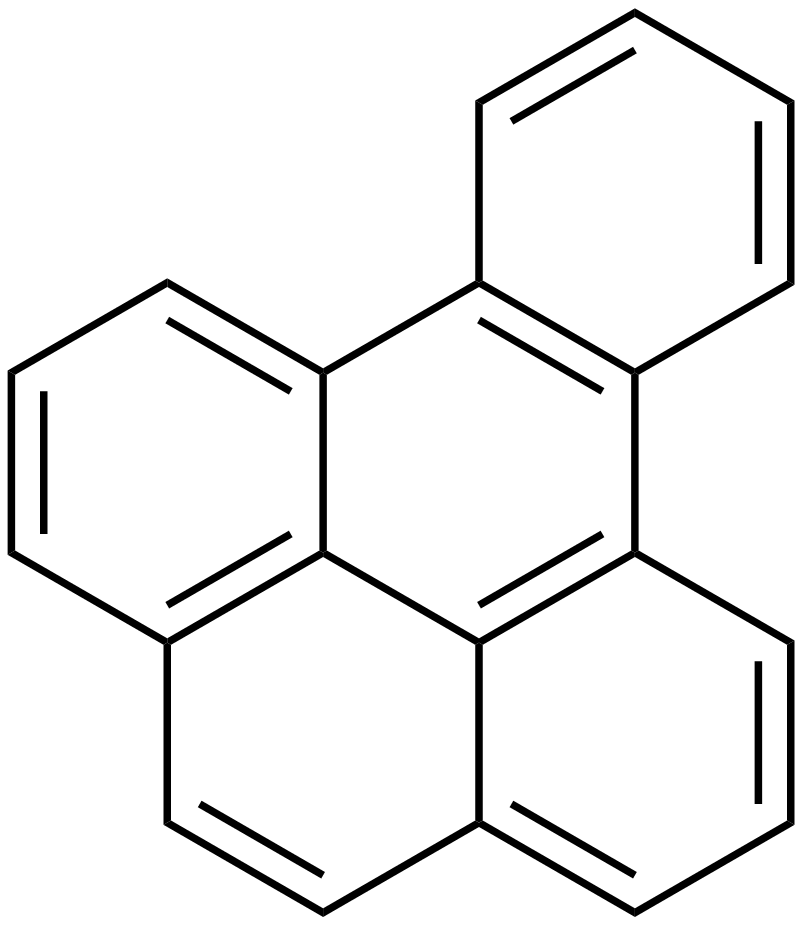
Dėl antžeminio transporto oro taršos išmetamosiomis dujomis ir kietosiomis dalelėmis (suodžiais), tiesiogiai yra teršimos teritorijos šalia automagistralių bei geležinkelių (nuo keliolikos iki keleto šimto metrų nuo jų). Pakelių dirvožemiai labiausiai būna užteršti Pb junginiais ir policikliniais (arba daugiacikliais) aromatiniais angliavandeniliais (pvz. pirenu, benzpireno izomerais).
|
|
|
|
|
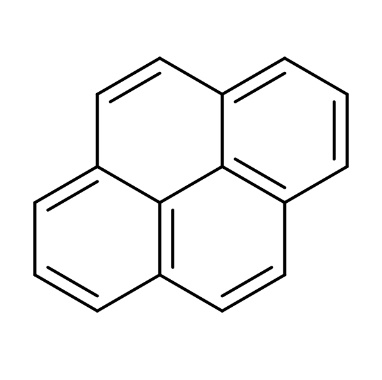
Pirenas |
Benz(a)pirenas |
Benz(e)pirenas |
Nors daug kur pasaulyje, o taip pat ir Lietuvoje, uždrausta naudoti švino junginių turintį benziną, tačiau pakelių dirvožemyje yra susikaupusios gan didelės šio toksiško metalo koncentracijos nuo tų laikų, kai švinuotas benzinas buvo naudojamas.
Dar vienas gan dažnai pasitaikantis dirvožemio taršos šaltinis yra atsitiktinėse, neleistinose vietose išmestos įvairios buitinės ir gamybinės atliekos. Ypač užteršiamas dirvožemis bioneskaidžiomis ir ilgai (nuo keleto dešimtmečių iki keleto šimtmečių ar dar ilgiau) chemiškai yrančiomis bei dūlėjančiomis šiukšlėmis:
- įvairiais metalais ir jų turinčiomis atliekomis (pvz. metalo laužas, galvaniniai elementai, elektros akumuliatoriai, gyvsidabrio turinčios liuminescencinės lempos);
- polimerų atliekomis (automobilių padangos, plastikiniai indai, pakavimo ir statybinės plėvelės, putplasčiai, dažai, lakai ir kt.);
- stiklo atliekomis (langų stiklų, stiklinės taros duženos)

http://www.greenpeace.org/russia/en/multimedia/photos/illegal-forest-dump-on-the-olk-3/
Yra žinoma, kad popierius aplinkoje, veikiamas kritulių, saulės šviesos, temperatūrų svyravimų bei mikroorganizmų, visiškai suyra per 2-3 metus, tai smulkios stiklo bei daugumos iš naftos pagamintų plastikų (polietilenas, polivinilchloridas, polistirenas) atliekos suyra per kelis šimtus metų. Be to, irdami plastikai išskiria kitus junginius, kurie gali lemti ilgalaikę to paties dirvožemio, gruntinio vandens arba oro taršą.
Siekiant išvengti dirvožemio taršos tokiomis atliekomis, efektyviausia priemonė yra kaip galima mažiau atliekų kaupti sąvartynuose, jas rūšiuoti bei pritaikant naujausias technologijas perdirbti. Kai atliekas išrūšiuoti yra per daug sudėtinga arba kai išrūšiuotos atliekos yra netinkamos perdirbti, jos yra deginamos šiuolaikinius aplinkosaugos reikalavimus atitinkančiose šiukšlių deginimo gamyklose. Jose degimo šiluma yra efektyviai panaudojama elektros gamybai bei pastatų ir vandens šildymui, o degimo metu susidarantys dūmai valomi specialiais filtrais. Tokia gamykla jau keletą metų veikia Klaipėdoje, o artimiausiu metu bus pastatytos Vilniuje ir Kaune.

https://www.fortum.lt/apie-mus/imones-lietuvoje/fortum-klaipeda