Teorinė medžiaga su pavyzdžiais
6.2. Angliavandeniliai
6.2.2.2. Alkinai
Angliavandeniliai, kurių bendroji formulė CnH2n-2 ir kurių molekulėse tarp anglies atomų yra vienas trigubasis ryšys, vadinami alkinais.
Nomenklatūra
Bendrojoje alkinų formulėje indeksas n – sveikasis skaičius, rodantis anglies atomų skaičių, nuo kurio priklauso pavadinimas. Alkinų pavadinimai sudaromi su priesaga –in – ir galūne –as, pvz. C2H2 – etinas, C3H4 – propinas ir kt. Pagrindinės nomenklatūros taisyklės pateiktos 6.1. skyriuje. Skirtingai nuo alkanų pagrindinė C atomų grandinė (nebūtinai ilgiausia) turi būti su trigubuoju ryšiu. Ji numeruojama nuo tos pusės, kur arčiau yra trigubasis ryšys. Pvz.:
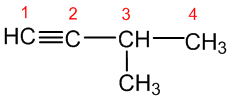
3 - metil - 1 - butinas
Izomerija
Alkinams būdingos šios izomerijos rūšys:
1. Anglies grandinės izomerija (pentino C5H8):

1 - pentinas 3 - metil - 1- butinas
2. Trigubojo ryšio padėties izomerija (pentino C5H8):
![]()
1 - pentinas 2 - pentinas
3. Tarpklasinė izomerija. Alkinų ir dienininių angliavandenilių (alkadienų) yra ta pati bendroji molekulinė formulė. Todėl, pvz. butinas ir butadienas yra tarpusavyje izomerai.
Gavimas
Pramonėje etinas gaunamas kaitinant gamtines dujas (metaną). Šiame procese vienas iš tarpinių produktų yra etinas, kuris greitai šalinamas iš aukštos temperatūros zonos.
![]()
metanas etinas
Laboratorijoje ir pramonėje etiną galima gauti kalcio karbidą veikiant vandeniu:
CaC2 + 2H2O → C2H2 + Ca(OH)2
Tai pats seniausias etino gamybos būdas.
Kiti alkinai laboratorijoje gaunami dihalogenalkanus (halogenų atomai yra prie gretimų anglies atomų) veikiant alkoholiniais šarmų tirpalais:
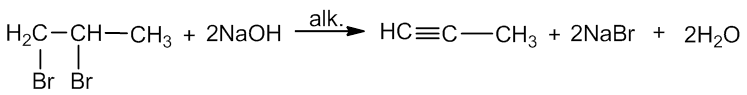
1, 2 – dibrompropanas propinas
Fizikinės savybės
Pirmieji trys alkinų homologinės eilės nariai turintys (C2 – C4) – dujos, (C5 – C16) – skysčiai, (C17 ir >) – kietos medžiagos. Žemesnieji alkinai geriau tirpsta vandenyje negu alkenai ir alkanai. Alkinai gerai tirpsta mažo poliškumo organiniuose tirpikliuose (benzene, dietileteryje, benzine, tetrachlormetane). Alkinų virimo temperatūra ir tankiai šiek tiek didesni, negu atitinkamų alkenų ir alkanų. Kuo didesnė molinė masė, tuo aukštesnė virimo temperatūra.
Etinas (acetilenas) – bespalvės, lengvesnės už orą dujos, mažai tirpios vandenyje. Grynas etinas beveik bekvapis.
Cheminės savybės
Alkinams būdingos prisijungimo, oksidacijos ir polimerizacijos reakcijos.
1. Prisijungimo reakcijos.
a) reaguoja su vandeniliu (hidrinimo reakcija). Priklausomai nuo vandenilio kiekio – gali susidaryti alkenas arba alkanas:
![]()
propinas propenas
![]()
propenas propanas
b) reaguoja su halogenais (halogeninimas):
![]()
propinas 1,2 - dibrompropenas
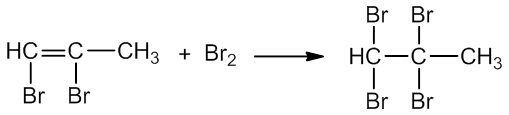
1,2 - dibrompropenas 1,1,2,2 - tetrabrompropanas
Ši reakcija yra alkinų atpažinimo reakcija – alkinai blukina bromo vandenį greičiau negu alkenai.
c) reaguoja su vandenilio halogenidais (Markovnikovo taisyklė: vandenilio atomas prisijungia prie labiau hidrinto anglies atomo, o halogeno atomas – prie kito anglies atomo. Prisijungimas vyksta prie anglies atomų, tarp kurių yra trigubasis ryšys):
![]()
propinas 2 - brompropenas
2 - brompropenas 2,2 - dibrompropanas
d) hidratacijos reakcija (Kučerovo reakcija) vyksta esant sieros rūgšties ir katalizatoriumi naudojant Hg2+ druskas:
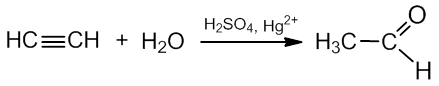
etinas etanalis
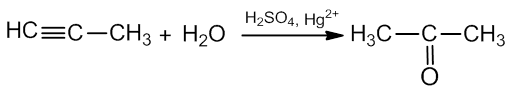
propinas propanonas
2. Oksidacijos reakcijos.
a) blukina kalio permanganato tirpalą – kokybinė alkinų atpažinimo reakcija. Anglies atomų grandinė trūksta trigubojo ryšio vietoje ir susidaro dvi karboksirūgštys:
![]()
propinas metano rūgštis etano rūgštis
b) aukštoje temperatūroje alkinai dega iki CO2 ir H2O išskirdami didelį kiekį šilumos:
C3H4 + 4O2 → 3CO2 + 2H2O
3. Polimerizacijos reakcijos.
Vykdant etino trimerizacijos reakciją ir naudojant katalizatorių – aktyvuotą C, susidaro benzenas:
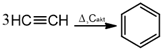
propinas benzenas
Panaudojimas
Iš alkinų plačiausiai naudojamas etinas (acetilenas) sintetinant vinilchloridą (chloreteną), vinilacetileną ir akrilnitrilą, naudojamus polimerizacijos reakcijose. Iš jo gaminamas etanalis, etano rūgštis, ir kiti junginiai. Etino mišinys su deguonimi naudojamas autogeninio metalų suvirinimo ir metalų pjovimo darbams.
