Teorinė medžiaga su pavyzdžiais
| Svetainė: | KTU atvirieji mokymai |
| Kursas: | ★ CHEMIJA išlyginamieji mokymai |
| Knyga: | Teorinė medžiaga su pavyzdžiais |
| Spausdino: | Svečio paskyra |
| Data: | šeštadienis, 2026 gegužės 30, 14:02 |
6. Įvadas į organinę chemiją
Organinė chemija – anglies junginių (išskyrus anglies dioksidą, karbonato rūgštį ir jos druskas, cianido rūgštį ir cianidus, tiocianato rūgštį ir tiocianatus, karbidus) chemija.
Organinių junginių sandaros pagrindiniai teiginiai:
1. Visi atomai, sudarantys organinių medžiagų molekules, tarpusavyje jungiasi tam tikra tvarka pagal valentingumą:
Anglis yra keturvalentė. Ji gali sudaryti 4 ryšius:
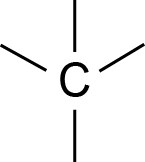
Deguonis yra dvivalentis. Jis gali sudaryti du ryšius:
![]()
Vandenilis ir halogenai yra vienvalenčiai. Jie gali sudaryti po vieną ryšį:
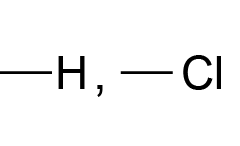 ir kt.
ir kt.
2. Anglies atomai gali jungtis tarpusavyje sudarydami viengubuosius, dvigubuosius bei trigubuosius ryšius:
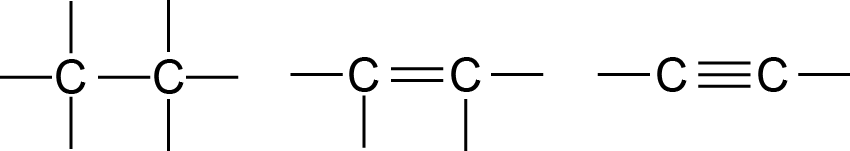
3. Medžiagų savybės priklauso nuo cheminių elementų atomų jungimosi molekulėje sekos bei tvarkos, t.y. erdvinės struktūros. Šis teiginys paaiškina izomerijos reiškinį.
Izomerai – junginiai, kurių sudėtis ir molekulinė masė vienoda, bet jie skiriasi atomų jungimosi tvarka arba jų išsidėstymu erdvėje bei fizikinėmis ir cheminėmis savybėmis. Nenurodant tikslaus pavadinimo, junginio izomero pavadinimas pradedamas priešdėliu izo-, pavyzdžiui C4H10: butanas ir izobutanas:
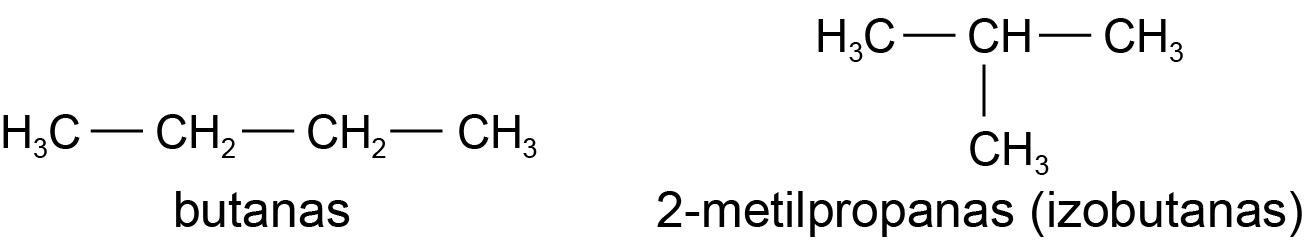
4. Medžiagos molekulėje atomai ar atomų grupės veikia vieni kitus; veikia ne tik šalia esantys, bet ir tarpusavyje nesusiję atomai.
5. Pagal medžiagos savybes galima nustatyti jos molekulės struktūrą, o pagal struktūrą numatyti savybes. Neorganinių medžiagų savybės priklauso nuo jų sudėties ir kristalinių gardelių struktūros. Norint apibūdinti ir visiems suprantamai pavaizduoti organinį junginį, reikia nurodyti šiuos požymius:
- junginio sudėtį (sudarančius atomus ir jų santykį);
- junginio sandarą (jungiančius ryšius, ryšių tipą ir atomų išsidėstymą).
6.1. Organinių junginių nomenklatūra
Junginių pavadinimai sudaromi pagal pagrindinės (ilgiausios) anglies atomų grandinės pavadinimą. 6.1 lentelėje pateikta alkanų homologinė eilė ir pakaitų pavadinimai.
6.1 lentelė. Alkanų homologinė eilė
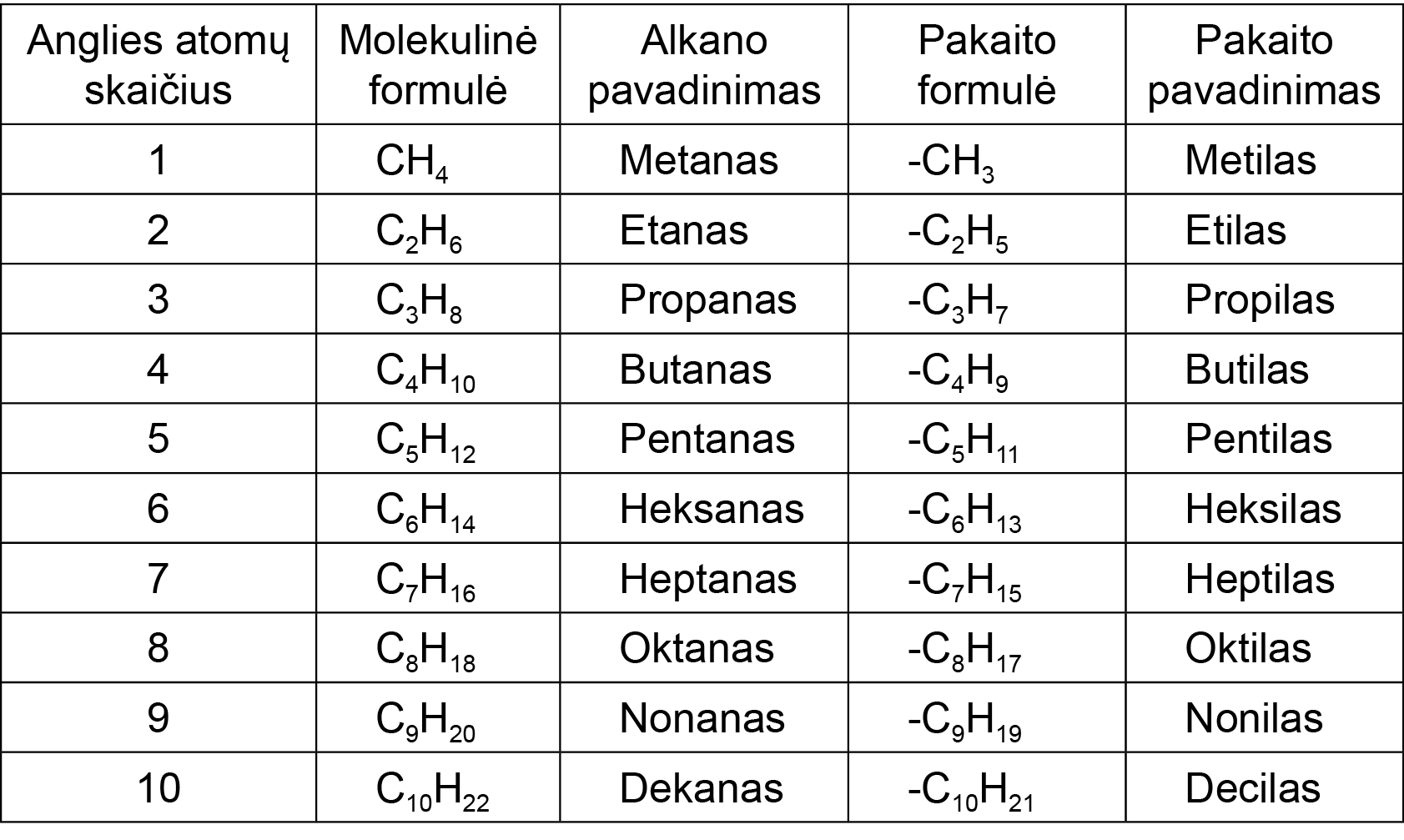
Pakaitas – atomas ar atomų grupė, kurie pakeičia molekulėje vandenilio atomą.
Pagrindinės IUPAC nomenklatūros organinių junginių pavaidinimų sudarymo taisyklės
1. Nustatoma ilgiausia anglies atomų grandinė junginyje ir anglies atomai numeruojami tokia tvarka, kad pakaitas būtų sujungtas su kuo mažesnį numerį turinčiu anglies atomu, pvz.

2. Anglies atomai, nepatekę į ilgiausią (sunumeruotą) grandinę tampa atšakomis ir vadinami pakaitais. Pakaitai vadinami pagal anglies atomų skaičių (žr. lentelę). Rašant pavadinimą nurodomas anglies atomo numeris, prie kurio prijungtas pakaitas, po to parašomas brūkšnelis, pakaito pavadinimas ir ilgiausios grandinės pavadinimas:
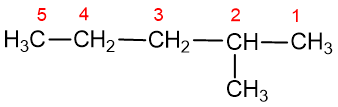
2-metilpentanas
3. Jeigu yra keletas vienodų pakaitų, tai prieš pakaito pavadinimą naudojami priešdėliai: 2- di-, 3- tri-, 4- tetra- ir t.t. Kai yra po kelis skirtingus pakaitus, priešdėlis nekeičia abėcėlinės vardinimo tvarkos (trietil– bus prieš dimetil–). Jeigu du vienodi pakaitai yra prie to paties C atomo, tai rašoma pvz. 2,2 (kaip duotame pavyzdyje):
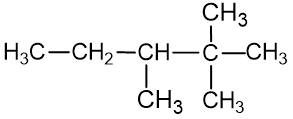
2,2,3-trimetilpentanas
Trivialioji nomenklatūra
Trivialioji nomenklatūra – tai atsitiktiniai pavadinimai, atsiradę tada, kai dar nebuvo organinių junginių sandaros teorijos. Todėl jie neturi sisteminio pagrindo, neatspindi sandaros. Organinių junginių pavadinimai buvo sudaromi remiantis radimo vieta, gavimo būdu, spalva ar kuria nors savybe, neturinčia nieko bendro su struktūra, pavyzdžiui, medžio spiritas, vyno spiritas, metanas, etanas, skruzdžių, acto, vyno, obuolių ir citrinų rūgštys, fruktozė, benzenas, fenolis ir kt. Trivialieji pavadinimai yra trumpi, lengvai įsimenami, todėl vartojami iki šiol.
6.2. Angliavandeniliai
Angliavandeniliai – paprasčiausi organiniai junginiai, sudaryti tik iš anglies ir vandenilio atomų. Angliavandeniliai skirstomi į sočiuosius ir nesočiuosius.
6.2.1. Sotieji angliavandeniliai
Sotieji angliavandeniliai skirstomi į:
- alkanus (acikliniai) – anglies atomų grandinė linijinė arba šakotoji;
- cikloalkanus (cikliniai) – anglies atomų grandinė uždara.
6.2.1.1. Alkanai
Angliavandeniliai, kurių bendroji formulė CnH2n+2 ir visi anglies atomai sujungti viengubuoju ryšiu, yra vadinami sočiaisiais angliavandeniliais arba alkanais. Bendrojoje alkanų formulėje indeksas n – sveikasis skaičius, rodantis anglies atomų skaičių, nuo kurio priklauso pavadinimas.
Nomenklatūra
Alkanų pavadinimai sudaromi su priesaga –an – ir galūne –as, pvz. CH4 – metanas, C3H8 – propanas ir kt. Visos alkanų nomenklatūros taisyklės pateiktos 6.1. skyriuje.
Homologai ir izomerai
1 lentelėje (6.1. skyrius) pateikta alkanų homologinė eilė. Panašios struktūros junginiai, besiskiriantys viena arba keliomis –CH2– grupėmis, vadinami homologais, o nuosekliai vienas po kito einantys homologai sudaro homologinę eilę. –CH2– grupė vadinama homologiniu skirtumu.
Homologai pvz. metanas (CH4) ir propanas (C3H8).
Izomerai – žr. skyrių „Įvadas į organinę chemiją“. Alkanams būdinga anglies atomų grandinės izomerija. Daugėjant anglies atomų alkane daugėja ir jo izomerų.
Paplitimas gamtoje
Metanas susidaro gamtoje yrant be oro augalų ir gyvūnų liekanoms. Todėl pastaruoju metu atliekų tvarkymo aikštelėse šiuolaikinėmis atliekų perdirbimo technologijomis surinktas metanas naudojamas kaip kuras. Pelkėtose vietose kylantys burbuliukai yra taip pat daugiausiai metano dujos. Nors metanas silpnai tirpsta vandenyje, vandenynų dugne susidaro metano hidratai CH4 . nH2O.
Metano išsiskiria akmens anglių kloduose ir susikaupia šachtose. Todėl metanas – dažna avarijų (sprogimų) priežastis. Alkanai yra viena iš pagrindinių naftos sudedamųjų dalių ir yra viena iš svarbiausių “šiltnamio efekto” priežasčių.
Kietos būsenos alkanai įeina į bičių vaško ir kai kurių augalų lapų, žiedų bei sėklų vaško sudėtį.
Gavimas
Pramonėje alkanai gaunami iš gamtinių dujų ir naftos.
Laboratorijoje alkanai gali būti gaunami įvairiais būdais:
1. Tiesioginė sintezė iš elementų aukštoje temperatūroje (450 – 470 oC), dideliame slėgyje (300 at) ir dalyvaujant katalizatoriams (Mo, W arba Ni oksidai):
C + 2H2 → CH4
2. Natrio acetatą kaitinant (250 – 300 0C) su kietu natrio šarmu:
CH3COONa + NaOH → CH4 + Na2CO3
3. Hidrinant alkenus (žr. 6.2.2.1. skyrių).
4. Metanas gaunamas aliuminio karbidui reaguojant su vandeniu (hidrolizės reakcija):
Al4C3 + 12H2O → 3CH4 + 4Al(OH)3
4. Viurco sintezė. Halogenalkanai reaguoja su metaliniu natriu arba kaliu ir sudaro alkanus, kurių molekulėse anglies atomų yra tiek, kiek jų buvo dviejose halogenalkano molekulėse:
2CH3Cl + 2Na → C2H6 + 2NaCl
2C2H5Cl + 2Na → C4H10 + 2NaCl
Fizikinės savybės
Didėjant alkanų molekulinei masei, kinta ir jų fizikinės savybės - kyla virimo temperatūra, didėja tankis ir klampa. Pirmieji keturi alkanų homologinės eilės nariai turintys (C1 – C4) – dujos, (C5 – C15) – skysčiai, (C16 ir >) – kietos medžiagos. Visi alkanai lengvesni už vandenį, jame netirpsta tačiau gerai tirpsta organiniuose tirpikliuose (benzene, dietileteryje).
Labai svarbios organinių medžiagų charakteristikos yra virimo ir lydymosi temperatūros. Didėjant alkanų santykinei molekulinei masei, didėja jų tankis, virimo bei lydymosi temperatūros.
Alkanai yra bespalviai. Dujiniai ir kietieji alkanai neturi kvapo, skystieji – kvepia benzinu.
Cheminės savybės
Alkanai neprisijungia vandenilio ir kitų cheminių elementų. Jiems būdingos pakaitų reakcijos.
1. Pakaitų reakcijos (žr. 4.1. skyrių) su halogenais (halogeninimo reakcijos). Pramonėje halogeninimo reakcijos vykdomos 300–400 oC temperatūroje. Jos gali vykti ir kambario temperatūroje, tačiau reikia saulės šviesos arba apšvitinti ultravioletiniais spinduliais:
CH4 + Cl2 → CH3Cl + HCl
chlormetanas
Esant halogenų pertekliui, palaipsniui gali būti pakeisti visi vandenilio atomai:
CH3Cl + Cl2 → CH2Cl2 + HCl
dichlormetanas
CH2Cl2 + Cl2 → CHCl3 + HCl
trichlormetanas
CHCl3 + Cl2 → CCl4 + HCl
tetrachlormetanas
Pakaitų reakcijos su bromu vyksta lėčiau, su jodu visai nevyksta, o su fluoru vyksta labai audringai su sprogimu, todėl jis naudojamas labai išimtinais atvejais.
2. Oksidacijos reakcijos. Aukštoje temperatūroje alkanai ore dega iki CO2 ir H2O išskirdami didelį kiekį šilumos. Ši oksidacijos reakcija turi didžiulę praktinę reikšmę, nes ja paremtas dujinių ir skystųjų alkanų naudojimas kurui.
C3H8 + 5O2 → 3CO2 + 4H2O
Metano ir oro mišiniai yra sprogūs.
3. Pirolizės reakcija – organinių medžiagų skaidymas aukštoje temperatūroje (1100-1200 oC) be oro, susidarant suodžiams ir vandeniliui:
CH4 → C + 2H2
4. Dehidrinimo reakcija – vandenilio atskėlimo reakcija. Ši reakcija naudojama nesočiųjų angliavandenilių gavimui iš alkanų.
![]()
5. Krekingas – didelės molinės masės alkanų skaidymas į mažesnės molinės masės alkanus ir alkenus aukštoje temperatūroje (> 450 oC):
C10H22 → C5H12 + C5H10
Panaudojimas
Alkanai plačiai naudojami kaip vidaus degimo variklių kuras. Sintetinant alkanus iš jų gaunami chlorintieji junginiai, pavyzdžiui, chlormetanas. Jis naudojamas kaip šaldymo agentas šaldytuvuose. Pramonėje metanas yra pagrindinė žaliava vandeniliui gauti.
6.2.1.2. Cikloalkanai
Ciklinės struktūros sotieji angliavandeniliai, kurių bendroji formulė CnH2n, vadinami cikloalkanais.
Nomenklatūra
Cikloalkanų pavadinime šalia atitinkamo alkano pavadinimo rašoma ciklo-. Pirmieji keturi cikloalkanai:
Ciklopropanas 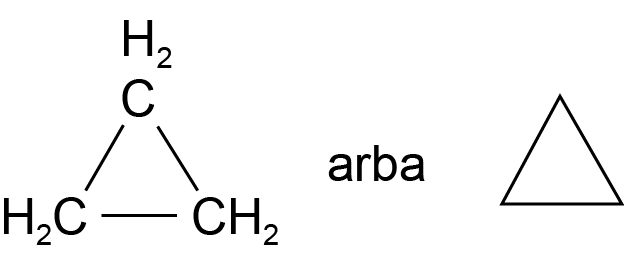
Ciklobutanas 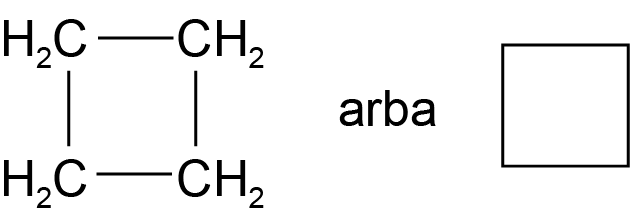
Ciklopentanas 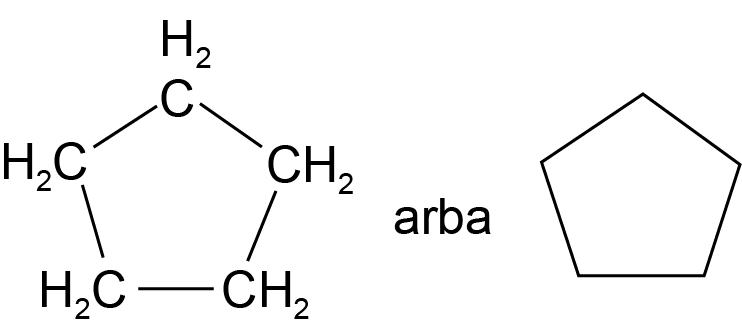
Cikloheksanas 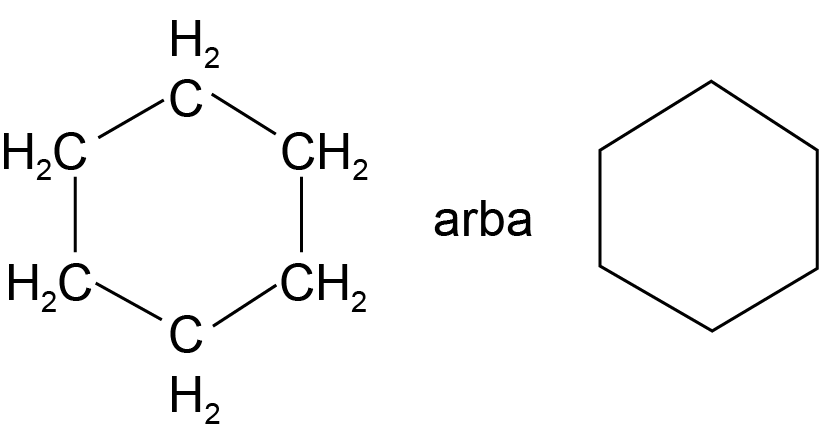
Jeigu yra pakaitų, tai cikle esantys anglies atomai numeruojami taip, kad pakaitai turėtų mažiausius skaičius, pvz.:
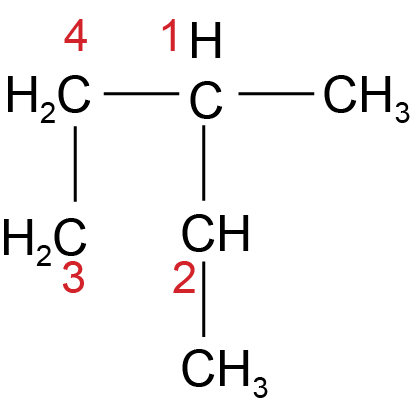 1,2 – dimetilciklobutanas
1,2 – dimetilciklobutanas
Jeigu šoninės grandinės anglies atomų skaičius yra didesnis už cikle esančių anglies atomų skaičių, tai pagrindine grandine tampa šoninė ciklo grandinė, pvz.: 1 – ciklopropilbutanas, bet ne butilciklopropanas.
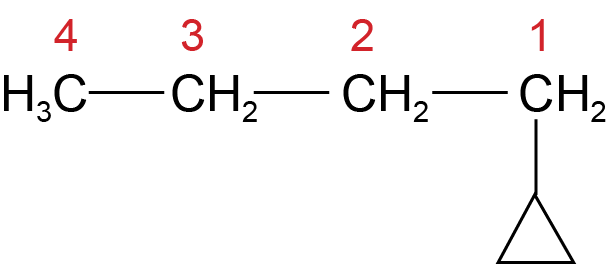
Paplitimas gamtoje
Dažniausiai cikloalkanai randami įvairių rūšių naftoje, todėl dar vadinami naftenais. Plačiausiai paplitę penkianariai ir šešianariai cikloalkanai.
Gavimas
Pramonėje cikloalkanai gaunami dehidrinant alkanus:
![]()
propanas ciklopropanas
Laboratorijoje cikloalkanai ciklizuojant dihalogenalkanus, esant Na arba Zn:
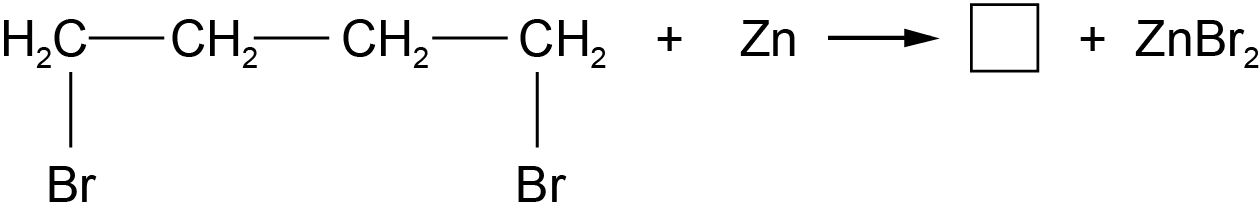
1,4 - dibrombutanas ciklobutanas
Fizikinės savybės
Ciklopropanas ir ciklobutanas yra dujos, o ciklopentanas ir cikloheksanas – skysčiai. Cikloalkanai lengvesni už vandenį ir jame netirpsta, bet tirpsta organiniuose tirpikliuose (benzene, dietileteryje). Jų virimo ir lydymosi temperatūros aukštesnės už atitinkamų alkanų ir alkenų, turinčių tiek pat anglies atomų.
Cheminės savybės
1. Prisijungimo reakcijos. Lengviau prisijungimo reakcijose dalyvauja mažų ciklų cikloalkanai (gali prisijungti vandenilį, halogenus):
![]()
ciklobutanas butanas
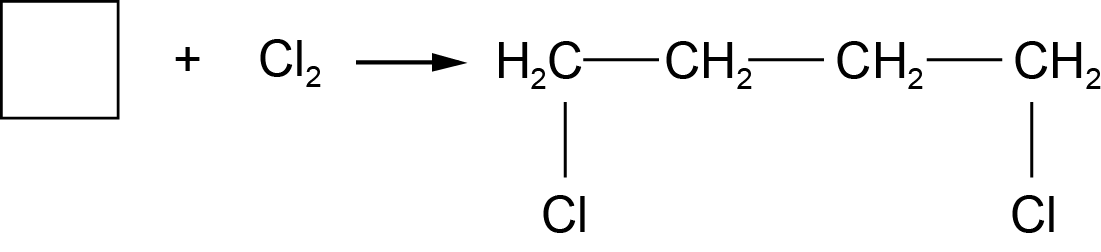
ciklobutanas 1,4 - dichlorbutanas
Kuo mažesnis ciklas, tuo cikloalkanas aktyviau dalyvauja prisijungimo reakcijose, o kuo ciklas didesnis, tuo būdingesnės pakaitų reakcijos.
2. Pakaitų reakcijos.
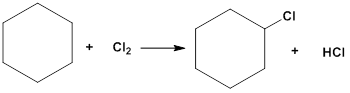
cikloheksanas chlorcikloheksanas
Panaudojimas
Cikliniai junginiai naudojami parfumerijos pramonėje. Ciklopropanas naudojamas medicinoje narkozei. Ciklopentano ir jo darinių, cikloheksano yra variklių kuro ir alyvų sudėtyje. Cikloheksanas naudojamas poliamidinio pluošto (nailono 6,6) sintezėje.
6.2.2. Nesotieji angliavandeniliai
Nesotieji angliavandeniliai skirstomi į:
- alkenus (acikliniai) – anglies atomų grandinė linijinė arba šakotoji; tarp dviejų anglies atomų yra dvigubasis ryšys
- alkinus (acikliniai) – anglies atomų grandinė linijinė arba šakotoji; tarp dviejų anglies atomų yra trigubasis ryšys
- dienus (acikliniai) – anglies atomų grandinė linijinė arba šakotoji; tarp anglies atomų yra keli dvigubieji ryšiai.
- arenus (cikliniai) – anglies atomų grandinė uždara.
6.2.2.1. Alkenai
Angliavandeniliai, kurių bendroji formulė CnH2n ir kurių molekulėse tarp anglies atomų yra vienas dvigubasis ryšys, vadinami alkenais.
Nomenklatūra
Bendrojoje alkenų formulėje indeksas n – sveikasis skaičius, rodantis anglies atomų skaičių, nuo kurio priklauso pavadinimas. Alkenų pavadinimai sudaromi su priesaga –en – ir galūne –as, pvz. C2H4 – etenas, C3H6 – propenas ir kt. Pagrindinės nomenklatūros taisyklės pateiktos 6.1. skyriuje. Skirtingai nuo alkanų pagrindinė C atomų grandinė (nebūtinai ilgiausia) turi būti su dvigubuoju ryšiu. Ji numeruojama nuo tos pusės, kur arčiau yra dvigubasis ryšys. Pvz.:
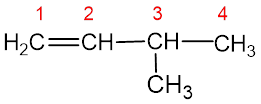
3 - metil - 1 - butenas
Izomerija
Alkenams būdingos šios izomerijos rūšys:
1. Anglies grandinės izomerija (penteno C5H10):

2. Dvigubojo ryšio padėties izomerija (penteno C5H10):
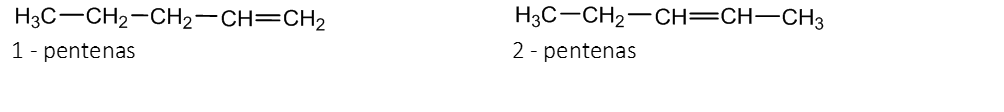
3. Geometrinė izomerija (cis- ir trans-). Kai anglies atomai sudaro viengubąjį ryšį, jie sukasi aplink ryšio ašį, bet ryšys nenutrūksta. Kai grandinėje yra dvigubasis ryšys, sukimasis neįmanomas. Jei medžiagos molekulėje pakaitai išsidėstę vienoje dvigubojo ryšio pusėje, tai – cis-izomeras, jei skirtingose pusėse – trans-izomeras.
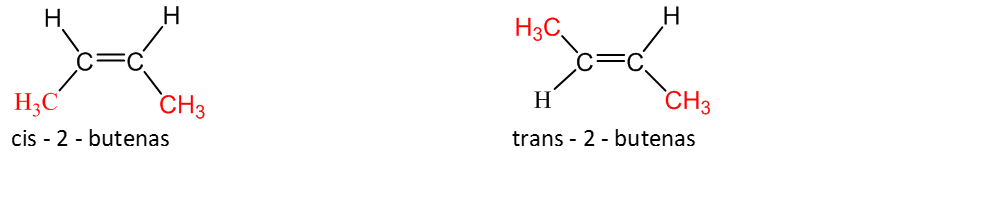
4. Tarpklasinė izomerija. Alkenų ir
cikloalkanų yra ta pati bendroji molekulinė formulė. Todėl, pvz. propenas ir
ciklopropanas yra izomerai.
Paplitimas gamtoje
Alkenai gamtoje mažai paplitę. Jų yra vabzdžių (bičių, musių) feromonuose. Žemesniųjų alkenų nedideliais kiekiais būna naftos dujose, aukštesniųjų – kai kurių rūšių naftoje.
Gavimas
Pramonėje etenas gaunamas iš gamtinių dujų, naftos pirolizės bei krekingo metu.
Laboratorijoje alkenai gali būti gaunami:
1. Dehidrinant alkanus. Pramonėje ir laboratorijoje alkenai gaunami dehidrinant sočiuosius angliavandenilius. Reakcija atliekama aukštoje temperatūroje, dalyvaujant katalizatoriui – metalų oksidams.
![]()
propanas propenas
2. Hidrinant alkinus:
![]()
propinas propenas
3. Dihalogenalkanus, kuriuose halogeno atomai yra prie gretimų C atomų, veikiant Mg arba Zn:
![]()
1 ,2 - dibrompropanas propenas
4. Halogenalkanus veikiant alkoholiniu kalio šarmo tirpalu:
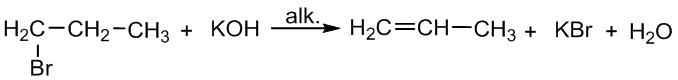
1 - brompropanas propenas
5. Dehidratuojant alkoholius, kaip katalizatorių naudojant koncentruotą sieros rūgštį:
![]()
etanolis etenas
Fizikinės savybės
Pirmieji trys alkenų homologinės eilės nariai turintys (C2 – C4) – dujos, (C5 – C18) – skysčiai, (C19 ir >) – kietos medžiagos. Alkenai netirpsta vandenyje, bet labai gerai tirpsta nepoliniuose tirpikliuose (benzene, trichlormetane, žibale). Jie yra lengvesni už vandenį, virimo temperatūra didėja, didėjant anglies atomų skaičiui molekulėje. Alkenams būdingas specifinis aštrus kvapas.
Cheminės savybės
Alkenams būdingos prisijungimo, oksidacijos ir polimerizacijos reakcijos.
1. Prisijungimo reakcijos.
a) reaguoja su vandeniliu (hidrinimas):
![]()
propenas propanas
b) reaguoja su halogenais (halogeninimas):
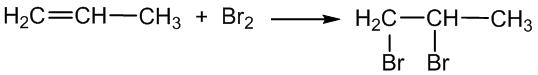
propenas 1, 2 - dibrompropanas
Ši reakcija yra alkenų atpažinimo reakcija – alkenai blukina bromo vandenį.
c) reaguoja su vandenilio halogenidais (Markovnikovo taisyklė: vandenilio atomas prisijungia prie labiau hidrinto anglies atomo, o halogeno atomas – prie kito anglies atomo. Prisijungimas vyksta prie anglies atomų, tarp kurių yra dvigubasis ryšys):
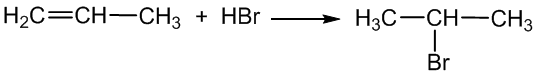
propenas 2 - brompropanas
d) reaguoja su vandeniu (hidratacijos reakcija):
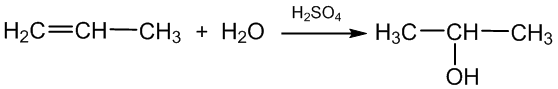
propenas 2 - propanolis
2. Oksidacijos reakcijos.
a) blukina kalio permanganato tirpalą – kokybinė alkenų atpažinimo reakcija:
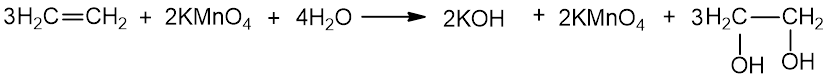
b) aukštoje temperatūroje alkenai dega iki CO2 ir H2O išskirdami didelį kiekį šilumos:
2C3H6 + 9O2 → 6CO2 + 6H2O
3. Polimerizacijos reakcijos.
Vienodų molekulių susijungimas į didesnes vadinamas polimerizacija. Monomeras – pradinis junginys (mažos molekulinės masės), iš kurio sintetinamas polimeras (stambiamolekulis junginys). Polimerizacijos laipsnis n – monomero grandžių skaičius polimero makromolekulėje.
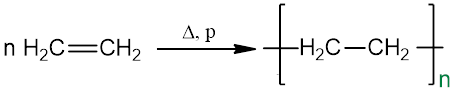
etenas polietenas
(monomeras) (polimeras)
Panaudojimas
Dujinis etenas pagreitina vaisių ir daržovių nokimą, yra žaliava aukšto oktaninio skaičiaus kurui, plastikui, etanoliui, etano oksidui, halogenalkanams gaminti.
Ypač plačiai naudojami alkenų polimerizacijos reakcijų produktai.
6.2.2.2. Alkinai
Angliavandeniliai, kurių bendroji formulė CnH2n-2 ir kurių molekulėse tarp anglies atomų yra vienas trigubasis ryšys, vadinami alkinais.
Nomenklatūra
Bendrojoje alkinų formulėje indeksas n – sveikasis skaičius, rodantis anglies atomų skaičių, nuo kurio priklauso pavadinimas. Alkinų pavadinimai sudaromi su priesaga –in – ir galūne –as, pvz. C2H2 – etinas, C3H4 – propinas ir kt. Pagrindinės nomenklatūros taisyklės pateiktos 6.1. skyriuje. Skirtingai nuo alkanų pagrindinė C atomų grandinė (nebūtinai ilgiausia) turi būti su trigubuoju ryšiu. Ji numeruojama nuo tos pusės, kur arčiau yra trigubasis ryšys. Pvz.:
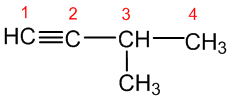
3 - metil - 1 - butinas
Izomerija
Alkinams būdingos šios izomerijos rūšys:
1. Anglies grandinės izomerija (pentino C5H8):

1 - pentinas 3 - metil - 1- butinas
2. Trigubojo ryšio padėties izomerija (pentino C5H8):
![]()
1 - pentinas 2 - pentinas
3. Tarpklasinė izomerija. Alkinų ir dienininių angliavandenilių (alkadienų) yra ta pati bendroji molekulinė formulė. Todėl, pvz. butinas ir butadienas yra tarpusavyje izomerai.
Gavimas
Pramonėje etinas gaunamas kaitinant gamtines dujas (metaną). Šiame procese vienas iš tarpinių produktų yra etinas, kuris greitai šalinamas iš aukštos temperatūros zonos.
![]()
metanas etinas
Laboratorijoje ir pramonėje etiną galima gauti kalcio karbidą veikiant vandeniu:
CaC2 + 2H2O → C2H2 + Ca(OH)2
Tai pats seniausias etino gamybos būdas.
Kiti alkinai laboratorijoje gaunami dihalogenalkanus (halogenų atomai yra prie gretimų anglies atomų) veikiant alkoholiniais šarmų tirpalais:
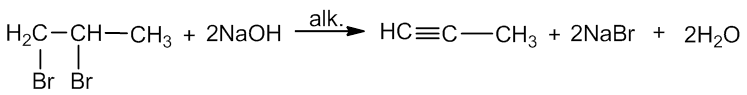
1, 2 – dibrompropanas propinas
Fizikinės savybės
Pirmieji trys alkinų homologinės eilės nariai turintys (C2 – C4) – dujos, (C5 – C16) – skysčiai, (C17 ir >) – kietos medžiagos. Žemesnieji alkinai geriau tirpsta vandenyje negu alkenai ir alkanai. Alkinai gerai tirpsta mažo poliškumo organiniuose tirpikliuose (benzene, dietileteryje, benzine, tetrachlormetane). Alkinų virimo temperatūra ir tankiai šiek tiek didesni, negu atitinkamų alkenų ir alkanų. Kuo didesnė molinė masė, tuo aukštesnė virimo temperatūra.
Etinas (acetilenas) – bespalvės, lengvesnės už orą dujos, mažai tirpios vandenyje. Grynas etinas beveik bekvapis.
Cheminės savybės
Alkinams būdingos prisijungimo, oksidacijos ir polimerizacijos reakcijos.
1. Prisijungimo reakcijos.
a) reaguoja su vandeniliu (hidrinimo reakcija). Priklausomai nuo vandenilio kiekio – gali susidaryti alkenas arba alkanas:
![]()
propinas propenas
![]()
propenas propanas
b) reaguoja su halogenais (halogeninimas):
![]()
propinas 1,2 - dibrompropenas
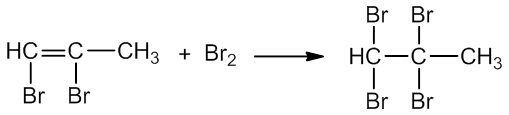
1,2 - dibrompropenas 1,1,2,2 - tetrabrompropanas
Ši reakcija yra alkinų atpažinimo reakcija – alkinai blukina bromo vandenį greičiau negu alkenai.
c) reaguoja su vandenilio halogenidais (Markovnikovo taisyklė: vandenilio atomas prisijungia prie labiau hidrinto anglies atomo, o halogeno atomas – prie kito anglies atomo. Prisijungimas vyksta prie anglies atomų, tarp kurių yra trigubasis ryšys):
![]()
propinas 2 - brompropenas
2 - brompropenas 2,2 - dibrompropanas
d) hidratacijos reakcija (Kučerovo reakcija) vyksta esant sieros rūgšties ir katalizatoriumi naudojant Hg2+ druskas:
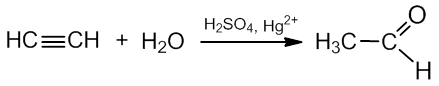
etinas etanalis
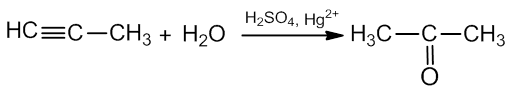
propinas propanonas
2. Oksidacijos reakcijos.
a) blukina kalio permanganato tirpalą – kokybinė alkinų atpažinimo reakcija. Anglies atomų grandinė trūksta trigubojo ryšio vietoje ir susidaro dvi karboksirūgštys:
![]()
propinas metano rūgštis etano rūgštis
b) aukštoje temperatūroje alkinai dega iki CO2 ir H2O išskirdami didelį kiekį šilumos:
C3H4 + 4O2 → 3CO2 + 2H2O
3. Polimerizacijos reakcijos.
Vykdant etino trimerizacijos reakciją ir naudojant katalizatorių – aktyvuotą C, susidaro benzenas:
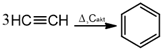
propinas benzenas
Panaudojimas
Iš alkinų plačiausiai naudojamas etinas (acetilenas) sintetinant vinilchloridą (chloreteną), vinilacetileną ir akrilnitrilą, naudojamus polimerizacijos reakcijose. Iš jo gaminamas etanalis, etano rūgštis, ir kiti junginiai. Etino mišinys su deguonimi naudojamas autogeninio metalų suvirinimo ir metalų pjovimo darbams.
6.2.2.3. Dienai
Angliavandeniliai, kurių bendroji formulė CnH2n-2 ir kurių molekulėse tarp anglies atomų yra du dvigubieji ryšiai, vadinami dienais (alkadienais).
Nomenklatūra
Dienų pavadinimai sudaromi su priesaga –dien – ir galūne –as. Pagrindinė grandinė numeruojama nuo tos pusės, kur arčiau yra dvigubasis ryšys. Pvz.:
![]()
2 - metil - 1,3 - butadienas
Izomerija
Dienams būdingos šios izomerijos rūšys:
1. Anglies grandinės izomerija (pentadienas C5H8):
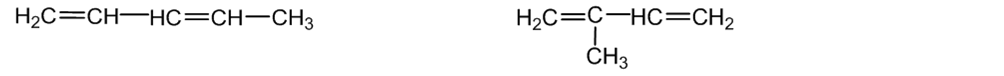
1,3 - pentadienas 2 - metil -1,3 - butadienas
2. Dvigubojo ryšio padėties izomerija (pentadienas C5H8):
![]()
1,3 - pentadienas 1,4 - pentadienas
3. Tarpklasinė izomerija. Alkinų ir dienininių angliavandenilių (alkadienų) yra ta pati bendroji molekulinė formulė. Todėl, pvz. butinas ir butadienas yra tarpusavyje izomerai.
Paplitimas gamtoje
Alkadienai labai paplitę gamtoje, turi malonų kvapą, naudojami kaip eteriniai aliejai, balzamai, natūralus kaučiukas. Atogrąžų augalų pieninėse sultyse (latekse) yra izopreno polimero, kuris vadinamas natūraliuoju kaučiuku. Daugiausia jo gaunama iš Brazilijoje augančio medžio hevėjos. Natūralus kaučiukas susidaro polimerizuojantis 2 - metil - 1,3 butadienui. Polimero fragmento formulė:
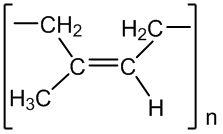
Gavimas
1,3 - butadienas gaunamas dehidrinant ir dehidratuojant etanolį (S. Lebedevo būdas):
![]()
etanolis 1,3 - butadienas
Pramonėje alkadienai gaunami dehidrinant alkanus (daugumoje esančius naftos dujose):
![]()
butanas 1,3 - butadienas
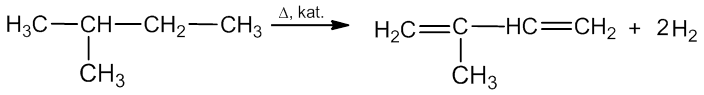
2 - metilbutanas 2 - metil-1,3 - butadienas
Fizikinės savybės
Alkadienai – tai bespalvės dujos ar skysčiai, kuriems būdingas nemalonus kvapas. Pavyzdžiui, 1,3 - butadienas yra dujos (n. s.), kurios skystėja -4,5 °C temperatūroje, o 2 - metil - 1,3 - butadienas – skystis, kurio virimo temperatūra yra 34,1 °C.
Cheminės savybės
Dienams būdingos prisijungimo, oksidacijos ir polimerizacijos reakcijos.
1. Prisijungimo reakcijos.
a) reaguoja su vandeniliu (hidrinimo reakcija). Priklausomai nuo vandenilio kiekio – gali susidaryti alkenas arba alkanas:
![]()
1,3 - butadienas 2 - butenas
![]()
1,3 - butadienas butanas
b) reaguoja su halogenais (halogeninimas). Priklausomai nuo halogeno kiekio – gali susidaryti dihalogenalkenas arba tetrahalogenalkanas:
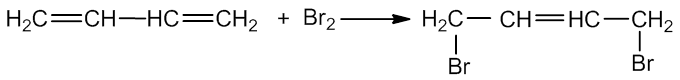
1,3 - butadienas 1,4 - dibrom - 2 - butenas
![]()
1,3 - butadienas 1,2,3,4 - tetrabrombutanas
Ši reakcija yra alkadienų atpažinimo reakcija – alkadienai blukina bromo vandenį greičiau negu alkenai.
c) reaguoja su vandenilio halogenidais (Markovnikovo taisyklė: vandenilio atomas prisijungia prie labiau hidrinto anglies atomo, o halogeno atomas – prie kito anglies atomo. Prisijungimas vyksta prie anglies atomų, tarp kurių yra dvigubasis ryšys):
![]()
1,3 - butadienas 3 - brom -1 - butenas
2. Oksidacijos reakcijos. Alkadienai dega ore iki CO2 ir H2O išskirdami didelį kiekį šilumos:
2C4H6 + 11O2 → 8CO2 + 6H2O
3. Polimerizacijos reakcijos. Dienai turi du dvigubuosius ryšius, todėl veikiant slėgiui, katalizatoriui ir temperatūrai π ryšius galima nutraukti. Polimerizuojant dienus, gaunami kaučiukai:

arba

1,3 - butadienas butadieninis (divinilinis) kaučiukas
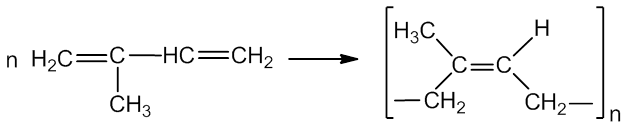
2 - metil-1,3 - butadienas izopreninis kaučiukas
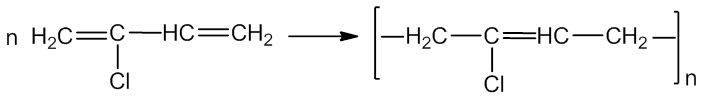
2 - chlor-1,3 - butadienas cloropreninis kaučiukas
Panaudojimas
Pramonėje dienai naudojami sintetiniam kaučiukui gaminti. Iš natūralaus ir sintetinio kaučiuko gaminamos padangos, konvejerių juostos, dirbtinė oda, batų padai ir kt.
6.2.2.4. Arenai (aromatiniai angliavandeniliai)
Anglies ir vandenilio junginiai, kurių molekulėse yra benzeno ciklas, vadinami arenais (aromatiniais angliavandeniliais). Jų bendroji formulė CnH2n-6.
Nomenklatūra ir izomerija
Paprasčiausias arenas yra benzenas (C6H6). Benzeno struktūrinė formulė:

Benzenas be vieno vandenilio atomo vadinamas fenilo pakaitu –C6H5.
Aromatinių angliavandenilių nomenklatūra skiriasi nuo kitų angliavandenilių savo trivialiaisiais pavadinimais (6.1. skyrius), kurie vartojami dažniau nei IUPAC pavadinimai.
![]()
metibenzenas (toluenas)
Jeigu benzeno cikle yra ne vienas, o keli pakaitai, tai jame anglies atomai numeruojami taip, kad skaičių (kurie žymi pakaitų vietas) suma būtų mažiausia. Pakaitų pavadinimai rašomi abėcėlės tvarka:

Pakaitų padėtys nurodomos skaičiais arba priešdėliais:
orto- kai pakaitai išsidėstę prie gretimų anglies atomų. Rašant pavadinimą, nurodoma tik raidė o - :
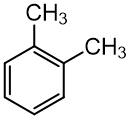
o - dimetilbenzenas (1,2 - dimetilbenzenas)
meta- kai pakaitai vienas nuo kito atskirti vienu anglies atomų. Rašant pavadinimą, nurodoma tik raidė m - :
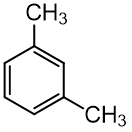
m - dimetilbenzenas (1,3 - dimetilbenzenas)
para- kai pakaitai vienas nuo kito atskirti dviem anglies atomais. Rašant pavadinimą, nurodoma tik raidė p - :
![]()
p - dimetilbenzenas (1,4 - dimetilbenzenas)
Paplitimas gamtoje
Daug aromatinių junginių randama naftoje ir akmens anglių perdirbimo produktuose. Benzenas ir jo homologai yra toksiški, o kai kurie sukelia vėžį. Buvimas ten, kur ore yra benzeno, randamo prastesnės kokybės cigaretėse, benzino garuose, žmogui gali sukelti įvairius sveikatos sutrikimus. Atliekant eksperimentus su aromatiniais junginiais būtina dirbti traukos spintoje.
Gavimas
Aromatinių angliavandenilių šaltiniai yra akmens anglių koksavimo produktai (degutas, koksavimo dujos) ir nafta. Gavimo būdai:
1. Dehidrinant alkanus:
![]()
heksanas benzenas
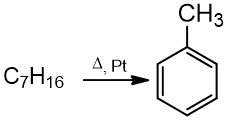
heptanas metilbenzenas (toluenas)
2. Dehidrinant cikloalkanus:
![]()
cikloheksanas benzenas
3. Trimerizuojant etiną susidaro benzenas:
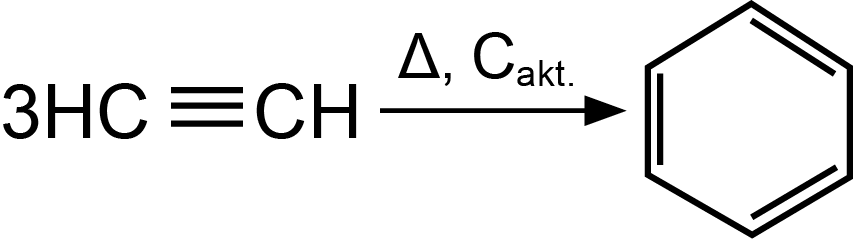
etinas benzenas
Fizikinės savybės
Benzenas kambario temperatūroje yra specifinio kvapo bespalvis, takus, skaidrus, savito kvapo, , netirpstantis vandenyje skystis. Lengvesnis už vandenį. Šaldomas lengvai kristalizuojasi. Benzeno lydymosi temperatūra +5,53 °C, virimo temperatūra 80,1 °C. Benzenas ir jo homologai toksiški, kai kurie kancerogeniški.
Cheminės savybės
Benzenui būdingos pakaitų, prisijungimo reakcijos. Aromatinis žiedas labai atsparus oksidatoriams. Tik su dideliu vargu labai stiprūs oksidatoriai gali ji suardyti. Kai kurie benzeno dariniai polimerizuojasi.
1. Pakaitų reakcijos. Benzeno ar kito aromatinio žiedo vandenilio atomus galima pakeisti halogenais, nitro, sulfo ir kitomis grupėmis.
a) reaguoja su halogenais:
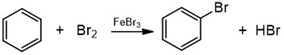
benzenas brombenzenas
b) nitrinasi. Veikiant aromatinius žiedus azoto ir sieros rūgščių mišiniu, vieną vandenilį pakeičia azoto rūgšties liekana – nitrogrupė (nitrinimo reakcija).
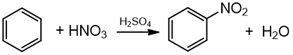
benzenas nitrobenzenas
2. Prisijungimo reakcijos. Šios reakcijos vyksta suardžius stabilią benzeno ciklinę sistemą.
a) reaguoja su vandeniliu (hidrinimo reakcija):
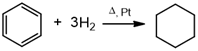
benzenas cikloheksanas
b) reaguoja su halogenais (halogeninimas).
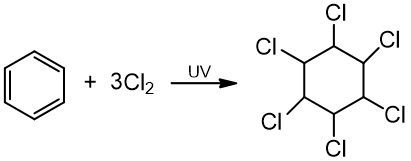
benzenas 1,2,3,4,5,6 - heksachlorcikloheksanas
3. Oksidacijos reakcijos. Arenai dega ore rūkstančia liepsna iki CO2 ir H2O:
2C6H6 + 15O2 → 12CO2 + 6H2O
Benzenas su vandeniniu kalio permanganato tirpalu nereaguoja, o alkilbenzenai oksiduojasi iki benzenkarboksirūgšties:
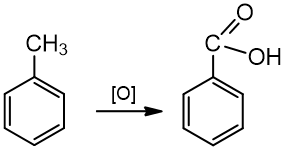
metilbenzenas benzenkarboksirūgštis
4. Polimerizacijos reakcijos Vinilbenzenas (stirenas) gali polimerizuotis iki polivinilbenzeno (polistireno):
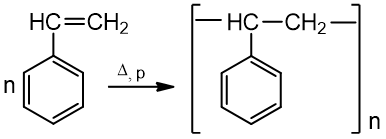
stirenas polistirenas
Panaudojimas
Benzenas – yra labiausiai paplitęs arenas. Jis – geras riebalų, kaučiukų, lakų, polimerų tirpiklis. Iš benzeno ir tolueno gaminami dažai, vaistai, sprogstamosios medžiagos (trinitrotoluenas), augalų apsaugos priemonės, plastikai, sintetiniai pluoštai.
6.3. Alkoholiai ir fenoliai
Alkoholiais vadinami junginiai, turintys vieną arba kelias hidroksigrupes (–OH).
Pagal hidroksigrupių skaičių molekulėje alkoholiai skirstomi į:
- vienhidroksilius;
- daugiahidroksilius.
Aromatinių angliavandenilių junginiai, turintys molekulėje vieną arba kelias –OH grupes, prisijungusias prie aromatinio žiedo anglies atomų, vadinami fenoliais.
6.3.1. Vienhidroksiliai alkoholiai
Vienhidroksiliai alkoholiai – angliavandenilių junginiai, kurių molekulėse vienas vandenilio atomas pakeistas hidroksigrupe (–OH). Jų bendroji formulė CnH2n+1OH.
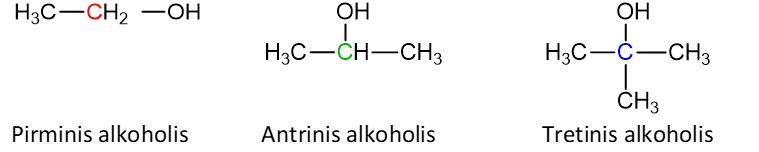
Pagal funkcinės hidroksigrupės padėtį alkholiai gali būti pirminiai, antriniai arba tretiniai.
Pirminiu alkoholiu vadiname tokį alkoholį, kuriame funkcinė grupė yra prisijungusi prie pirminio anglies atomo.
- Antriniu alkoholiu vadiname tokį alkoholį, kuriame funkcinė grupė yra prisijungusi prie antrinio anglies atomo.
- Tretiniu alkoholiu vadiname tokį alkoholį, kuriame funkcinė grupė yra prisijungusi prie tretinio anglies atomo.
- Kas tas pirminis, antrinis arba tretinis C atomas?
Atsakymas. Pagal tai, su keliais šalia esančiais anglies atomais yra susijungę anglies atomai, jie gali būti pirminiai, antriniai, tretiniai arba ketvirtiniai:
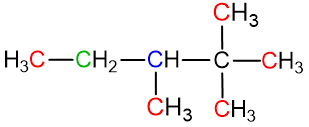
Raudona spalva parašytas C atomas yra pirminis;
Žalia – antrinis;
Mėlyna – tretinis;
Juoda – ketvirtinis.
Nomenklatūra
Bendrojoje alkoholių formulėje indeksas n – sveikasis skaičius, rodantis anglies atomų skaičių, nuo kurio priklauso pavadinimas. Alkoholių pavadinimai sudaromi su priesaga –ol – ir galūne –is, pvz. C2H5OH – etanolis, C3H7OH – propanolis ir kt. Pagrindinė C atomų grandinė (nebūtinai ilgiausia) turi būti su funkcine grupe. Ji numeruojama nuo tos pusės, kur arčiau yra funkcinė hidroksigrupė. Pvz.:
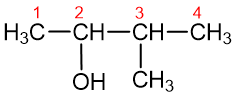
3 - metil - 2 - butanolis
Izomerija
Alkoholiams būdingos šios izomerijos rūšys:
1. Anglies grandinės izomerija:
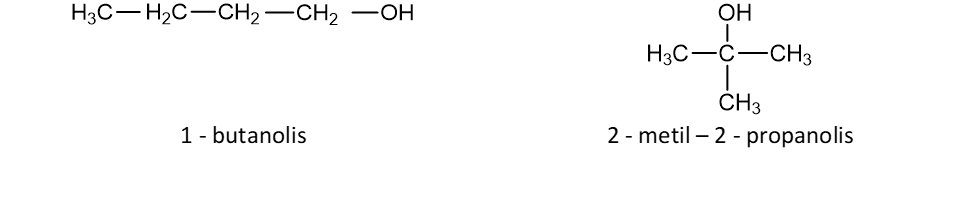
2. Funkcinės grupės izomerija (C3H8O):

3. Tarpklasinė izomerija. Alkoholių ir eterių yra ta pati bendroji molekulinė formulė. Todėl, pvz. etanolis ir dimetileteris yra tarpusavyje izomerai:

Paplitimas gamtoje
Etanolis – tai žinduolių ir žmonių organizmuose vykstančių reakcijų produktas. Alkoholio nevartojančio žmogaus organizme normali etanolio koncentracija kraujyje kinta nuo 0,001 iki 0,1 g/l (vadinasi, etanolis yra endogeninė, t. y. gaminama organizmo, medžiaga). Etanolio kiekis kraujyje matuojamas promilėmis ‰ (promilė – tūkstantoji dydžio dalis).
Gavimas
1. Laboratorijoje alkoholius galima gauti halogenintus angliavandenilius veikiant natrio, kalio ir kalcio hidroksidų vandeniniais tirpalais.
C2H5Cl + KOH → C2H5OH + KCl
chloretanas etanolis
2. Pramonėje metanolis gaunamas aukštoje temperatūroje ir slėgyje reaguojant tarpusavyje anglies monoksidui su vandeniliu, katalizatoriais naudojant Cu, ZnO:
CO + 2H2 → CH3OH
metanolis
3. Alkoholiai gaunami hidratuojant alkenus:
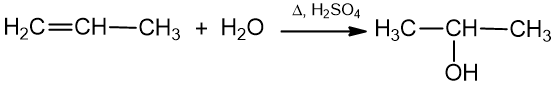
propenas 2 - propanolis
4. Etanolis gaunamas fermentacijos metu, beorėje erdvėje iš gliukozės:
C6H12O6→ 2C2H5OH + 2CO2
gliukozė etanolis
5. Alkoholiai susidaro redukuojant karbonilinius junginius (žr. 6.4. skyrių).
Fizikinės savybės
Vienhidroksiliai sotieji pirminiai alkoholiai su trumpa anglies atomų grandine – skysčiai, o aukštesnieji, t. y. didesnės santykinės molekulinės masės, pavyzdžiui, C12H25OH, – kietosios medžiagos. Pirmųjų homologinės eilės narių kvapas silpnas, butanolio, pentanolio ir heksanolio – stiprus, nemalonus. Didelės molinės masės alkoholiai – bekvapiai. Didėjant alkoholių santykinei molekulinei masei, didėja jų virimo temperatūra. Alkoholių virimo temperatūra daug aukštesnė negu panašios santykinės molekulinės masės atitinkamų angliavandenilių. Šį reiškinį galima paaiškinti vandenilinių ryšių (žr. 2.4. skyrių) susidarymu tarp alkoholio molekulių ir tarp alkoholio ir vandens molekulių:
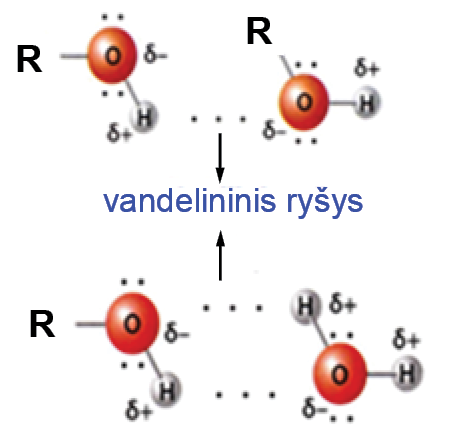
Alkoholiai turi polinę hidroksigrupę, kuri gali sudaryti vandenilinius ryšius su vandeniu arba su kitomis alkoholių molekulėmis. Vandeniliniai ryšiai tarp alkoholių ir vandens susidaro dėl deguonies atomo laisvųjų elektronų porų: šiais elektronais deguonis gali sudaryti silpnus vandenilinius ryšius su kitos molekulės (alkoholio arba vandens) dalinai teigiamais vandenilio atomais.
Vandeniliniai ryšiai taip pat lemia metanolio, etanolio ir propanolio neribotą tirpumą vandenyje. Kitų vienhidroksilių alkoholių tirpumas vandenyje ribotas. Tirpumas mažėja dėl didėjančios netirpios anglies grandinės dalies molekulėje.
Cheminės savybės
Alkoholiams nebūdingos nei rūgštinės, nei bazinės savybės, todėl indikatorių spalvos jie nekeičia (žr. 5.2.8. skyrių).
1. Alkoholiai reaguoja su aktyviais metalais (susidaro alkoholiatai), bet nereaguoja su šarmais:
![]()
etanolis kalio etanoliatas
2. Alkoholiai reaguoja su koncentruotais vandenilio halogenidais:
![]()
etanolis brometanas
3. Alkoholių dehidratavimas – vandens molekulės eliminavimas. Priklausomai nuo temperatūros, gali susidaryti alkenai arba eteriai:
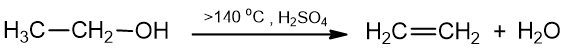
etanolis etenas
![]()
etanolis dimetileteris
4. Alkoholiai reaguoja su karboksirūgštimis ir sudaro esterius (žr. 6.6. skyrių).
5. Alkoholiai lengvai oksiduojasi. Pirminiai alkoholiai oksiduojasi iki adehidų, o antriniai – iki ketonų. Tretiniai alkoholiai nesioksiduoja (žr. 6.4. skyrių).
6. Alkoholiai ore dega melsva liepsna:
C2H5OH + 3O2 → 2CO2 + 3H2O
Panaudojimas. Poveikis žmogui
Etanolis vartojamas alkoholinių gėrimų gamyboje, medicinoje, parfumerijos pramonėje. Techninis etilo spiritas – sintetinio kaučiuko, dirbtinio šilko, organinio stiklo, plastmasių, lakų, dažų, fotografijos reikmenų gamybos žaliava. Kai kuriose šalyse etanolis yra degalai. Į benziną įterpus iki 15% etanolio, pagerėja degalų savybės, į aplinką patenka mažiau teršalų.
Etanolis naudojamas kaip tirpiklis.
Alkoholio vartojimas dideliais kiekiais yra pavojingas žmogaus organizmui. Medikai teigia, kad 4,5-5,0 g/l alkoholio dozė žmogaus kraujyje daugeliui yra mirtina. Ši dozė atitinka 300 ml 96 % koncentracijos alkoholio. Dažnai vartojantys alkoholį žmonės ilgainiui suserga alkoholizmu. Etanolis yra kepenų, širdies, nervų ir lytinių ligų priežastis.
Metanolis labai nuodingas junginys. Išgėręs jo tik 2 g, žmogus gali apakti, o nuo 40 g mirti. Pagal kvapą, skonį ir išvaizdą metanolis labai panašus į etanolį. Apsinuodijimo metanoliu priešnuodis – etanolis.
6.3.2. Daugiahidroksiliai alkoholiai
Daugiahidroksiliai alkoholiai – tai organiniai junginiai, kurių molekulėse yra kelios hidroksigrupės, sujungtos su angliavandenilio pakaitais.
Nomenklatūra
Paprasčiausi daugiahidroksiliai alkoholiai yra 1,2-etandiolis (etilenglikolis), 1,2,3-propantriolis (glicerolis):

Izomerija
Polihidroksiliams alkoholiams būdinga funkcinių grupių tarpusavio padėties izomerija:

Gavimas
1. Polihidroksilius alkoholius galima gauti halogenintus angliavandenilius veikiant vandeniu:
![]()
1,2 - dichloretanas 1,2 - etandiolis
2. Etilenglikolis susidaro oksiduojant eteną kalio permanganato tirpalu:
![]()
3. Glicerolis gaunamas iš riebalų, juos hidrolizuojant.
1,2 - etandiolio ir 1,2,3 - propantriolio fizikinės savybės
1,2-etandiolis (etilenglikolis) – tai bespalvis, klampus, labai nuodingas, gerai tirpstantis vandenyje (dėl vandenilinių ryšių tarp vandens ir daugiahidroksilių alkoholių susidarymo) skystis. Etilenglikolis – saldus, lipnus skystis, todėl kartais jo išgeriama per klaidą (vietoj likerio). Mirtina dozė – 100–150 ml, toksinė – 50 ml.
Etilenglikolis yra kraujagyslių ir protoplazmos nuodas. Labiausiai pažeidžiamios kepenys ir inkstai. Ūmiai apsinuodijęs žmogus miršta po 1-2 parų.
1,2,3-propantriolis (glicerolis) – tai bespalvis, bekvapis, saldus, klampus, gerai tirpstantis vandenyje bei labai gerai sugeriantis drėgmę skystis. Geras tirpiklis – tirpina daugelį organinių ir neorganinių junginių. Priešingai negu 1,2-etandiolis, jis visai nenuodingas, todėl naudojamas ne tik dervų, sprogstamųjų medžiagų, bet ir vaistų, kosmetikos gamyboje bei maisto pramonėje.
Cheminės savybės
1. Polihidroksiliai alkoholiai kaip ir vienhidroksiliai reaguoja su šarminiais metalais, bet nereaguoja su šarmais:
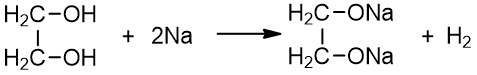
1,2 - etandiolis natrio etilenglikoliatas
2. Polihidroksiliai alkoholiai kaip ir vienhidroksiliai reaguoja su koncentruotais vandenilio halogenidais:
![]()
1,2 - etandiolis 1,2 - dichloretanas
3. Reaguoja su šviežiai pagamintu vario hidroksidu – polihidroksilių alkoholių atpažinimo reakcija. Susidaro ryškiai mėlynos spalvos tirpalas (vario gliceratas, vario glikoliatas):
![]()
1,2 - etandiolis vario glikoliatas
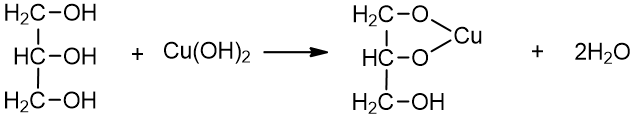
1,2,3 - propantriolis vario gliceratas
4. Glicerolis reaguoja su azoto (nitrato) rūgštimi. Esterinimo reakcijos (žr. 6.6. skyrių) metu susidaro nitroglicerolis, kuris naudojamas medicinoje bei sprogstamųjų medžiagų gamybai:
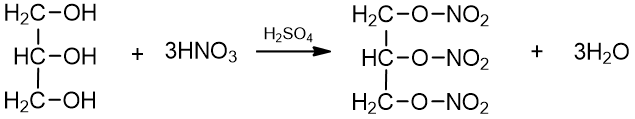
glicerolis nitroglicerolis
Panaudojimas
35–55% vandeninis etilenglikolio tirpalas labai geras antifrizas (medžiaga pažeminanti skysčių užšalimo temperatūrą) – užšąla daug žemesnėje temperatūroje negu vanduo (36,4% vandeninis etilenglikolio tirpalas užšąla –20°C temperatūroje, o 52,6% koncentracijos užšąla –40°C temperatūroje). Jo yra stabdžių skystyje. Etilenglikolis naudojamas lavsano, poliuretano ir kt. plastikų gamybai.
Glicerolis naudojamas dervų, sprogstamųjų medžiagų, vaistų bei kosmetikos gamyboje, odos bei maisto pramonėse.
6.3.3. Fenoliai
Aromatiniai angliavandenilių dariniai, kurių molekulėse hidroksigrupė susijungusi su benzeno ciklu, vadinami fenoliais.
Nomenklatūra ir izomerija
Fenoliai gali būti vienhidroksiliai ir daugiahidroksiliai:
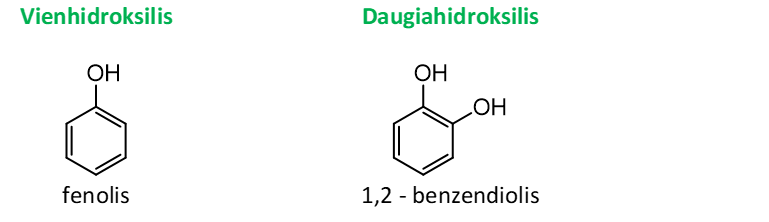
Pagal IUPAC nomenklatūrą fenolius priimta vadinti kaip pirmojo jų eilės nario fenolio darinius.
Anglies atomus benzeno cikle pradedama numeruoti nuo hidroksigrupės, pavyzdžiui, 3-metilfenolis:
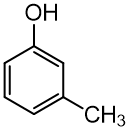
Fenoliams būdinga tarpklasinė izomerija. Medžiagos, kurių molekulėse hidroksigrupė nėra tiesiogiai prisijungusi prie benzeno ciklo, nėra vadinamos fenoliais.
Jeigu hidroksigrupė prie benzeno ciklo prisijungusi netiesiogiai, o per –CH2– ar kitą ryšį, toks darinys vadinamas aromatiniu alkoholiu.
2-metilfenolis ir fenilmetanolis yra izomerai (ta pati molekulinė formulė C7H8O), bet nėra homologai.

Gavimas
Fenolis pramonėje sintetinamas iš benzeno. Pirmiausia iš benzeno sudaromas izopropilbenzenas, o šis verčiamas fenoliu. Šalutinis produktas – propanonas.
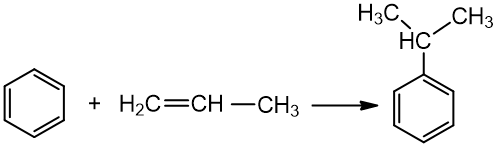
benzenas izopropilbenzenas
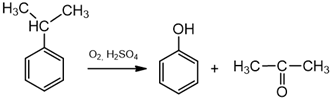
izopropilbenzenas fenolis propanonas
Laboratorijoje fenolis gaunamas taip pat iš benzeno. Pirmiausia benzenas veikiamas chloru - susidaro chlorbenzenas. Po to chlorbenzenas reaguoja su šarmu ir susidaro fenolis.
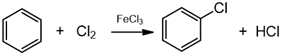
benzenas chlorbenzenas
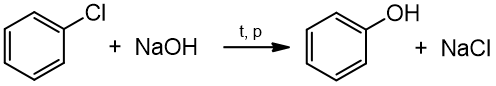
chlorbenzenas fenolis
Fizikinės savybės
Fenolis – specifinio (guašo) kvapo kieta medžiaga. Ore bespalviai fenolio kristalai greitai oksiduojasi ir tampa rausvos spalvos. Šaltame vandenyje mažai tirpus (6,7 g/100 g vandens), o karštame gali tirpti neribotai. Fenolio lydymosi temperatūra 40,9 °C, virimo temperatūra 182 °C.
Cheminės savybės
Vandeniniam fenolio tirpalui būdingos silpnos rūgštinės savybės. Dėl šios priežasties vandeninis fenolio tirpalas vadinamas karbolio rūgštimi.
1. Reaguoja su aktyviais metalais:
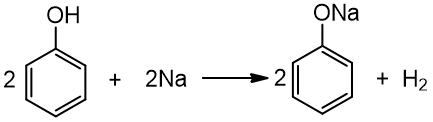
fenolis natrio fenoliatas
2. Reaguoja su šarmais (skirtingai negu vienhidroksiliai ir daugiahidroksiliai alkoholiai):
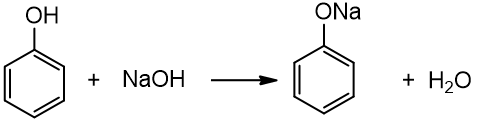
fenolis natrio fenoliatas
3. Reaguoja su bromo vandeniu – brominimo reakcija:
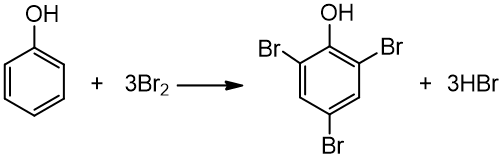
fenolis 2,4,6 – tribromfenolis
4. Reaguoja su nitrato (azoto) rūgštimi – nitrinimo reakcija:
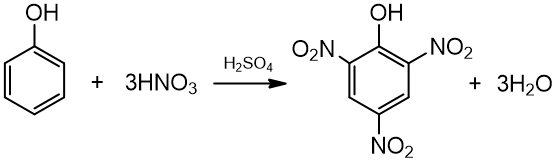
fenolis 2,4,6 – trinitrofenolis (pikrino rūgštis)
5. Fenolio kokybinė atpažinimo reakcija – su FeCl3 tirpalu susidaro violetinės spalvos tirpalas:
6C6H5OH + FeCl3 → 3HCl + H3[Fe(OC6H5)6]
6. Fenoliui būdingos polikondensacijos reakcijos.
Panaudojimas
Fenoliai naudojami dervoms, poliamidams, dažikliams, vaistams, baktericidams, pesticidams, sprogstamosioms medžiagoms gaminti. Fenolis kaip antiseptinė priemonė naudojama medicinoje ir stomatologijoje.
6.4. Karboniliniai junginiai
Karboniliniai junginiai – tai organiniai junginiai kurių molekulėje yra karbonilo grupė:
![]()
Karboniliniai junginiai skirstomi į aldehidus ir ketonus, kurių funkcinės grupės:
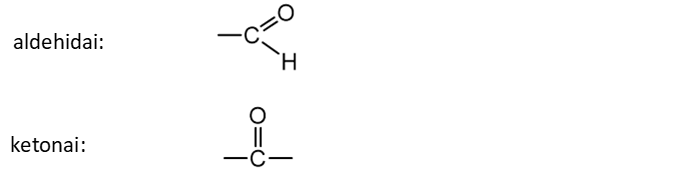
Nomenklatūra
Bendrojoje karbonilinių junginių formulėje (CnH2nO) indeksas n – sveikasis skaičius, rodantis anglies atomų skaičių, nuo kurio priklauso pavadinimas. Aldehidų pavadinimai sudaromi su priesaga –al – ir galūne –is, pvz. C2H4O – etanalis, C3H6O – propanalis ir kt. Pagrindine aldehido grandinė yra ta, kurioje yra funkcinė karbonilo grupė. Karbonilo grupės C atomas visuomet yra pirmas ir rašant aldehido pavadinimą jo padėtis nenurodoma. Pvz.:
![]()
etanalis
Ketonų pavadinimai sudaromi su priesaga –on – ir galūne –as, pvz. C3H6O – propanonas, C4H8O – 2 - butanonas ir kt. Skirtingai nei aldehidus, vardinant ketonus būtina nurodyti karbonilo grupės vietą, jeigu grandinėje yra daugiau nei 4 anglies atomai. Pvz.:
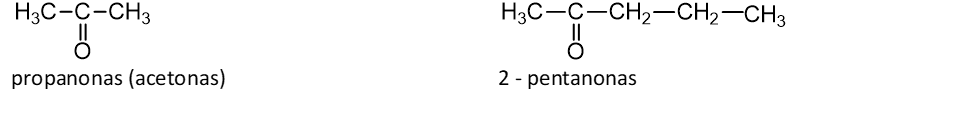
Izomerija
Tą pačią molekulinę formulę turintys aldehidai ir ketonai yra vieni kitiems izomerai, pvz.: propanalis ir propanonas (molekulinė formulė C3H6O).
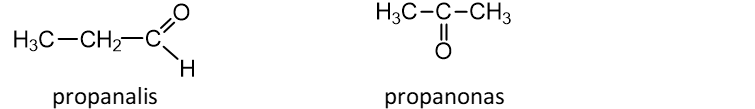
Aldehidams ir ketonams būdinga anglies atomų grandinės izomerija (molekulinė formulė C4H8O):

Ilgesnės grandinės ketonams būdinga dar ir funkcinės karbonilo grupės padėties izomerija (2 – pentanonas, 3 – pentanonas).
Paplitimas gamtoje
Karboniliniai
junginiai – vieni iš labiausiai paplitusių gamtinių junginių. Daugelis jų yra
kvapūs junginiai, randami augaluose ir gyvūnų organizmuose. Pvz. furonolis išsiskiria kepant mėsą, todėl
mes jaučiame jo kvapą, korilonas
karamelės skonio sudėtinė dalis, vanilino
yra vanilėje, demaskenonas lemia
rožių kvapą, bitės radusios nektaro, išskiria citralį. Tarpinis medžiagų apykaitos junginys etanalis nuolat
susidaro žmogaus organizme.
Gavimas
Pramonėje:
- metanalis gaunamas oksiduojant metaną oro deguonimi:
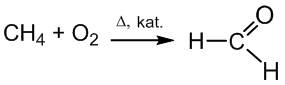
metanalis
- etanalis gaunamas hidratuojant etiną (žr. 6.2.2.2. skyrių):
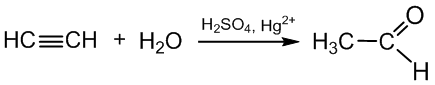
etinas etanalis
Laboratorijoje aldehidai gaunami oksiduojant (oksidatorius vario (II) oksidas) pirminius alkoholius, o ketonai – antrinius alkoholius:
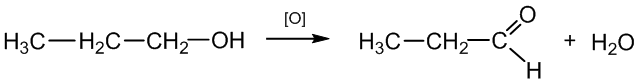
1 - propanolis propanalis
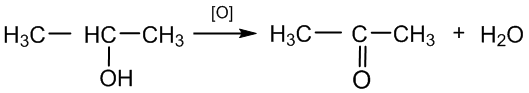
2 - propanolis propanonas
Fizikinės savybės
Metanalis – bespalvės, aštraus kvapo dujos. Jo tirpalas vandenyje (~40%) vadinamas formalinu. Kiti žemesnieji aldehidai ir ketonai (C2 – C4) – lakūs, specifinio kvapo skysčiai, kurie maišosi beveik su visais organiniais tirpikliais, gerai tirpsta vandenyje. Didėjant aldehidų molinei masei, jų lakumas ir tirpumas vandenyje mažėja. Aukštesnieji karboniliniai junginiai (nuo C12) – bekvapės, vandenyje netirpios, neaukštos lydymosi temperatūros kietosios medžiagos. Karbonilinių junginių virimo temperatūros yra daug žemesnės nei alkoholių, turinčių tiek pat anglies atomų. Šis skirtumas yra todėl, kad tarp karbonilinių junginių nesusidaro vandeniliniai ryšiai.
Cheminės savybės
Aldehidams būdingos prisijungimo, oksidacijos ir polimerizacijos reakcijos.
1. Prisijungimo reakcijos. Prisijungia vandenilį ir virsta alkoholiais (hidrinimo reakcija):
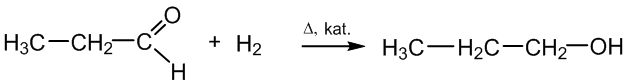
propanalis 1 - propanolis
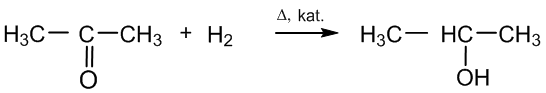
propanonas 2 - propanolis
2. Oksidacijos reakcijos. Oksiduojant aldehidus susidaro karboksirūgštys.
a) Sidabrinio veidrodžio reakcija – kokybinė aldehidų atpažinimo reakcija – aldehidai veikiami sidabro oksido amoniakiniu tirpalu. Įvykus reakcijai, mėgintuvėlio sienelės pasidengia plona veidrodinio sidabro plėvele:
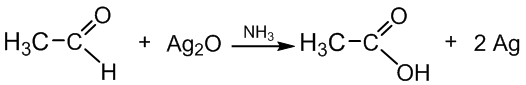
etanalis etano rūgštis
b) Varinio veidrodžio reakcija – kokybinė aldehidų atpažinimo reakcija – aldehidai veikiami šviežiai pagamintu Cu(OH)2. Reakcija vyksta kaitinant – pradžioje susidaro geltonos vario (I) hidroksido nuosėdos, o vėliau susidaro raudonos spalvos Cu2O:
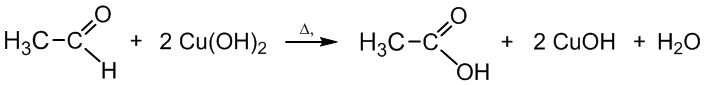
etanalis etano rūgštis geltonos nuosėdos
![]()
Raudonai rudos nuosėdos
3. Polimerizacijos reakcijos.
Metanalis polimerizacijos ir polikondensacijos reakcijose naudojamas polimerų gavimui.
Panaudojimas
Dauguma aldehidų yra naudojami maisto pramonėje, nes yra kvapūs. Metanalis naudojamas vaistų ir dažiklių gamybai, formalinas (metanalio vandeninis tirpalas) – baltymams denatūruoti, dezinfekcijai. Etanalis naudojamas etano rūgščiai gaminti. Propanonas (acetonas) ir kiti ketonai yra geri lakų, dažiklių bei sintetinių dervų tirpikliai.
6.5. Esteriai
Esteriai – organiniai junginiai, kurie susidaro rūgštims reaguojant su alkoholiais. Esterio funkcinė grupė:
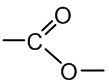
Bendroji esterių formulė yra:
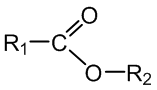
R1, R2 – angliavandenilių pakaitai.
Nomenklatūra
Pagal IUPAC nomenklatūrą esterių pavadinimai sudaromi taip: pirmiausia nurodomas alkoholio pakaitas su galūne –il, po to karboksirūgšties pavadinimas pridedant priesagą –oat– ir galūnę –as, pvz.:
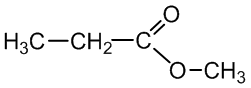
metilpropanoatas
Izomerija
Esteriams būdinga anglies atomų grandinės bei tarpklasinė izomerija.
1. Anglies atomų grandinės izomerija (molekulinė formulė C4H8O2):

2. Tarpklasinė izomerija. Karboksirūgščių ir esterių yra ta pati bendroji molekulinė formulė. Todėl, pvz. etano rūgštis ir metilmetanoatas yra tarpusavyje izomerai.

Paplitimas gamtoje
Esterių gamtoje yra labai daug kur. Jų yra įvairiose gėlėse, vaisiuose, eteriniuose aliejuose. Pvz. izopentilpentanoatas suteikia būdingą kvapą bananams, o etilbutanoatas – ananasams. Esterių yra riebaluose ir vaškuose.
Gavimas
Esterių susidarymo reakcija vadinama esterinimo reakcija. Laboratorijoje esterinimo reakcija vyksta reaguojant karboksirūgštims su alkoholiais. Reakcija yra grįžtamoji. Norint gauti daugiau produkto (esterio) paprastai naudojama koncentruota sieros rūgštis, kuri sugeria vandenį. Bendroji esterinimo reakcijos lygtis:
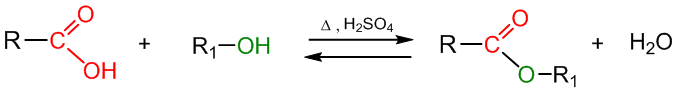
Iš bendrosios reakcijos lygties matyti, kad hidroksigrupė atskyla nuo karboksirūgšties molekulės, o vandenilio atomas – nuo alkoholio molekulės.
Fizikinės savybės
Monokarboksirūgščių ir alkoholių esteriai yra lengvesni už vandenį, lakūs, dažniausiai malonaus kvapo skysčiai. Esterių virimo ir lydymosi temperatūros yra žemesnės negu atitinkamų rūgščių, nes tarp esterių molekulių nesusidaro vandeniliniai ryšiai. Vandenyje tirpūs tik nedidelės molekulinės masės esteriai.
Cheminės savybės
Esteriai hidrolizuojasi (reaguoja su vandeniu). Reakcija yra grįžtamoji kuomet katalizatoriumi naudojama sieros rūgštis:

Metilpropanoatas propano rūgštis metanolis
Hidrolizės reakcija yra negrįžtamoji, kuomet katalizatoriumi naudojamas šarmas. Šios reakcijos vadinamos muilinimo reakcijomis. Jų metu susidaro karboksirūgšties druska ir alkoholis:
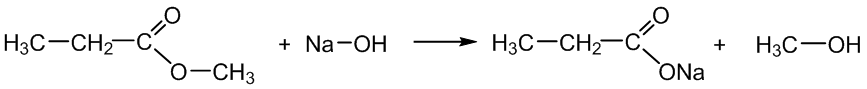
Metilpropanoatas natrio propanoatas metanolis
Panaudojimas
Labai daug esterių naudojami kaip maisto priedai: dedama į gaiviuosius gėrimus, saldainius bei į kitus maisto produktus. Kai kurie esteriai yra tirpikliai. Gyvūnų vaškas naudojamas parfumerijoje tepalų ir kremų gamyboje.
Esteriai taip pat plačiai naudojami plastikų bei sintetinio pluošto gamyboje.
6.6. Karboksirūgštys
Karboksirūgštys – organiniai junginiai, kurie turi vieną ar kelias karboksigrupes:
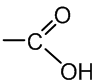
Bendroji karboksirūgščių formulė yra CnH2nO2 arba R–COOH, kur R – pakaitas.
Karboksirūgštys pagal karboksigrupių skaičių molekulėje skirstomos į:
- monokarbosirūgštis (gr. monos – vienas);
- dikarboksirūgštis (gr. di – du);
- polikarboksirūgštis (gr. polys – didelis, gausus).
Karboksirūgštys pagal pagrindinės anglies grandinės sudėtį skirstomos į:
- sočiąsias (anglies grandinėje tarp anglies atomų yra tik viengubieji ryšiai);
- nesočiąsias (anglies grandinėje tarp anglies atomų yra ne tik viengubųjų, bet ir dvigubųjų arba trigubųjų ryšių);
- aromatines (įprastą anglies grandinę atstoja aromatinis žiedas).
Monokarboksirūgštys, turinčios ilgą C atomų grandinę ir įeinančios į riebalų sudėtį, vadinamos riebalų rūgštimis.
Nomenklatūra
Pagal IUPAC nomenklatūrą karboksirūgščių pavadinimai sudaromi suskaičiuojant ilgiausios anglies grandinės atomus (įskaitant ir karboksigrupės anglies atomą), prie C atomų skaičių atitinkančio angliavandenilio pavadinimo pridėjus žodį “rūgštis“, pvz. etano rūgštis. Labai dažnai naudojami trivialieji pavadinimai, kurie rodo rūgšties kilmę. Pagrindinių rūgščių pavadinimai pateikti lentelėje.
6.1. lentelė. Karboksirūgščių pavadinimai
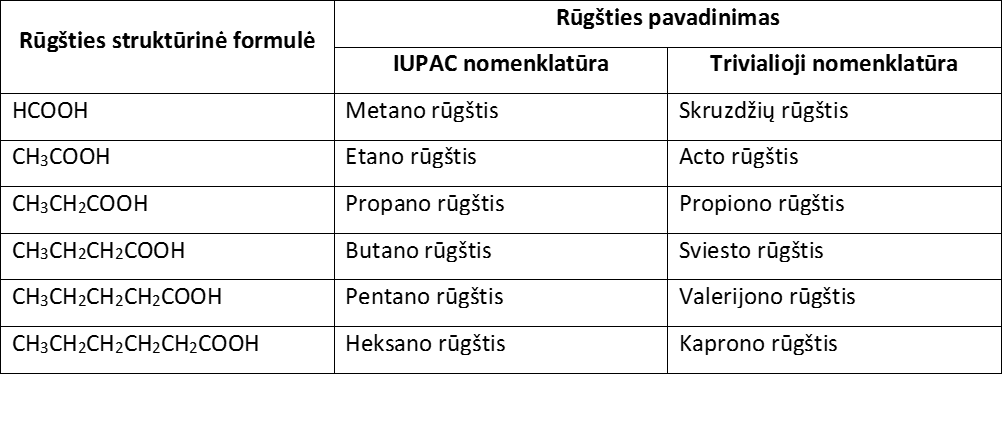
Numeruojant C atomų grandinę, pirmasis anglies atomas visuomet yra karboksigrupės C atomas.
Izomerija
Karboksirūgštims būdinga anglies grandinės bei tarpklasinė izomerija.
1. Anglies grandinės izomerija (butano rūgštis C4H8O2):

2. Tarpklasinė izomerija. Karboksirūgščių ir esterių yra ta pati bendroji molekulinė formulė. Todėl, pvz. etano rūgštis ir metilmetanoatas yra tarpusavyje izomerai.

Paplitimas gamtoje
Karboksirūgščių ir jų druskų yra augaluose ir gyvūnų bei žmonių organizmuose. Skruzdžių rūgšties turi skruzdėlės, yra eglių spygliuose. Įsidilginimas – skruzdžių rūgšties dirginantis poveikis. Pentano rūgšties aptinkama valerijono šaknyse. Pieno rūgštis (2 – hidroksipropano rūgštis) susidaro vykstant pienarūgščiam rūgimui. Jos yra raugintuose kopūstuose. Jeigu po fiziškai įtempto darbo ar intensyviai sportavusiam žmogui skauda raumenis, tai vadinasi juose susikaupė pieno rūgštis. Karboksirūgščių yra įvairiuose vaisiuose, todėl dažnai tokioms rūgštims suteikiami atitinkamų vaisių pavadinimai, pvz.: citrinų, vyno, obuolių ir kt. rūgštys.
Gavimas
Laboratorijoje karboksirūgštys gaunamos kaitinant karboksirūgščių druskas su stipria rūgštimi.
2CH3COONa + H2SO4 → Na2SO4 + 2CH3COOH
Pramonėje karboksirūgštys gali būti gaunamos:
a) oksiduojant angliavandenilius:
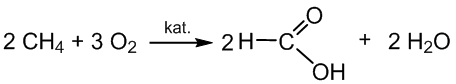
metano rūgštis
b) oksiduojant alkoholius:
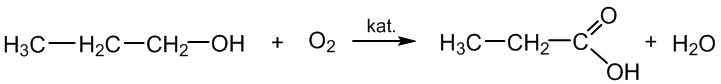
1 – propanolis propano rūgštis
c) oksiduojant aldehidus (žr. 6.4. skyrių);
d) kiti specialūs gavimo būdai:
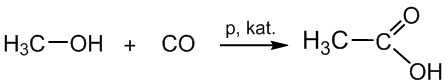
metanolis etano rūgštis
Fizikinės savybės
Pirmieji karboksirūgščių homologinės eilės nariai yra aštraus specifinio kvapo, gerai tirpstantys vandenyje skysčiai. Jei anglies atomų rūgšties molekulėje yra daugiau nei 10, tai karboksirūgštys yra kietos būsenos. Jos - netirpios vandenyje, bekvapės medžiagos. Didėjant karboksirūgščių molinei masei, rūgščių tirpumas vandenyje mažėja, o virimo temperatūra didėja.
Tarp karboksirūgščių ir vandens molekulių susidaro vandeniliniai ryšiai (žr. 2.4. skyrių), todėl jų virimo ir lydymosi temperatūros yra didesnės už atitinkamų angliavandenilių ir net alkoholių. Etano rūgšties lydymosi temperatūra yra +16,8 °C, todėl gryna etano rūgštis kartais vadinama „ledine acto rūgštimi“.
Cheminės savybės
Karboksirūgštys tirpdamos vandenyje jonizuojasi:
![]()
Kadangi karboksirūgštys yra silpnos rūgštys, tai jų jonizacija yra grįžtamasis procesas.
1. Reaguoja su metalais:
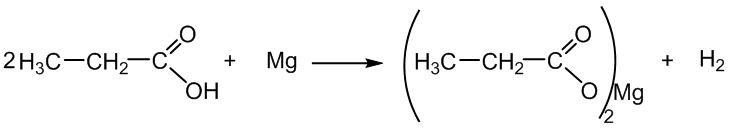
propano rūgštis magnio propanoatas
2. Reaguoja su metalų oksidais:
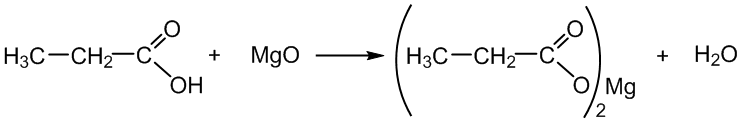
propano rūgštis magnio propanoatas
3. Reaguoja su bazėmis:
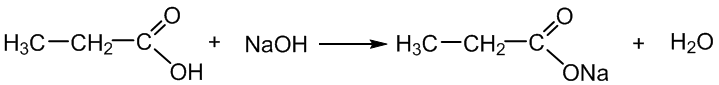
propano rūgštis natrio propanoatas
4. Reaguoja su silpnesniųjų ir lakiųjų rūgščių (žr. 5.1. skyrių) druskomis:
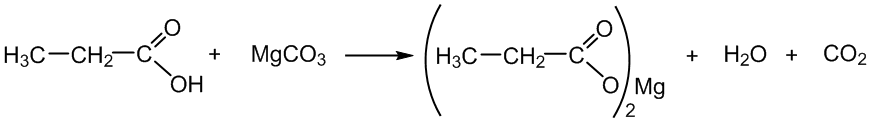
propano rūgštis magnio propanoatas
5. Reaguoja su alkoholiais (esterinimo reakcija):
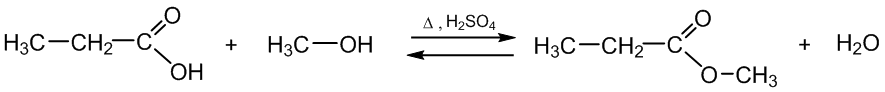
propano rūgštis metanolis metilpropanoatas
6. Kaitinant su fosforo (V) oksidu, susidaro rūgščių anhidridai:
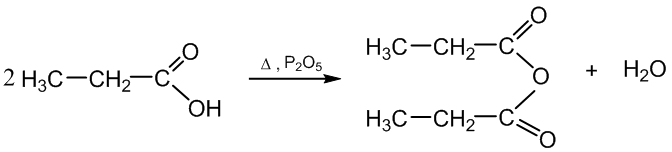
propano rūgštis propano rūgšties anhidridas
7. Metano rūgštis oksiduojasi (sidabrinio veidrodžio reakcija):
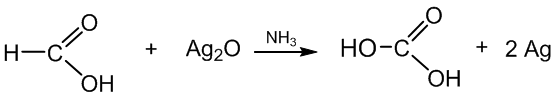
metano rūgštis anglies rūgštis
8. Karboksirūgštys reaguoja su halogenais:
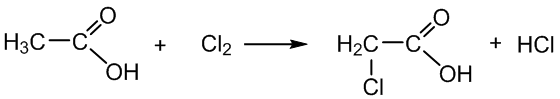
etano rūgštis chloretano rūgštis
Panaudojimas
Skruzdžių (metano) rūgštis yra stiprus reduktorius. 1,3 % metano rūgštis etanolyje naudojamas medicinoje, o skruzdžių rūgšties esteriai – kaip tirpikliai ir kvapiosioms medžiagoms gauti.
Iš visų rūgščių plačiausiai naudojama etano (acto) rūgštis. 80 % koncentracijos acto rūgštis vadinama acto esencija. 6–10 % acto rūgšties tirpalas naudojamas maisto pramonėje kaip konservantas. Daug etano rūgšties sunaudojama kitų junginių (etilacetato, monochloracto rūgšties, aspirino ir kt.) sintezei.
6.7. Aminai
Aminai yra svarbi azoto turinčių organinių junginių klasė. Tai – amoniako dariniai, kurių molekulėse vienas ar keli vandenilio atomai pakeisti angliavandenilių pakaitais. Aminuose yra aminogrupė –NH2, sujungta su anglies atomų grandine. Priklausomai nuo to, kelios angliavandenilio grupės prijungtos prie azoto atomo, aminai skirstomi į pirminius R – NH2, antrinius R2NH ir tretinius R3N:
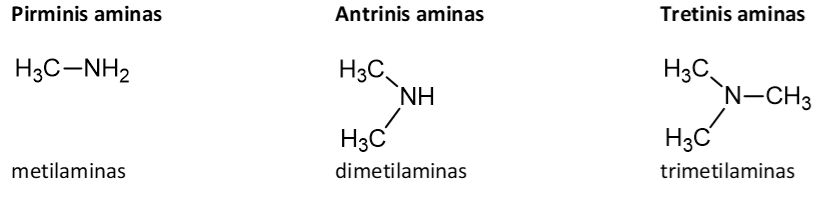
Jeigu pakaitas yra aromatinis ciklas – tai tokie aminai vadinami arilaminais.
![]()
fenilaminas (anilinas)
Nomenklatūra
Pagal IUPAC nomenklatūrą pirminių aminų pavadinimai sudaromi prie angliavandenilio, turinčio prijungtą aminogrupę, pavadinimo šaknies pridedant žodį aminas:
![]()
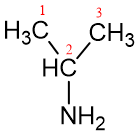
metanaminas 2-propanaminas
Rašant pavadinimus antriniams ir tretiniams aminams, prie azoto atomo esantis pakaitas su ilgiausia anglies atomų grandine laikomas pagrindiniu, o prieš jį abėcėlės tvarka surašomi kiti pakaitai. Jeigu aminas antrinis, tai prieš pakaitą rašome N-, o jeigu tretinis aminas, prieš pakaitus rašome N,N-. Pvz.:
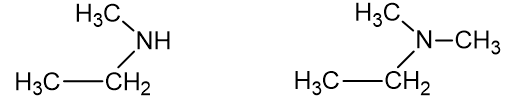
N-metiletanaminas N,N-dimetiletanaminas
(Etilmetilaminas) (dimetiletilaminas)
Aminams pavadinti dažnai taikomas paprastesnis būdas: išvardinami visi pakaitai ir gale parašomas žodis „aminas“. (pavadinimai parašyti raudona spalva). Šį būdą toliau naudosime vadinant aminus.
Izomerija
Aminams būdinga anglies atomų grandinės, funkcinės grupės padėties ir pakaitų padėties izomerija. Pirminiai, antriniai ir tretiniai aminai tarpusavyje yra izomerai:
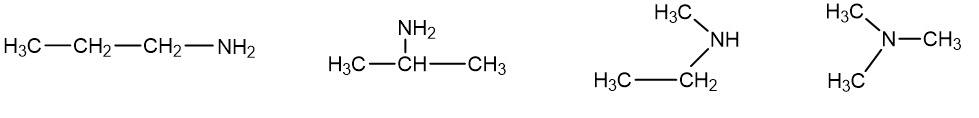
propilaminas izopropilaminas etilmetilaminas trimetilaminas
Paplitimas gamtoje
Aminai – vieni iš labiausiai paplitusių medžiagų gamtoje. Trimetilamino yra žuvų taukuose. Aminams būdingą aštrų kvapą galima pajusti žuvų parduotuvėje (kuo žuvis nešviežesnė, tuo stipresnis juntamas aštrus, specifinis aminų kvapas), pvz., yrančios silkės kvapą lemia trimetilamino kvapas. Aminogrupė yra vaistuose, dažuose, plastikuose ir kt. medžiagose.
Gavimas
Pirminiai aminai gaunami halogenalkanus veikiant amoniaku:
![]()
brommetanas metanaminas
(metilaminas)
![]()
brometanas etanaminas
(etilaminas)
Antriniai aminai gaunami halogenalkanus veikiant pirminiais aminais:
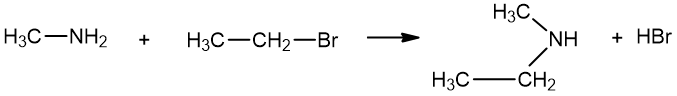
metanaminas brometanas N-metiletanaminas
(etilmetilaminas)
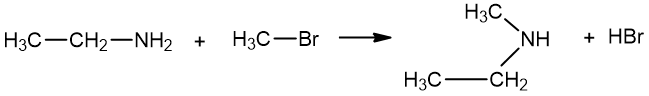
etanaminas brommetanas N-metiletanaminas
(etilmetilaminas)
Tretiniai aminai gaunami halogenalkanus veikiant antriniais aminais:
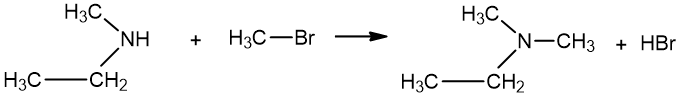
N-metiletanaminas brommetanas N,N-dimetiletanaminas
(etilmetilaminas) (dimetiletilaminas)
Anilinas gaunamas redukuojant nitrobenzeną alavu praskiestoje druskos rūgštyje:
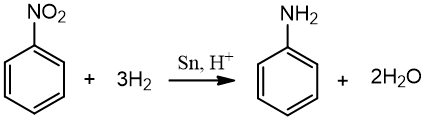
Nitrobenzenas fenilaminas
(anilinas)
Fizikinės savybės
Mažesnės molinės masės alifatiniai aminai (metilaminas, etilaminas, dimetilaminas ir trimetilaminas) yra dujos, didesnės – skysčiai arba kietosios medžiagos. Dujinės būsenos aminai turi aštrų specifinį kvapą. Pirminiai ir antriniai aminai gali sudaryti vandenilinius ryšius tarpusavyje arba su vandens molekulėmis:
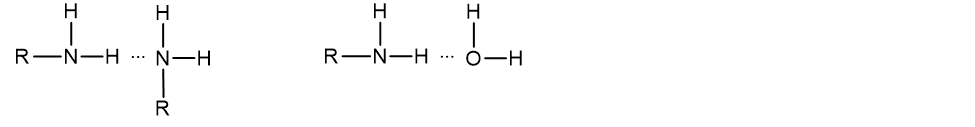
Dėl to šių aminų virimo temperatūros aukštesnės, nei panašios molinės masės alkanų, pvz. propanas verda -42,1°C temperatūroje, o etilaminas verda +16,6°C temperatūroje. Dėl to kad pirminiai ir antriniai aminai sudaro vandenilinius ryšius su vandens molekulėmis, jie gerai tirpsta vandenyje, o tretiniai aminai – silpnai. Didėjant aminuose angliavandenilio pakaito santykinei molekulinei masei, aminų tirpumas vandenyje mažėja.
Aromatinis aminas – anilinas – bespalvis, aliejaus pavidalo, savito kvapo skystis. Gerai tirpsta etanolyje, eteryje, benzene, blogai tirpsta vandenyje, užšąla -5,96°C, verda 184,4°C temperatūroje.
Cheminės savybės
Aminai savo sandara panašūs į amoniaką – jie pasižymi bazinėmis savybėmis. Vandeniniame tirpale vyksta tokia pusiausvyroji reakcija:
CH3CH2NH2 + H2O ↔ CH3CH2NH3+ + HO-
Susidaręs hidroksido jonas lemia bazines amino tirpalų savybes. Lakmusas amino tirpale nusidažo mėlynai, o fenolftaleinas – violetine spalva.
Bazinės aminų savybės priklauso nuo azoto atome esančios laisvosios elektronų poros, susidariusio teigiamojo jono patvarumo bei amino tirpumo.
Pagal bazinių savybių stiprumą alkilaminų, anilino ir amoniako eilė yra tokia:
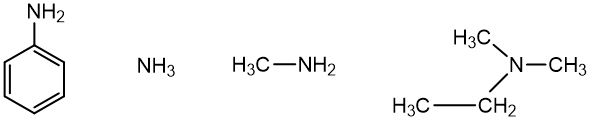
Anilinas amoniakas metilaminas N-metiletanaminas
Aromatinis aminas pirminis aminas antrinis aminas
![]()
BAZINĖS SAVYBĖS STIPRĖJA
1. Aminai reaguoja su rūgštimis, susidaro amonio druskos:
H3C-NH2 + HCl → [CH3-NH3]+Cl-
Metilaminas metilamonio chloridas
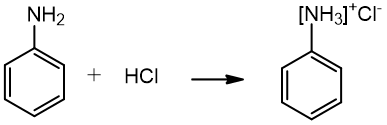
Anilinas fenilamonio chloridas
2. Anilinas dalyvauja pavadavimo reakcijose, pvz. reaguoja su halogenais, azoto (nitrato) rūgštimi:
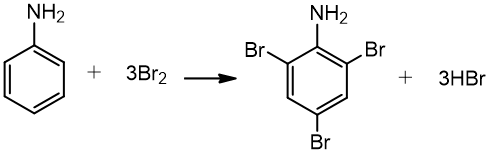
Anilinas 2,4,6 - tribromanilinas
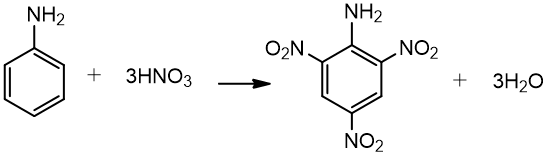
Anilinas 2,4,6 - trinitroanilinas
Panaudojimas
Aminai yra dažiklių, pesticidų, polimerų, korozijos inhibitorių, antioksidantų ir kt. tarpiniai produktai. Oksiduojant aniliną galima gauti įvairius spalvotus junginius. Anilinas taip pat naudojamas vaistų, pesticidų bei sprogstamųjų medžiagų gamyboje.
6.7.1. Aminorūgštys
Aminorūgštimis vadinamos karboksirūgštys, turinčios vieną arba dvi aminogrupes. Paprasčiausia aminorūgštis yra aminoetano rūgštis:
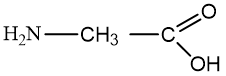
Nomenklatūra
Pagal IUPAC nomenklatūrą vadinant aminorūgštis, numeruoti anglies atomų grandinę pradedame nuo karboksigrupės anglies atomo:

3-aminopropano rūgštis
Dažnai aminorūgštys vadinamos pagal aminogrupės padėtį karboksigrupės atžvilgiu. Aminogrupės padėtis nurodoma ne skaičiumi, bet graikų abėcėlės raide: α, β, γ ir t.t. Numeracija pradedama nuo to anglies atomo, kuris yra greta funkcinės karboksigrupės, pvz.:

β -aminopropano rūgštis
Baltymai ir peptidai yra α- aminorūgščių polimerai. Iš viso baltymuose randama 20 pagrindinių aminorūgščių (6.2 lentelė), kurių beveik visų bendroji formulė:
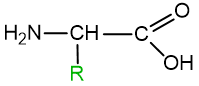
čia: R – pakaitas (radikalas)
6.2 lentelė. Pagrindinės baltymų α- aminorūgštys
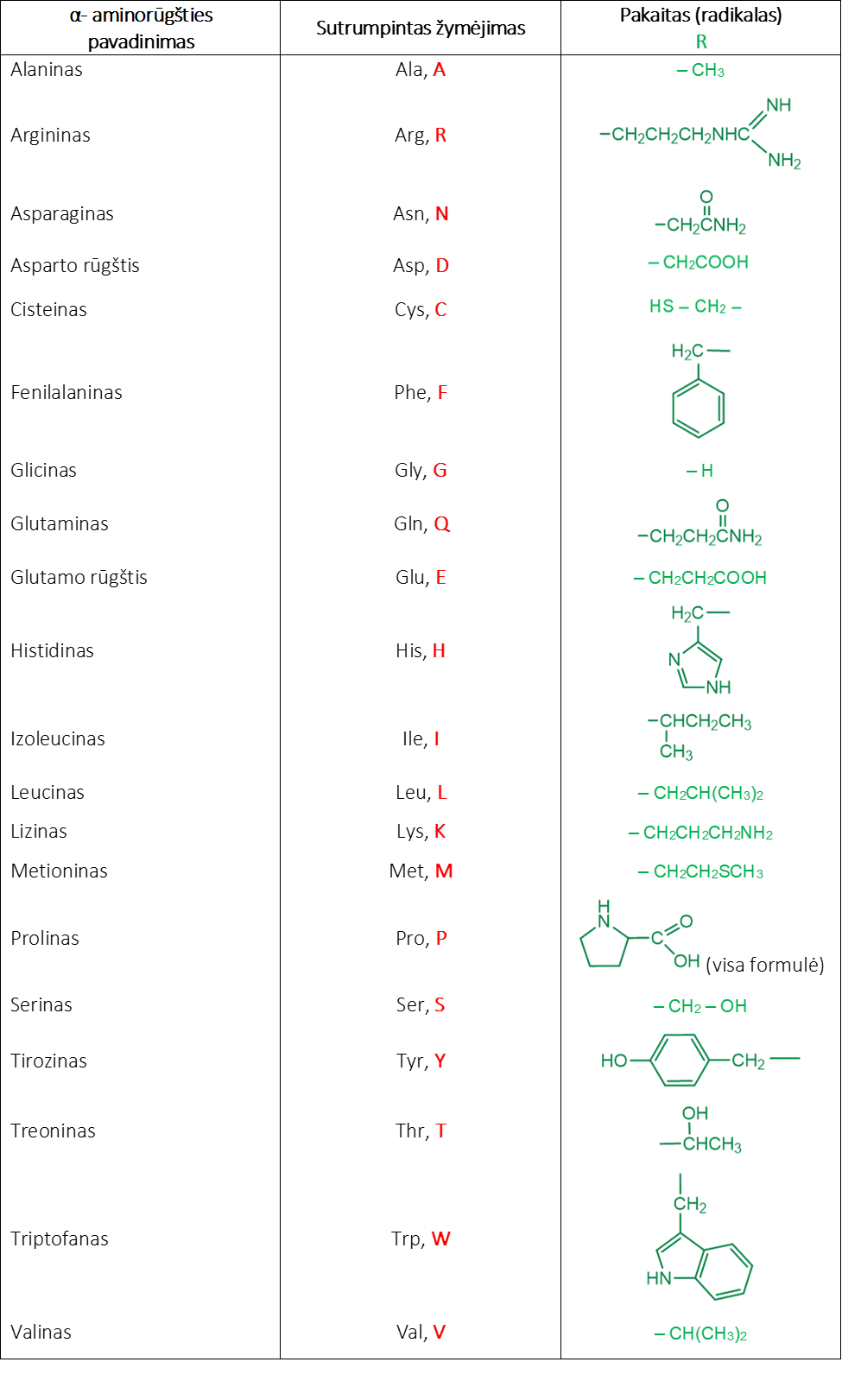
Izomerija
Aminorūgštims būdinga anglies atomų grandinės izomerija ir amino- bei karboksigrupių tarpusavio išsidėstymo izomerija, pvz. aminobutano rūgšties izomerai:
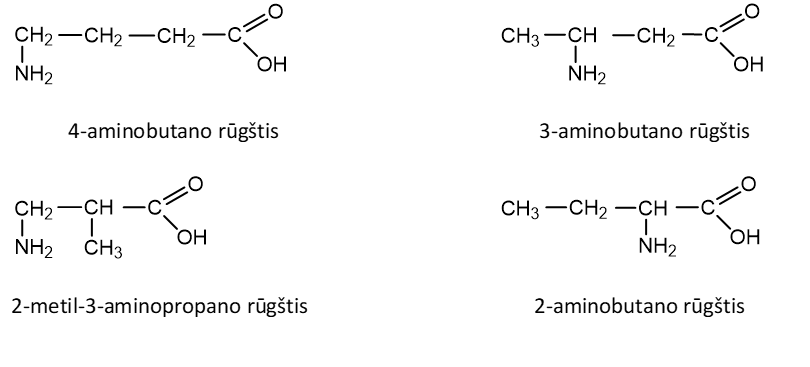
Paplitimas gamtoje
Iš α- aminorūgščių yra sudaryti baltymai.
Gavimas
Aminorūgštys gaunamos:
1. Hidrolizuojant baltymus – hidrolizė vyksta trūkstant peptidiniam ryšiui :
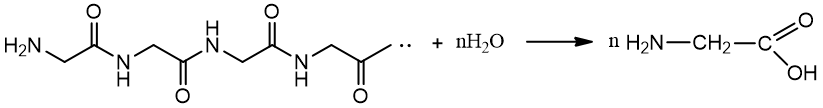
2. Iš halogenkarboksirūgščių:
Cl-CH2COOH + 2NH3 → NH2-CH2COOH + NH4Cl
Chloretano rūgštis aminoetano rūgštis
Fizikinės savybės
Aminorūgštys yra bespalvės, kristalinės, gerai tirpstančios vandenyje, medžiagos.
Cheminės savybės
Aminorūgštyse yra bazines savybes lemianti aminogrupė (-NH2) ir rūgštines savybes lemianti karboksigrupė (-COOH). Abi šios grupės gali jonizuotis. Karboksigrupė nesunkiai atiduoda protoną ir virsta anijonu:
![]()
Aminogrupė, atvirkščiai, linkusi prisijungti protoną ir virsti katijonu:
![]()
1. Aminorūgštys yra amfoteriniai junginiai, turintys ir rūgštinių, ir bazinių savybių:
a) reaguoja su rūgštimis:
NH2 – CH2 – COOH + HCl → [NH3 – CH2 – COOH]+Cl-
Aminoetano rūgštis aminoetano rūgšties hidrochloridas
b) reaguoja su šarmais:
NH2 – CH2 – COOH + NaOH → NH2 – CH2 – COONa + H2O
Aminoetano rūgštis natrioaminoetanoatas
2. Aminorūgštys reaguoja tarpusavyje, sudarydamos di-, tri-,....polipeptidus:
dipeptidas
Visos kitos aminorūgščių savybės tokios pačios kaip karboksirūgščių ir aminų (žr. 6.5 ir 6.6 sk.)
Panaudojimas
Aminorūgštys būtinos baltymų sintezei organizmuose. Pradines aminorūgštis gyvūnai ir žmonės gauna su baltyminiu maistu, kuris žarnyne suskaidomas į atskiras aminorūgštis, iš kurių vėliau sintetinami reikalingi baltymai. Kai kurios aminorūgštys naudojamos medicinoje, dedamos kaip priedai į gyvūnų pašarą.