Teorinė medžiaga su pavyzdžiais
6.2. Angliavandeniliai
6.2.2.1. Alkenai
Angliavandeniliai, kurių bendroji formulė CnH2n ir kurių molekulėse tarp anglies atomų yra vienas dvigubasis ryšys, vadinami alkenais.
Nomenklatūra
Bendrojoje alkenų formulėje indeksas n – sveikasis skaičius, rodantis anglies atomų skaičių, nuo kurio priklauso pavadinimas. Alkenų pavadinimai sudaromi su priesaga –en – ir galūne –as, pvz. C2H4 – etenas, C3H6 – propenas ir kt. Pagrindinės nomenklatūros taisyklės pateiktos 6.1. skyriuje. Skirtingai nuo alkanų pagrindinė C atomų grandinė (nebūtinai ilgiausia) turi būti su dvigubuoju ryšiu. Ji numeruojama nuo tos pusės, kur arčiau yra dvigubasis ryšys. Pvz.:
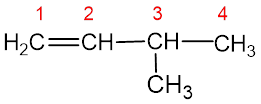
3 - metil - 1 - butenas
Izomerija
Alkenams būdingos šios izomerijos rūšys:
1. Anglies grandinės izomerija (penteno C5H10):

2. Dvigubojo ryšio padėties izomerija (penteno C5H10):
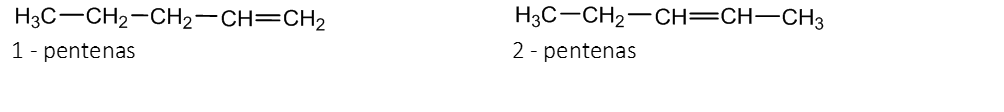
3. Geometrinė izomerija (cis- ir trans-). Kai anglies atomai sudaro viengubąjį ryšį, jie sukasi aplink ryšio ašį, bet ryšys nenutrūksta. Kai grandinėje yra dvigubasis ryšys, sukimasis neįmanomas. Jei medžiagos molekulėje pakaitai išsidėstę vienoje dvigubojo ryšio pusėje, tai – cis-izomeras, jei skirtingose pusėse – trans-izomeras.
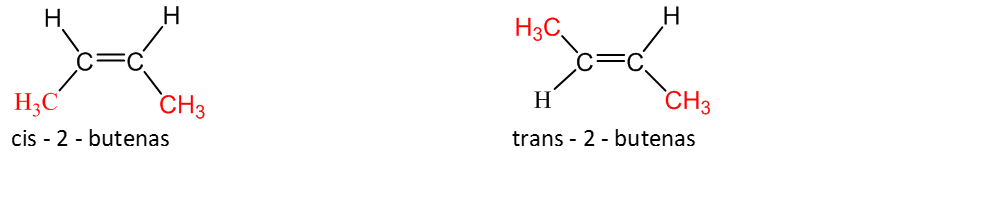
4. Tarpklasinė izomerija. Alkenų ir
cikloalkanų yra ta pati bendroji molekulinė formulė. Todėl, pvz. propenas ir
ciklopropanas yra izomerai.
Paplitimas gamtoje
Alkenai gamtoje mažai paplitę. Jų yra vabzdžių (bičių, musių) feromonuose. Žemesniųjų alkenų nedideliais kiekiais būna naftos dujose, aukštesniųjų – kai kurių rūšių naftoje.
Gavimas
Pramonėje etenas gaunamas iš gamtinių dujų, naftos pirolizės bei krekingo metu.
Laboratorijoje alkenai gali būti gaunami:
1. Dehidrinant alkanus. Pramonėje ir laboratorijoje alkenai gaunami dehidrinant sočiuosius angliavandenilius. Reakcija atliekama aukštoje temperatūroje, dalyvaujant katalizatoriui – metalų oksidams.
![]()
propanas propenas
2. Hidrinant alkinus:
![]()
propinas propenas
3. Dihalogenalkanus, kuriuose halogeno atomai yra prie gretimų C atomų, veikiant Mg arba Zn:
![]()
1 ,2 - dibrompropanas propenas
4. Halogenalkanus veikiant alkoholiniu kalio šarmo tirpalu:
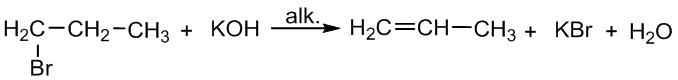
1 - brompropanas propenas
5. Dehidratuojant alkoholius, kaip katalizatorių naudojant koncentruotą sieros rūgštį:
![]()
etanolis etenas
Fizikinės savybės
Pirmieji trys alkenų homologinės eilės nariai turintys (C2 – C4) – dujos, (C5 – C18) – skysčiai, (C19 ir >) – kietos medžiagos. Alkenai netirpsta vandenyje, bet labai gerai tirpsta nepoliniuose tirpikliuose (benzene, trichlormetane, žibale). Jie yra lengvesni už vandenį, virimo temperatūra didėja, didėjant anglies atomų skaičiui molekulėje. Alkenams būdingas specifinis aštrus kvapas.
Cheminės savybės
Alkenams būdingos prisijungimo, oksidacijos ir polimerizacijos reakcijos.
1. Prisijungimo reakcijos.
a) reaguoja su vandeniliu (hidrinimas):
![]()
propenas propanas
b) reaguoja su halogenais (halogeninimas):
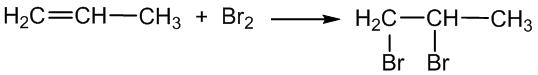
propenas 1, 2 - dibrompropanas
Ši reakcija yra alkenų atpažinimo reakcija – alkenai blukina bromo vandenį.
c) reaguoja su vandenilio halogenidais (Markovnikovo taisyklė: vandenilio atomas prisijungia prie labiau hidrinto anglies atomo, o halogeno atomas – prie kito anglies atomo. Prisijungimas vyksta prie anglies atomų, tarp kurių yra dvigubasis ryšys):
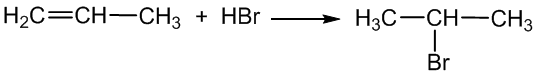
propenas 2 - brompropanas
d) reaguoja su vandeniu (hidratacijos reakcija):
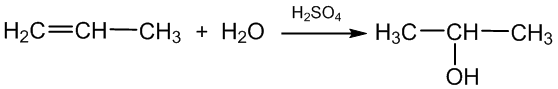
propenas 2 - propanolis
2. Oksidacijos reakcijos.
a) blukina kalio permanganato tirpalą – kokybinė alkenų atpažinimo reakcija:
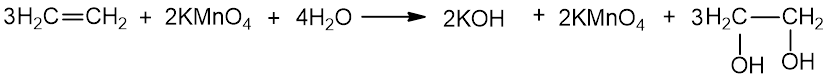
b) aukštoje temperatūroje alkenai dega iki CO2 ir H2O išskirdami didelį kiekį šilumos:
2C3H6 + 9O2 → 6CO2 + 6H2O
3. Polimerizacijos reakcijos.
Vienodų molekulių susijungimas į didesnes vadinamas polimerizacija. Monomeras – pradinis junginys (mažos molekulinės masės), iš kurio sintetinamas polimeras (stambiamolekulis junginys). Polimerizacijos laipsnis n – monomero grandžių skaičius polimero makromolekulėje.
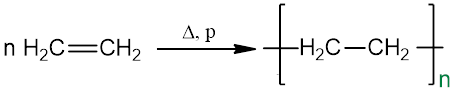
etenas polietenas
(monomeras) (polimeras)
Panaudojimas
Dujinis etenas pagreitina vaisių ir daržovių nokimą, yra žaliava aukšto oktaninio skaičiaus kurui, plastikui, etanoliui, etano oksidui, halogenalkanams gaminti.
Ypač plačiai naudojami alkenų polimerizacijos reakcijų produktai.
