Teorinė medžiaga su pavyzdžiais
6.6. Karboksirūgštys
Karboksirūgštys – organiniai junginiai, kurie turi vieną ar kelias karboksigrupes:
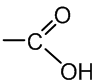
Bendroji karboksirūgščių formulė yra CnH2nO2 arba R–COOH, kur R – pakaitas.
Karboksirūgštys pagal karboksigrupių skaičių molekulėje skirstomos į:
- monokarbosirūgštis (gr. monos – vienas);
- dikarboksirūgštis (gr. di – du);
- polikarboksirūgštis (gr. polys – didelis, gausus).
Karboksirūgštys pagal pagrindinės anglies grandinės sudėtį skirstomos į:
- sočiąsias (anglies grandinėje tarp anglies atomų yra tik viengubieji ryšiai);
- nesočiąsias (anglies grandinėje tarp anglies atomų yra ne tik viengubųjų, bet ir dvigubųjų arba trigubųjų ryšių);
- aromatines (įprastą anglies grandinę atstoja aromatinis žiedas).
Monokarboksirūgštys, turinčios ilgą C atomų grandinę ir įeinančios į riebalų sudėtį, vadinamos riebalų rūgštimis.
Nomenklatūra
Pagal IUPAC nomenklatūrą karboksirūgščių pavadinimai sudaromi suskaičiuojant ilgiausios anglies grandinės atomus (įskaitant ir karboksigrupės anglies atomą), prie C atomų skaičių atitinkančio angliavandenilio pavadinimo pridėjus žodį “rūgštis“, pvz. etano rūgštis. Labai dažnai naudojami trivialieji pavadinimai, kurie rodo rūgšties kilmę. Pagrindinių rūgščių pavadinimai pateikti lentelėje.
6.1. lentelė. Karboksirūgščių pavadinimai
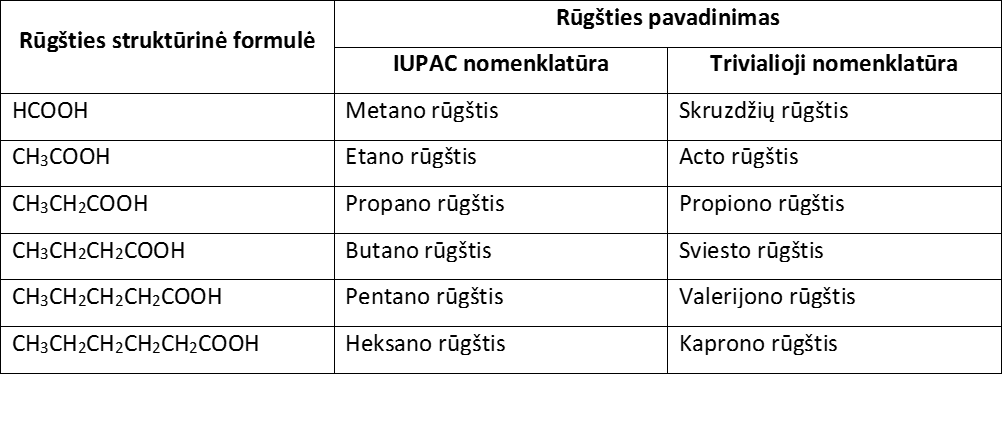
Numeruojant C atomų grandinę, pirmasis anglies atomas visuomet yra karboksigrupės C atomas.
Izomerija
Karboksirūgštims būdinga anglies grandinės bei tarpklasinė izomerija.
1. Anglies grandinės izomerija (butano rūgštis C4H8O2):

2. Tarpklasinė izomerija. Karboksirūgščių ir esterių yra ta pati bendroji molekulinė formulė. Todėl, pvz. etano rūgštis ir metilmetanoatas yra tarpusavyje izomerai.

Paplitimas gamtoje
Karboksirūgščių ir jų druskų yra augaluose ir gyvūnų bei žmonių organizmuose. Skruzdžių rūgšties turi skruzdėlės, yra eglių spygliuose. Įsidilginimas – skruzdžių rūgšties dirginantis poveikis. Pentano rūgšties aptinkama valerijono šaknyse. Pieno rūgštis (2 – hidroksipropano rūgštis) susidaro vykstant pienarūgščiam rūgimui. Jos yra raugintuose kopūstuose. Jeigu po fiziškai įtempto darbo ar intensyviai sportavusiam žmogui skauda raumenis, tai vadinasi juose susikaupė pieno rūgštis. Karboksirūgščių yra įvairiuose vaisiuose, todėl dažnai tokioms rūgštims suteikiami atitinkamų vaisių pavadinimai, pvz.: citrinų, vyno, obuolių ir kt. rūgštys.
Gavimas
Laboratorijoje karboksirūgštys gaunamos kaitinant karboksirūgščių druskas su stipria rūgštimi.
2CH3COONa + H2SO4 → Na2SO4 + 2CH3COOH
Pramonėje karboksirūgštys gali būti gaunamos:
a) oksiduojant angliavandenilius:
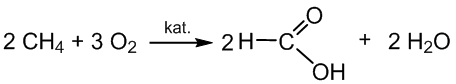
metano rūgštis
b) oksiduojant alkoholius:
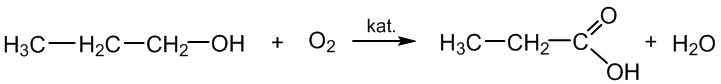
1 – propanolis propano rūgštis
c) oksiduojant aldehidus (žr. 6.4. skyrių);
d) kiti specialūs gavimo būdai:
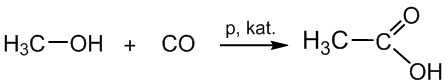
metanolis etano rūgštis
Fizikinės savybės
Pirmieji karboksirūgščių homologinės eilės nariai yra aštraus specifinio kvapo, gerai tirpstantys vandenyje skysčiai. Jei anglies atomų rūgšties molekulėje yra daugiau nei 10, tai karboksirūgštys yra kietos būsenos. Jos - netirpios vandenyje, bekvapės medžiagos. Didėjant karboksirūgščių molinei masei, rūgščių tirpumas vandenyje mažėja, o virimo temperatūra didėja.
Tarp karboksirūgščių ir vandens molekulių susidaro vandeniliniai ryšiai (žr. 2.4. skyrių), todėl jų virimo ir lydymosi temperatūros yra didesnės už atitinkamų angliavandenilių ir net alkoholių. Etano rūgšties lydymosi temperatūra yra +16,8 °C, todėl gryna etano rūgštis kartais vadinama „ledine acto rūgštimi“.
Cheminės savybės
Karboksirūgštys tirpdamos vandenyje jonizuojasi:
![]()
Kadangi karboksirūgštys yra silpnos rūgštys, tai jų jonizacija yra grįžtamasis procesas.
1. Reaguoja su metalais:
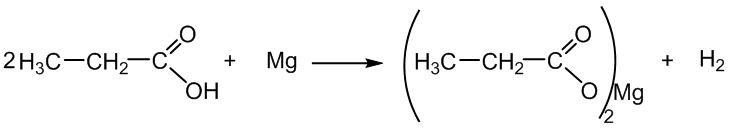
propano rūgštis magnio propanoatas
2. Reaguoja su metalų oksidais:
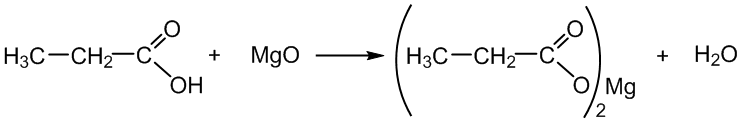
propano rūgštis magnio propanoatas
3. Reaguoja su bazėmis:
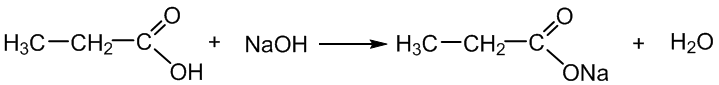
propano rūgštis natrio propanoatas
4. Reaguoja su silpnesniųjų ir lakiųjų rūgščių (žr. 5.1. skyrių) druskomis:
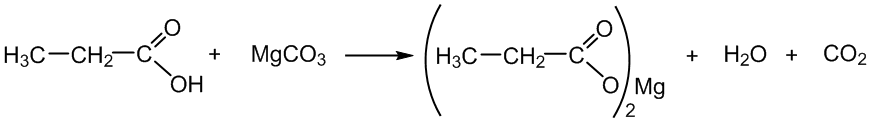
propano rūgštis magnio propanoatas
5. Reaguoja su alkoholiais (esterinimo reakcija):
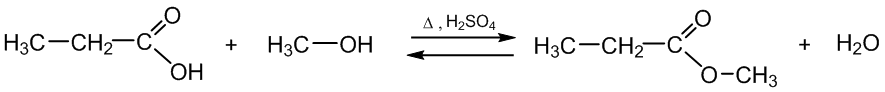
propano rūgštis metanolis metilpropanoatas
6. Kaitinant su fosforo (V) oksidu, susidaro rūgščių anhidridai:
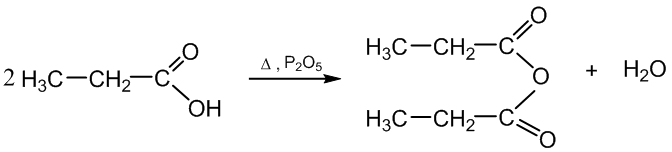
propano rūgštis propano rūgšties anhidridas
7. Metano rūgštis oksiduojasi (sidabrinio veidrodžio reakcija):
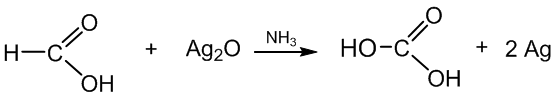
metano rūgštis anglies rūgštis
8. Karboksirūgštys reaguoja su halogenais:
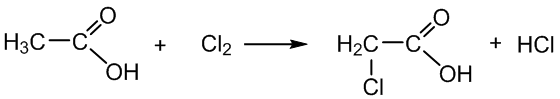
etano rūgštis chloretano rūgštis
Panaudojimas
Skruzdžių (metano) rūgštis yra stiprus reduktorius. 1,3 % metano rūgštis etanolyje naudojamas medicinoje, o skruzdžių rūgšties esteriai – kaip tirpikliai ir kvapiosioms medžiagoms gauti.
Iš visų rūgščių plačiausiai naudojama etano (acto) rūgštis. 80 % koncentracijos acto rūgštis vadinama acto esencija. 6–10 % acto rūgšties tirpalas naudojamas maisto pramonėje kaip konservantas. Daug etano rūgšties sunaudojama kitų junginių (etilacetato, monochloracto rūgšties, aspirino ir kt.) sintezei.
