Teorinė medžiaga su pavyzdžiais
6.3. Alkoholiai ir fenoliai
6.3.1. Vienhidroksiliai alkoholiai
Vienhidroksiliai alkoholiai – angliavandenilių junginiai, kurių molekulėse vienas vandenilio atomas pakeistas hidroksigrupe (–OH). Jų bendroji formulė CnH2n+1OH.
Pagal funkcinės hidroksigrupės padėtį alkholiai gali būti pirminiai, antriniai arba tretiniai.
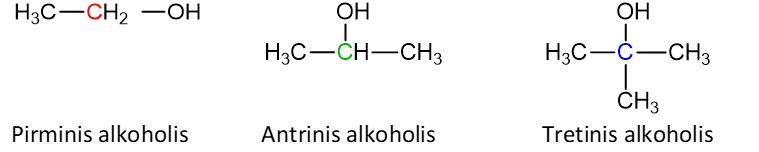
Pirminiu alkoholiu vadiname tokį alkoholį, kuriame funkcinė grupė yra prisijungusi prie pirminio anglies atomo.
- Antriniu alkoholiu vadiname tokį alkoholį, kuriame funkcinė grupė yra prisijungusi prie antrinio anglies atomo.
- Tretiniu alkoholiu vadiname tokį alkoholį, kuriame funkcinė grupė yra prisijungusi prie tretinio anglies atomo.
- Kas tas pirminis, antrinis arba tretinis C atomas?
Atsakymas. Pagal tai, su keliais šalia esančiais anglies atomais yra susijungę anglies atomai, jie gali būti pirminiai, antriniai, tretiniai arba ketvirtiniai:
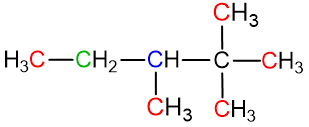
Raudona spalva parašytas C atomas yra pirminis;
Žalia – antrinis;
Mėlyna – tretinis;
Juoda – ketvirtinis.
Nomenklatūra
Bendrojoje alkoholių formulėje indeksas n – sveikasis skaičius, rodantis anglies atomų skaičių, nuo kurio priklauso pavadinimas. Alkoholių pavadinimai sudaromi su priesaga –ol – ir galūne –is, pvz. C2H5OH – etanolis, C3H7OH – propanolis ir kt. Pagrindinė C atomų grandinė (nebūtinai ilgiausia) turi būti su funkcine grupe. Ji numeruojama nuo tos pusės, kur arčiau yra funkcinė hidroksigrupė. Pvz.:
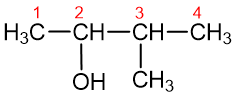
3 - metil - 2 - butanolis
Izomerija
Alkoholiams būdingos šios izomerijos rūšys:
1. Anglies grandinės izomerija:
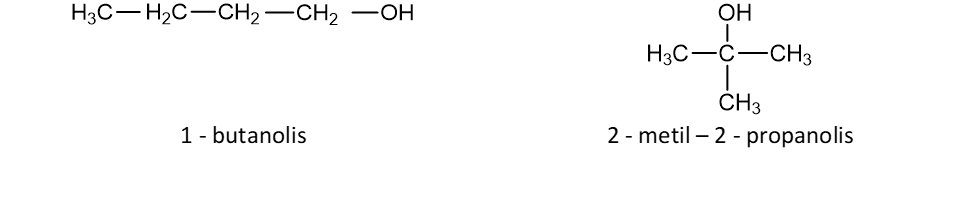
2. Funkcinės grupės izomerija (C3H8O):

3. Tarpklasinė izomerija. Alkoholių ir eterių yra ta pati bendroji molekulinė formulė. Todėl, pvz. etanolis ir dimetileteris yra tarpusavyje izomerai:

Paplitimas gamtoje
Etanolis – tai žinduolių ir žmonių organizmuose vykstančių reakcijų produktas. Alkoholio nevartojančio žmogaus organizme normali etanolio koncentracija kraujyje kinta nuo 0,001 iki 0,1 g/l (vadinasi, etanolis yra endogeninė, t. y. gaminama organizmo, medžiaga). Etanolio kiekis kraujyje matuojamas promilėmis ‰ (promilė – tūkstantoji dydžio dalis).
Gavimas
1. Laboratorijoje alkoholius galima gauti halogenintus angliavandenilius veikiant natrio, kalio ir kalcio hidroksidų vandeniniais tirpalais.
C2H5Cl + KOH → C2H5OH + KCl
chloretanas etanolis
2. Pramonėje metanolis gaunamas aukštoje temperatūroje ir slėgyje reaguojant tarpusavyje anglies monoksidui su vandeniliu, katalizatoriais naudojant Cu, ZnO:
CO + 2H2 → CH3OH
metanolis
3. Alkoholiai gaunami hidratuojant alkenus:
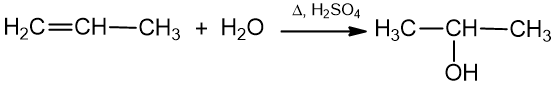
propenas 2 - propanolis
4. Etanolis gaunamas fermentacijos metu, beorėje erdvėje iš gliukozės:
C6H12O6→ 2C2H5OH + 2CO2
gliukozė etanolis
5. Alkoholiai susidaro redukuojant karbonilinius junginius (žr. 6.4. skyrių).
Fizikinės savybės
Vienhidroksiliai sotieji pirminiai alkoholiai su trumpa anglies atomų grandine – skysčiai, o aukštesnieji, t. y. didesnės santykinės molekulinės masės, pavyzdžiui, C12H25OH, – kietosios medžiagos. Pirmųjų homologinės eilės narių kvapas silpnas, butanolio, pentanolio ir heksanolio – stiprus, nemalonus. Didelės molinės masės alkoholiai – bekvapiai. Didėjant alkoholių santykinei molekulinei masei, didėja jų virimo temperatūra. Alkoholių virimo temperatūra daug aukštesnė negu panašios santykinės molekulinės masės atitinkamų angliavandenilių. Šį reiškinį galima paaiškinti vandenilinių ryšių (žr. 2.4. skyrių) susidarymu tarp alkoholio molekulių ir tarp alkoholio ir vandens molekulių:
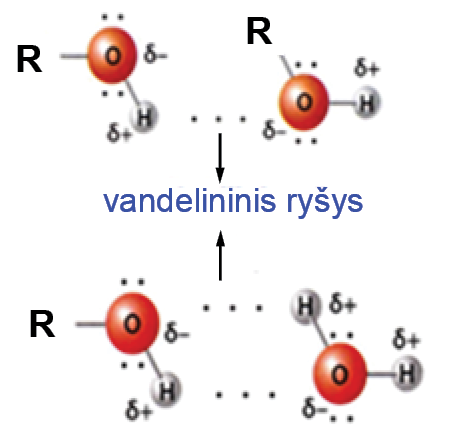
Alkoholiai turi polinę hidroksigrupę, kuri gali sudaryti vandenilinius ryšius su vandeniu arba su kitomis alkoholių molekulėmis. Vandeniliniai ryšiai tarp alkoholių ir vandens susidaro dėl deguonies atomo laisvųjų elektronų porų: šiais elektronais deguonis gali sudaryti silpnus vandenilinius ryšius su kitos molekulės (alkoholio arba vandens) dalinai teigiamais vandenilio atomais.
Vandeniliniai ryšiai taip pat lemia metanolio, etanolio ir propanolio neribotą tirpumą vandenyje. Kitų vienhidroksilių alkoholių tirpumas vandenyje ribotas. Tirpumas mažėja dėl didėjančios netirpios anglies grandinės dalies molekulėje.
Cheminės savybės
Alkoholiams nebūdingos nei rūgštinės, nei bazinės savybės, todėl indikatorių spalvos jie nekeičia (žr. 5.2.8. skyrių).
1. Alkoholiai reaguoja su aktyviais metalais (susidaro alkoholiatai), bet nereaguoja su šarmais:
![]()
etanolis kalio etanoliatas
2. Alkoholiai reaguoja su koncentruotais vandenilio halogenidais:
![]()
etanolis brometanas
3. Alkoholių dehidratavimas – vandens molekulės eliminavimas. Priklausomai nuo temperatūros, gali susidaryti alkenai arba eteriai:
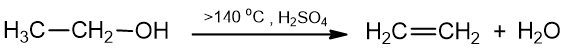
etanolis etenas
![]()
etanolis dimetileteris
4. Alkoholiai reaguoja su karboksirūgštimis ir sudaro esterius (žr. 6.6. skyrių).
5. Alkoholiai lengvai oksiduojasi. Pirminiai alkoholiai oksiduojasi iki adehidų, o antriniai – iki ketonų. Tretiniai alkoholiai nesioksiduoja (žr. 6.4. skyrių).
6. Alkoholiai ore dega melsva liepsna:
C2H5OH + 3O2 → 2CO2 + 3H2O
Panaudojimas. Poveikis žmogui
Etanolis vartojamas alkoholinių gėrimų gamyboje, medicinoje, parfumerijos pramonėje. Techninis etilo spiritas – sintetinio kaučiuko, dirbtinio šilko, organinio stiklo, plastmasių, lakų, dažų, fotografijos reikmenų gamybos žaliava. Kai kuriose šalyse etanolis yra degalai. Į benziną įterpus iki 15% etanolio, pagerėja degalų savybės, į aplinką patenka mažiau teršalų.
Etanolis naudojamas kaip tirpiklis.
Alkoholio vartojimas dideliais kiekiais yra pavojingas žmogaus organizmui. Medikai teigia, kad 4,5-5,0 g/l alkoholio dozė žmogaus kraujyje daugeliui yra mirtina. Ši dozė atitinka 300 ml 96 % koncentracijos alkoholio. Dažnai vartojantys alkoholį žmonės ilgainiui suserga alkoholizmu. Etanolis yra kepenų, širdies, nervų ir lytinių ligų priežastis.
Metanolis labai nuodingas junginys. Išgėręs jo tik 2 g, žmogus gali apakti, o nuo 40 g mirti. Pagal kvapą, skonį ir išvaizdą metanolis labai panašus į etanolį. Apsinuodijimo metanoliu priešnuodis – etanolis.
