Teorinė medžiaga
5.2. Tirpalai
Tirpalas – tai vienalytis skystasis arba kietasis medžiagų (tirpinio ir tirpiklio) mišinys.
Kietuosiuose tirpaluose vienos medžiagos atomai (molekulės) chaotiškai pasklinda tarp kitos kietosios medžiagos atomų (molekulių). Kietojo tirpalo pavyzdys – nerūdijantysis plienas, t. y. geležies lydinys, turintis 12–30 % Cr, ≤ 28 % Ni, ≤ 4,5 % Mo ir kitų priedų.
Jei tirpalą sudaro skystyje ištirpęs kitas skystis, nesikeičia ne tik tirpiklio, bet ir tirpinio agregatinė būsena, tai tirpikliu laikomas tas komponentas, kurio tirpale yra daugiau. Pavyzdžiui, jei 10 ml acetono (propanono) ištirpdoma 100 ml etanolio, tai tirpiklis yra etanolis. Tačiau jei tirpalas yra gaminamas iš dviejų skysčių, kurių vienas vanduo, tai vanduo visada laikomas tirpikliu, kad ir koks būtų jo kiekis. Pavyzdžiui, gaminant 65 % koncentracijos sieros rūgšties tirpalą, tirpiklio vandens jame bus 35 %.
Pagal ištirpusios medžiagos masę tirpalai yra koncentruotieji ir praskiesti.
Koncentruotasis tirpalas – tirpalas, kuriame daug ištirpusios medžiagos. Praskiestas tirpalas – mažos koncentracijos tirpalas.
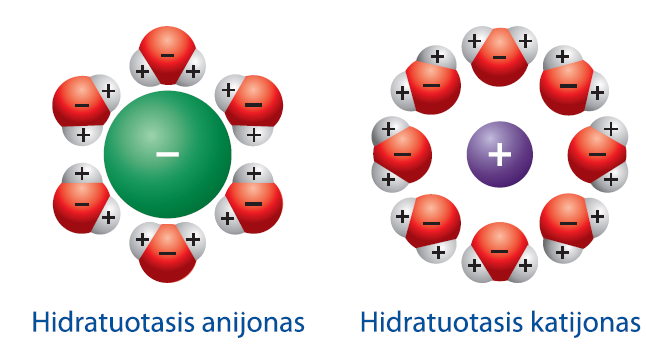
Praskiestuose tirpaluose jonai arba polinės molekulės prisijungia tam tikrą skaičių vandens molekulių ir tampa hidratuotosiomis (aq) dalelėmis. Hidratuoti junginiai vadinami hidratais, kurių bendroji formulė yra [M(H2O)x]z+:
Paruošė prof. A. Šulčius
