Teorinė medžiaga
| Impresso por: | Guest user |
| Data: | sábado, 30 de maio de 2026 às 12:44 |
Índice
- 5.1. Neorganinių junginių tipai
- 5.2. Tirpalai
- 5.2.1. Procentinė ir molinė tirpalų koncentracija
- 5.2.2. Elektrolitai ir neelektrolitai
- 5.2.3. Elektrolitų jonizacija ar disociacija
- 5.2.4. Rūgščių, hidroksidų ir druskų jonizacijos-disociacijos pavyzdžiai
- 5.2.5. Hidridų ir oksidų bazinės-rūgštinės savybės
- 5.2.6. Elektrolitų pH
- 5.2.7. pH uždavinių sprendimo pavyzdžiai
- 5.2.8. Indikatoriai ir neutralizavimas
- 5.2.9. Tirpalų tankio priklausomybė nuo koncentracijos
- 5.2.10. Įvairių medžiagų tirpumo priklausomybė nuo temperatūros
5.1. Neorganinių junginių tipai
Neorganiniai junginiai yra skirstomi į:
1) oksidus
2) hidroksidus
3) rūgštis
4) druskas
5.1.1. Oksidai
Oksidai − dviejų cheminių elementų, kurių vienas yra deguonis (oksidacijos laipsnis −2), junginys. Bendroji oksidų formulė RxOy. Oksidus sudaro visi cheminiai elementai, išskyrus Po, At, He, Ne, Ar ir F. Oksidai standartinėmis sąlygomis (STP) yra dujos (NO, NO2, SO3), skysčiai (H2O, Cl2O7) ar kietosios medžiagos (SiO2, CaO, P2O5).
Oksidų gavimo būdai
1. Tiesiogiai metalams ir nemetalams reaguojant su deguonimi:
2Mg(k) + O2(d) → 2MgO(k);
S(k) + O2(d) → SO2(d).
2. Deginant sudėtines medžiagas:
CH4(d) + 2O2(d) → CO2(d) + 2H2O(d);
2C2H5OH(s) + 7O2(d) → 4CO2(d) + 6H2O(d);
2H2S(d) + 3O2(d) → 2H2O(s) + 2SO2(d).
3. Termiškai skaidant druskas (karbonatus, nitratus, sulfatus):
2NaHCO3(k) ![]() Na2CO3(k) + CO2(d) + H2O(s);
Na2CO3(k) + CO2(d) + H2O(s);
MgCO3(k) ![]() MgO(k) + CO2(d).
MgO(k) + CO2(d).
4. Dehidratuojant (atskeliant vandenį) bazes ir rūgštis:
2Cr(OH)3(k) ![]() Cr2O3(k) + 3H2O(s);
Cr2O3(k) + 3H2O(s);
Cu(OH)2(k) ![]() CuO(k) + H2O(s);
CuO(k) + H2O(s);
2H3PO4 (aq) ![]() P2O5(k) + 3H2O(s);
P2O5(k) + 3H2O(s);
H2SO3(aq) ![]() SO2(d) + H2O(s).
SO2(d) + H2O(s).
5. Termiškai skaidant didžiausio oksidacijos laipsnio ir oksiduojant mažiausio oksidacijos laipsnio oksidus:
4CrO3(k) ![]() 2Cr2O3(k) + 3O2(d);
2Cr2O3(k) + 3O2(d);
4FeO(k) + O2(d) ![]() 2Fe2O3(k);
2Fe2O3(k);
2CO(d) + O2(d) → 2CO2(d).
6. Aukštoje temperatūroje nelakiu oksidu veikiant lakaus oksido druską:
Na2CO3(k) + SiO2(k) ![]() Na2SiO3(k) + CO2(d).
Na2SiO3(k) + CO2(d).
7. Reaguojant stiprių oksidacinių savybių turinčioms rūgštims su metalais ir kai kuriais nemetalais:
2H2SO4(s) + C(k) ![]() 2SO2(d) + CO2(d) + 2H2O(s).
2SO2(d) + CO2(d) + 2H2O(s).
Pagal chemines savybes oksidai skirstomi į:
1) rūgštinius;
2) bazinius;
3) amfoterinius;
4) neutralius (chemijos brandos egzaminų programoje įrašytas terminas „indiferentinis“ nebevartotinas).
Rūgštinius oksidus sudaro nemetalų oksidai ir didžiausio oksidacijos laipsnio metalų oksidai. Kadangi dauguma rūgštinių oksidų reaguoja su vandeniu ir susidaro atitinkamos rūgštys, tai rūgštiniai oksidai dar vadinami rūgščių anhidridais.
Rūgštiniai oksidai reaguoja:
1) su vandeniu sudarydami rūgštis:
SO2(d) + H2O(s) ![]() H2SO3(aq);
H2SO3(aq);
SO3(d) + H2O(s) → H2SO4(aq);
2) su hidroksidais:
KOH(aq) + CO2(d) → KHCO3(aq);
2KOH(aq) + CO2(d) → K2CO3(aq) + H2O(s);
3) su baziniais oksidais:
CaO(k) + SiO2(k) ![]() CaSiO3(k);
CaSiO3(k);
4) su amfoteriniais oksidais:
Al2O3(k)+ 3SO3(d) → Al2(SO4)3(k).
Kai kurių rūgštinių oksidų pavadinimai
Cl2O7 | Dichloro heptoksidas, arba chloro(VII) oksidas |
N2O5 | Diazoto pentoksidas, arba azoto(V) oksidas |
CO2 | Anglies dioksidas, arba anglies(IV) oksidas |
SO3 | Sieros trioksidas, arba sieros(VI) oksidas |
Bazinius oksidus sudaro tik metalų oksidai, pavyzdžiui, IA ir IIA grupės metalų oksidai (išskyrus BeO). Baziniai oksidai, reaguodami su vandeniu, sudaro hidroksidus.
Baziniai oksidai reaguoja:
1) su vandeniu sudarydami bazes:
CaO(k) + H2O(s) → Ca(OH)2(aq);
2) su rūgštimis:
Fe2O3(k) + 6HCl(aq) → 2FeCl3(aq) + 3H2O(s);
3) su rūgštiniais oksidais:
CaO(k) + CO2(d) → CaCO3(k);
4) su amfoteriniais oksidais:
Al2O3(k) + Li2O(k) ![]() 2LiAlO2(k).
2LiAlO2(k).
Amfoteriniai oksidai turi ir rūgštinių, ir bazinių savybių (ZnO, Al2O3, SnO ir PbO). Šie oksidai reaguoja ir su bazėmis (sudaro kompleksines druskas), ir su rūgštimis:
Al2O3(k) + 6HCl(aq) → 2AlCl3(k) + 3H2O(s);
Al2O3(k) + 2NaOH(aq) + 3H2O(s) → 2Na[Al(OH)4](aq).
Oksidų savybės labai priklauso nuo jų gavimo būdo. Pavyzdžiui, Al2O3, iškaitintas aukštoje temperatūroje, yra inertiškas. Amfoterinės Al2O3 savybės išryškėja tik tada, kai jis nėra ilgą laiką kaitinamas aukštoje temperatūroje ir tada yra blogai susikristalizavęs.
Bazinių ir amfoterinių oksidų pavadinimų pavyzdžiai
|
Pastovaus oksidacijos laipsnio oksidai | ||
|
Al2O3 |
Aliuminio oksidas | |
|
MgO |
Magnio oksidas | |
|
CaO |
Kalcio oksidas | |
|
Kintamo oksidacijos laipsnio oksidai | ||
|
Fe2O3 |
Geležies(III) oksidas | |
|
PbO |
Švino(II) oksidas | |
To paties metalo skirtingo oksidacijos laipsnio oksidams būdingos skirtingos savybės:
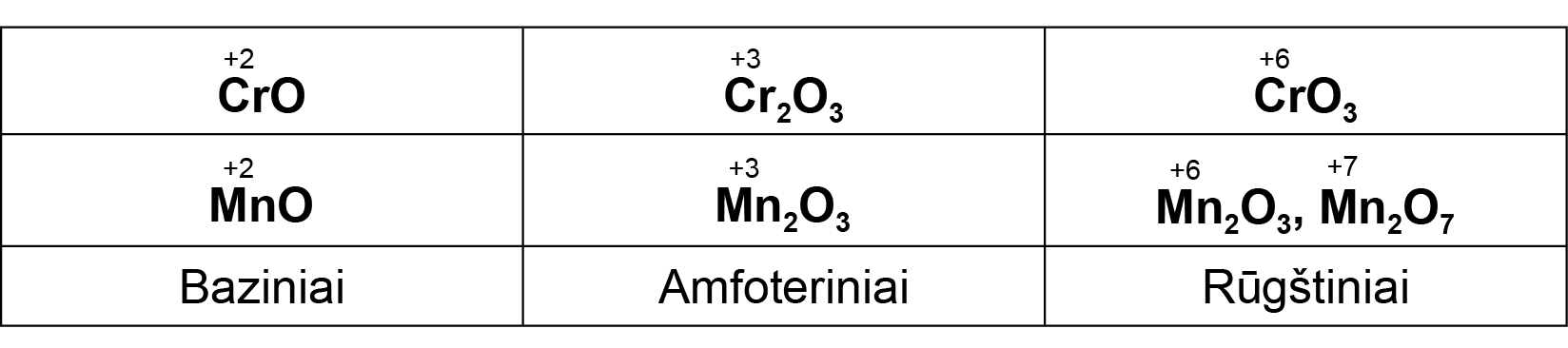
Didėjant oksidacijos laipsniui, stiprėja oksidų rūgštinės savybės.
Neutralieji oksidai (CO, NO, N2O, SiO) – tai oksidai, kuriems nebūdingos bazinės ir rūgštinės savybės reaguojant su vandeniu. Daugelis neutraliųjų oksidų tam tikromis sąlygomis (kaitinant ir esant slėgiui) gali reaguoti su šarmais ir sudaryti druskas. Pavyzdžiui:
CO + NaOH ![]() HCOONa;
HCOONa;
6NO + 4NaOH ![]() 4NaNO2 + N2 + 2H2O
4NaNO2 + N2 + 2H2O
arba 4NO + 2NaOH ![]() 2NaNO2 + N2O + 2H2O;
2NaNO2 + N2O + 2H2O;
SiO + 4NaOH → Na4SiO4 + H2 + H2O.
Oksidų bazines-rūgštines savybes paprasta nustatyti žinant elemento oksidacijos okside laipsnį (OL) ir jo elekrinio neigiamumo (EN) vertę (paimta iš M. Kurushkin, D. Kurushkin. Acid−Base
Behavior of 100 Element Oxides: Visual and Mathematical Representations.- J.
Chem. Educ. 2018, 95, 678−681):
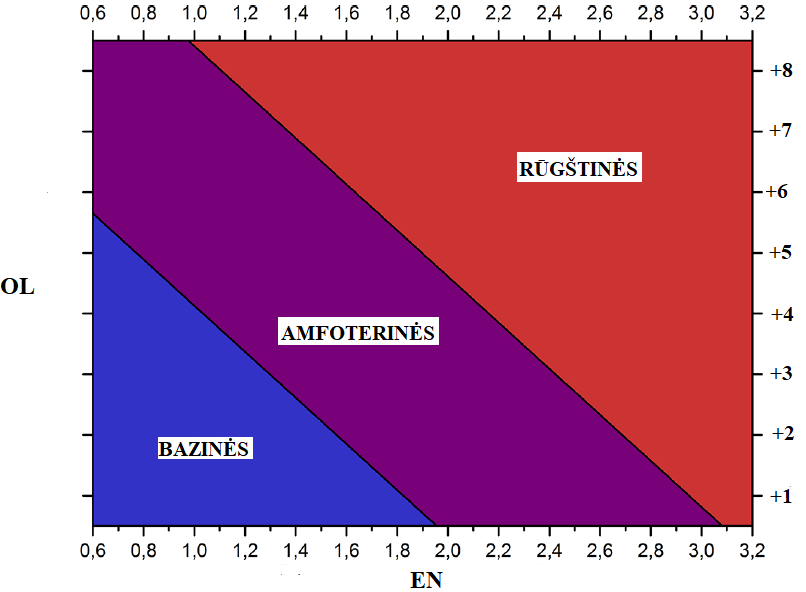
Šios diagramos tikslumas > 94 %. Ji netaikoma neutraliesiems oksidams ir 6 oksidams: rūgštiniams (Nb2O5, SiO2, P4O6) ir baziniams (ThO2, UO2, CrO) oksidams, kurie diagramoje patenka į amfoterinių oksidų sritį.
5.1.2. Hidroksidai
Hidroksidai – tai junginiai, sudaryti iš metalų jonų ir vienos ar kelių HO- grupių (MOH): KOH, Fe(OH)2, Ca(OH)2. Hidroksidai dažnai vadinami bazėmis (junginiais, galinčiais atskelti hidroksido jonus).
Pagal tirpumą vandenyje hidroksidai skirstomi į tirpius ir netirpius. Tirpūs vandenyje hidroksidai (IA ir IIA grupių elementų) vadinami šarmais: LiOH, KOH, NaOH, CsOH, RbOH, Ba(OH)2, Sr(OH)2.
Pagrindiniai bazių gavimo būdai
1. Reaguojant šarminiams ir šarminių žemių metalams su vandeniu:
2K(k) + H2O(s) → 2KOH(aq) + H2(d);
Ca(k) + 2H2O(s) → Ca(OH)2(aq) + H2(d).
2. Aktyviųjų metalų oksidams reaguojant su vandeniu:
K2O(k) + H2O(s) →2KOH(aq);
BaO(k) + H2O(s) → Ba(OH)2(aq).
3. Druskoms reaguojant su šarmais gaunami netirpūs vandenyje hidroksidai:
FeSO4(aq) + 2NaOH (aq) → Fe(OH)2(k) + Na2SO4(aq);
Fe2+(aq) + 2OH-(aq) → Fe(OH)2(k);
CrCl3(aq) + 3KOH(aq) → Cr(OH)3(k) + 3KCl(aq);
Cr3+(aq) + 3OH-(aq) → Cr(OH)3(k).
4. Vykdant šarminių metalų (IA gr.) vandeninių druskų elektrolizę.
Hidroksidai reaguoja:
1) su rūgštimis:
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(s);
(karboksirūgščių ir
aminorūgščių reakcijų lygtis su hidroksidais (žr. temoje „Organinė
chemija“);.
2) su rūgštiniais oksidais:
2NaOH(k) + SiO2(k) → Na2SiO3(k) + H2O(s);
3) su druskomis:
CuSO4(aq) + 2NaOH(aq) → Cu(OH)2(k) + Na2SO4(aq);
4) su amfoteriniais oksidais:
ZnO(k) + NaOH(aq) + H2O(s) →Na[Zn(OH)3](aq).
Kaitinami netirpūs hidroksidai skyla:
Cu(OH)2(k) ![]() CuO(k) + H2O(s).
CuO(k) + H2O(s).
Kai kurie hidroksidai (Al(OH)3, Zn(OH)2, Sn(OH)2) reaguoja ir su bazėmis, ir su rūgštimis. Tokie hidroksidai vadinami amfoteriniais:
Al(OH)3(k) + 3HCl(aq) → AlCl3(aq) + 3H2O(s);
Al(OH)3(k) + NaOH(aq) → Na[Al(OH)4](aq);
Al(OH)3(k) + OH-(aq) → [Al(OH)4]-(aq).
Šarmuose kinta indikatorių spalvos (žr. 5.2.8 skyrelį).
5.1.3. Rūgštys
Rūgštys – tai junginiai, kuriems skylant (jonizuojantis) vandenyje susidaro teigiamieji vandenilio jonai (protonai) H+. Rūgštys yra skirstomos į:
1) deguonines (H2SO4, HNO3, H2CO3, CH3COOH ir kt.);
2) nedeguones (H2S, HCl, HI, HBr ir kt.).
Pagal vandenilio atominį skaičių rūgštys skirstomos į:
1) vienprotones (HCl, HNO3 ir kt.);
2) poliprotones (H2S, H2SO4, H3PO4).
Bendroji deguoninių rūgščių formulė A(OH)mOn. Jei n = 0, tai tokia deguoninė rūgštis laikoma silpnąja (H3BO3, HClO); jei n = 1, tai deguoninė rūgštis yra silpnoji (H2CO3) arba vidutinio stiprumo (H3PO4); jei n = 2, tai rūgštis yra stiprioji (H2SO4, HNO3) (1 pav.).
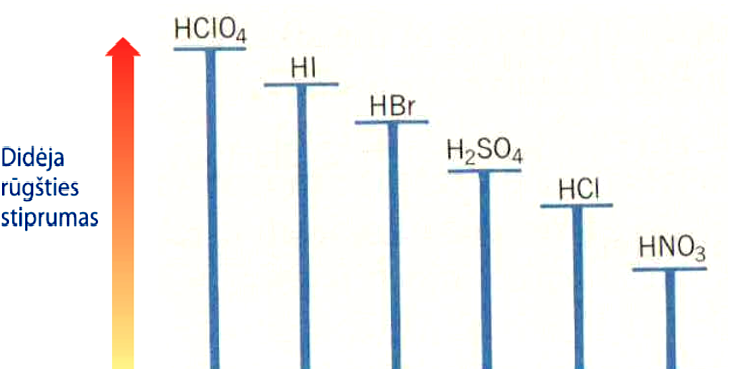
1 pav. Stipriųjų rūgščių stiprumo tarpusavio sąsaja
Kai kurių rūgščių pavadinimai
|
Formulė |
Nesisteminis pavadinimas |
Sisteminis (IUPAC) pavadinimas |
|
HCl |
Druskos rūgštis |
Vandenilio chloridas (1−) |
|
H2CO3 |
Anglies rūgštis, karbonato rūgštis |
Divandenilio trioksokarbonatas (2−) |
|
HNO3 |
Azoto rūgštis, nitrato rūgštis |
Vandenilio trioksonitratas (1−) |
|
H3PO4 |
Fosforo rūgštis, ortofosfato rūgštis |
Trivandenilio tetraoksofosfatas (3−) |
|
H2SO4 |
Sieros rūgštis, sulfato rūgštis |
Divandenilio tetraoksosulfatas (2−) |
|
H2SO3 |
Sulfito rūgštis |
Divandenilio trioksosulfatas (2−) |
|
HClO4 |
Perchlorato rūgštis |
Vandenilio tetraoksochloratas (1−) |
|
HClO |
Hipochlorito rūgštis |
Vandenilio monooksochloratas (1-) |
Chemijos laboratorijose dažnai naudojamos organinės rūgštys: metano arba skruzdžių HCOOH ir etano arba acto CH3COOH (daugiau žr. temos „Organiniai junginiai“ skyriuje „Karboksirūgštys“).
Pagrindiniai rūgščių gavimo būdai
1. Vykstant tiesioginei elementų sintezei:
Cl2(d) + H2(d) → 2HCl(d) (tirpinant vandenyje HCl(aq);
S(k) + H2(d) → H2S(d) (tirpinant vandenyje H2S(aq).
2. Tirpinant vandenyje rūgštinius oksidus (anhidridus):
SO2(d) + H2O(s) → H2SO3(aq);
N2O5 (d)+ H2O(s) → 2HNO3(aq).
3. Druskoms reaguojant su stipriosiomis rūgštimis:
NaCl(k) + H2SO4(s) → HCl(aq) + NaHSO4(aq);
NaNO3(k) + H2SO4(s) ![]() HNO3(aq) + NaHSO4(aq).
HNO3(aq) + NaHSO4(aq).
Pagal agregatinę būseną rūgštys yra skysčiai (H2SO4, HClO4) ir kietosios medžiagos (H3PO4, H2SiO3). Kai kurių rūgščių gali būti tik tirpaluose, pavyzdžiui, H2CO3, H2SO3.
Rūgštys reaguoja:
1) su bazėmis (vykstant neutralizacijos reakcijoms; (daugiau apie neutralizavimą žr. 5.2.8 skyrelį):
|
Stiprioji rūgštis ir stiprioji bazė | |
|
Visiška neutralizacija |
2NaOH(aq) + H2SO4(aq) → Na2SO4(aq) + 2H2O(s) OH−(aq) + H+(aq) → H2O(s) |
|
Nevisiška neutralizacija |
KOH(aq) + H2SO4(aq) → KHSO4(aq) + H2O(s) OH−(aq) + 2H+(aq) + SO42−(aq) → HSO4−(aq) + H2O(s) |
|
Silpnoji rūgštis ir stiprioji bazė | |
|
Visiška neutralizacija |
KOH(aq) + CH3COOH(aq) → KCH3COO(aq) + H2O(s) OH−(aq) + CH3COOH(aq) → CH3COO− (aq) + H2O(s) |
2) su baziniais oksidais:
Fe2O3(k) + 6HNO3(aq) → 2Fe(NO3)3(aq) + 3H2O(s);
Fe2O3(k) + 6H+(aq) → 2Fe3+(aq) + 3H2O(s);
3) su druskomis, jei susidaro mažai tirpus, lakus ar silpnai disocijuojantis junginys:
H2SO4(aq) + BaCl2(aq) → BaSO4(k) + 2HCl(aq);
SO42- (aq) + Ba2+(aq) → BaSO4(k);
2HCl(aq) + Na2CO3(aq) → 2NaCl(aq) + H2O(s) + CO2(d);
2H+(aq) + CO32- (aq) → H2O(s) + CO2(d);
4) kaitinamos deguonies turinčios rūgštys skyla:
H2SiO3(k) ![]() SiO2(k) + H2O(s);
SiO2(k) + H2O(s);
H2SO4(s) ![]() SO3(d) + H2O(s);
SO3(d) + H2O(s);
5) su metalais:
Zn(k) + 2HCl(aq) → ZnCl2(aq) + H2(d);
3Cu(k) + 8HNO3(aq) ![]() 3Cu(NO3)2(aq) + 2NO(d) + 4H2O(s).
3Cu(NO3)2(aq) + 2NO(d) + 4H2O(s).
Rūgštyse kinta indikatorių spalvos (žr. 5.2.8 skyrelį).
5.1.4. Druskos
Druskos – tai elektrolitai (išsamiau žr. toliau), kurie disocijuodami sudaro metalo Mn+ arba NH4+ katijoną ir rūgšties liekanos anijoną Am-. Druskos yra visiškos arba nevisiškos neutralizacijos reakcijos produktas. Pagal sudėtį ir savybes druskos skirstomos į neutraliąsias, arba normaliąsias (KNO3, CuSO4), rūgščiąsias (NaHSO4, Zn(H2PO4)2) ir kt.
Neutraliosios druskos yra visiškos neutralizacijos reakcijos produktas, sudarytas iš metalo katijonų Mn+ ir rūgšties liekanos anijonų Am-, t. y. metalo katijonai rūgštyse pakeičia vandenilio jonus, pavyzdžiui:
2Al(OH)3(k) + 3H2SO4(aq) → Al2(SO4)3(aq) + 6H2O(s).
Neutraliųjų druskų gavimo būdai
1. Metalams reaguojant su rūgštimis:
Zn(k) + 2HCl(aq) → ZnCl2(aq) + H2(d).
2. Bazėms reaguojant su rūgštimis:
NaOH(aq) + HNO3(aq) → NaNO3(aq) + H2O(s).
3. Baziniams ir amfoteriniams oksidams reaguojant su rūgštimis:
CuO(k) + H2SO4(aq) → CuSO4(aq) + H2O(s).
4. Druskoms reaguojant su rūgštimis:
H2S(aq) + CuCl2(aq) → CuS(k) + 2HCl(aq).
5. Baziniams oksidams reaguojant su rūgštiniais oksidais:
CaO(k) + CO2(d) → CaCO3(k).
6. Bazėms reaguojant su rūgštiniais oksidais:
Ca(OH)2(aq) + CO2(d) → CaCO3(k) + H2O(s).
7. Šarmams reaguojant su druskomis:
FeCl3(aq) + 3KOH(aq) → Fe(OH)3(k) + 3KCl(aq).
8. Reaguojant dviem vandenyje tirpioms druskoms:
BaCl2(aq) + Na2SO4(aq) → BaSO4(k) + 2NaCl(k).
9. Aktyviesiems metalams išstumiant mažiau aktyvius iš jų druskų tirpalų:
Zn(k) + CuSO4(aq) → ZnSO4(aq) + Cu(k).
10. Metalams reaguojant su nemetalais:
2K(k) + Cl2(d) →2KCl(k).
Druskos yra kietosios kristalinės medžiagos. Pagal tirpumą vandenyje jos skirstomos į tirpias (NaCl, KNO3), mažai tirpias (PbCl2, CaSO4) ir netirpias (BaSO4, PbSO4, PbS, CaCO3). Rūgščiosios druskos tirpsta geriau nei neutraliosios. Visos druskos yra stiprūs elektrolitai. Druskų disociacijos lygtys pateikiamos 5.2.3 skyriuje.
Druskos naudojamos pramonėje metalams gauti, medicinoje (praskiestas valgomosios druskos NaCl tirpalas – fiziologinis tirpalas, geriamoji soda NaHCO3 – skrandžio rūgštingumui mažinti, MgSO4 × 7H2O – vidurių laisvinamieji vaistai, CaSO4 × 0,5H2O – gipso tvarsčiams), buityje (valgomoji druska NaCl – maistui gardinti, NaHCO3 – pagrindinė kepimo miltelių sudedamoji dalis, natrio fosfatas Na3PO4 skalbiamųjų miltelių sudėtyje, potašas K2CO3 vandens minkštinimui) ir pramonėje (pvz. trąšos: salietros NaNO3, KNO3, NH4NO3; amonio sulfatas (NH4)2SO4; karbamidas (šlapalas) CO(NH2)2; dvigubasis superfosfatas Ca(H2PO4)2; amofosas (NH4)2HPO4)).
5.2. Tirpalai
Tirpalas – tai vienalytis skystasis arba kietasis medžiagų (tirpinio ir tirpiklio) mišinys.
Kietuosiuose tirpaluose vienos medžiagos atomai (molekulės) chaotiškai pasklinda tarp kitos kietosios medžiagos atomų (molekulių). Kietojo tirpalo pavyzdys – nerūdijantysis plienas, t. y. geležies lydinys, turintis 12–30 % Cr, ≤ 28 % Ni, ≤ 4,5 % Mo ir kitų priedų.
Jei tirpalą sudaro skystyje ištirpęs kitas skystis, nesikeičia ne tik tirpiklio, bet ir tirpinio agregatinė būsena, tai tirpikliu laikomas tas komponentas, kurio tirpale yra daugiau. Pavyzdžiui, jei 10 ml acetono (propanono) ištirpdoma 100 ml etanolio, tai tirpiklis yra etanolis. Tačiau jei tirpalas yra gaminamas iš dviejų skysčių, kurių vienas vanduo, tai vanduo visada laikomas tirpikliu, kad ir koks būtų jo kiekis. Pavyzdžiui, gaminant 65 % koncentracijos sieros rūgšties tirpalą, tirpiklio vandens jame bus 35 %.
Pagal ištirpusios medžiagos masę tirpalai yra koncentruotieji ir praskiesti.
Koncentruotasis tirpalas – tirpalas, kuriame daug ištirpusios medžiagos. Praskiestas tirpalas – mažos koncentracijos tirpalas.
Praskiestuose tirpaluose jonai arba polinės molekulės prisijungia tam tikrą skaičių vandens molekulių ir tampa hidratuotosiomis (aq) dalelėmis. Hidratuoti junginiai vadinami hidratais, kurių bendroji formulė yra [M(H2O)x]z+:
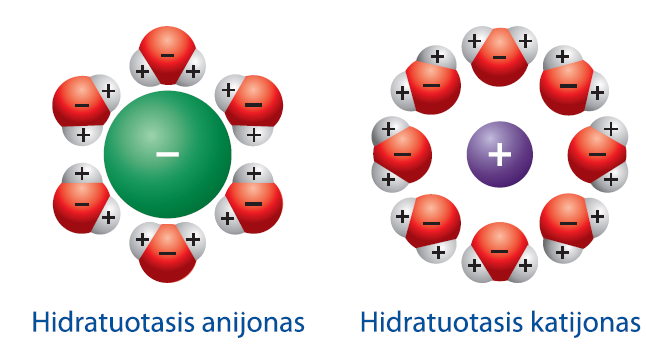
Paruošė prof. A. Šulčius
5.2.1. Procentinė ir molinė tirpalų koncentracija
Mišinių ir junginių kiekybinė sudėtis nusakoma jų sudedamųjų dalių masės dalimi, kuri reiškiama procentais. Pavyzdžiui, 15 % tirpalas reiškia, kad 100 g šio tirpalo yra 15 gramų ištirpusios medžiagos ir 85 g tirpiklio:
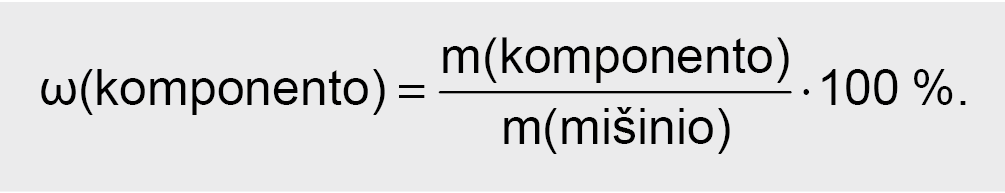
Molinė koncentracija reiškiama ištirpusios medžiagos kiekiu (n) viename litre tirpalo. Molinė koncentracija c matuojama mol/l arba mol/dm3:
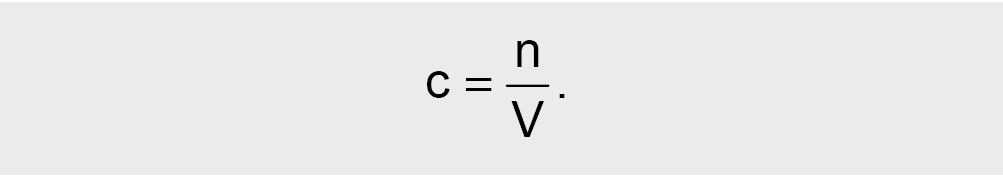
Uždavinių sprendimo pavyzdžiai
1 uždavinys
Praskiedus 800 ml 10 % CuCl2 tirpalo (r = 1,096 g/cm3), pagaminta 3 l tirpalo. Kokia gauto tirpalo molinė koncentracija?
Sprendimas
1. Apskaičiuojame 10 % CuCl2 tirpalo masę:
m(tirpalo) = V × r = 800 ml . 1,096 g/ml = 876,8 g.
2. Apskaičiuojame ištirpusios tirpale druskos masę:
10 g CuCl2 – 100 g tirpalo
x g – 876,8 g
x = 87,68 g CuCl2.
3. Apskaičiuojame tirpale ištirpusios druskos kiekį:
M(CuCl2) = 63,5 + 2 × 35,5 = 134,5 g/mol;
1 mol – 134,5 g
x – 87,68 g
x = 0,652 mol (3-uose litruose).
4. Apskaičiuojame molinę koncentraciją:
0,652 mol – 3 l
x mol – 1 l
x = 0,367 mol.
Atsakymas: 0,217 mol/l.
2 uždavinys
Apskaičiuokite 400 ml 0,2 mol/l Ba(OH)2 tirpalo procentinę koncentraciją, jei tirpalo tankis 1,15 g/ml.
Sprendimas
1. Apskaičiuojame bario hidroksido kiekį, ištirpusį 0,3 l:
1000 ml – 0,2 mol
400 ml – x mol
x = 0,08 mol.
2. Apskaičiuojame 0,08 mol bario hidroksido masę:
n = m/M
m(Ba(OH)2) = n × M = 0,08 mol × 171 g/mol = 13,68 g.
3. Apskaičiuojame 400 ml tirpalo masę:
m = V × r = 400 ml × 1,15 g/ml = 460 g.
4. Apskaičiuojame 400 ml 0,2 mol/l Ba(OH)2 tirpalo procentinę koncentraciją:
460 g tirpalo – 13,68 g Ba(OH)2
100 g tirpalo – y g
x = 2,97 g = 2,97 %.
Atsakymas: 2,97 %.
3 uždavinys
Praleidus vandenilio sulfido dujas pro 174 ml (r = 1,10 g/cm3) vario(II) sulfato tirpalą, iškrito 11,8 g nuosėdų. Apskaičiuokite vario(II) sulfato tirpalo procentinę koncentraciją.
Sprendimas
1. Užrašome ir išlyginame reakcijos lygtį ir pagal ją atliekame skaičiavimus:
CuSO4(aq) + H2S(d) → CuS(k) + H2SO4(aq);
159,5 g CuSO4 – 95,5 g CuS
x g CuSO4 – 11,8 g CuS
x = 19,71 g CuSO4.
2. Apskaičiuojame CuSO4 tirpalo masę:
m(tirpalo) = V × r = 174 ml × 1,10 g/cm3 = 191,4 g.
3. Apskaičiuojame CuSO4 procentinę koncentraciją:
I būdas
Pagal reakcijos lygtį:
191,4 g CuSO4 tirpalo – 19,71 g CuSO4
100 g CuSO4 tirpalo – y g
y = 10,30 g CuSO4 = 10,30 %.
II būdas
ω(CuSO4) = (m(medžiagos)/ m(tirpalo) )· 100 % = (19,71 g /191,4 g) · 100 % = 10,30 %
Atsakymas: 10,01 %.
4 uždavinys
Kokį tūrį 2,8 mol/l koncentracijos H2SO4 tirpalo galima pagaminti, praskiedus 900 ml 75 % H2SO4 tirpalo, kurio tankis 1,669 g/cm3?
Sprendimas
1. Apskaičiuojame pradinio tirpalo, kurio koncentracija yra 75 %, masę:
m = V · d = 900 ml · 1,669 g/ cm3 = 1502,1 g.
Tirpinio (H2SO4) masė šiame tirpale:
75 g H2SO4 – 100 g tirpalo
x g H2SO4 – 1502,1 g tirpalo
x = 1126,6 g H2SO4.
2. Skiedžiant tirpalą, tirpinio masė nekinta, tai ir naujame tirpale yra 1126,6 g H2SO4. Kadangi žinome naujo tirpalo molinę koncentraciją, tai ir tirpinio masę išreiškiame kiekio vienetais. Sieros (sulfato) rūgšties molinė masė:
M(H2SO4) = 2 · 1 + 32 + 4 · 16 = 98 g/mol.
Apskaičiuojame tirpinio kiekį:
1 mol H2SO4 – 98 g
x mol H2SO4 – 1126,6 g
x = 11,5 mol H2SO4.
3. Apskaičiuojame, kokį tūrį 2,8 mol/l H2SO4 tirpalo galima pagaminti iš 11,5 mol sulfato rūgšties:
2,8 mol H2SO4 – 1000 ml tirpalo
11,5 mol H2SO4 – x ml tirpalo
x = 4100 ml
Atsakymas: 4100 ml.
5.2.2. Elektrolitai ir neelektrolitai
Medžiagos, kurių vandeniniai tirpalai arba lydalai nepraleidžia elektros srovės, vadinamos neelektrolitais. Jais yra molekulinio tipo medžiagos.
Medžiagos, kurių vandeniniai tirpalai arba lydalai praleidžia elektros srovę, vadinamos elektrolitais (2 pav.). Elektrolitai yra medžiagos, kurios ištirpusios ar išlydytos praleidžia elektros srovę. Šios savybės būdingos rūgščių, bazių ir beveik visų druskų tirpalams. Elektrolitai, tirpdami vandenyje ar kitame poliniame tirpiklyje, savaime skyla (disocijuoja) į teigiamojo krūvio jonus − katijonus ir neigiamojo krūvio jonus – anijonus. Teigiamųjų jonų krūvių suma yra lygi neigiamųjų jonų krūvių sumai, todėl visas tirpalas yra elektriškai neutralus. Panardinus į indą su elektrolitu elektrodus ir prijungus prie jų išorinį srovės šaltinį, teigiamieji jonai (katijonai) ima slinkti prie katodo, neigiamieji jonai (anijonai) − prie anodo. Taip judėdami jonai perneša elektros krūvius (3 pav.).

2 pav. Elektrolito laidumo matavimas

3 pav. Krūvio perneša elektrolituose
Visi elektrolitai skirstomi į kelias grupes (4 pav.).
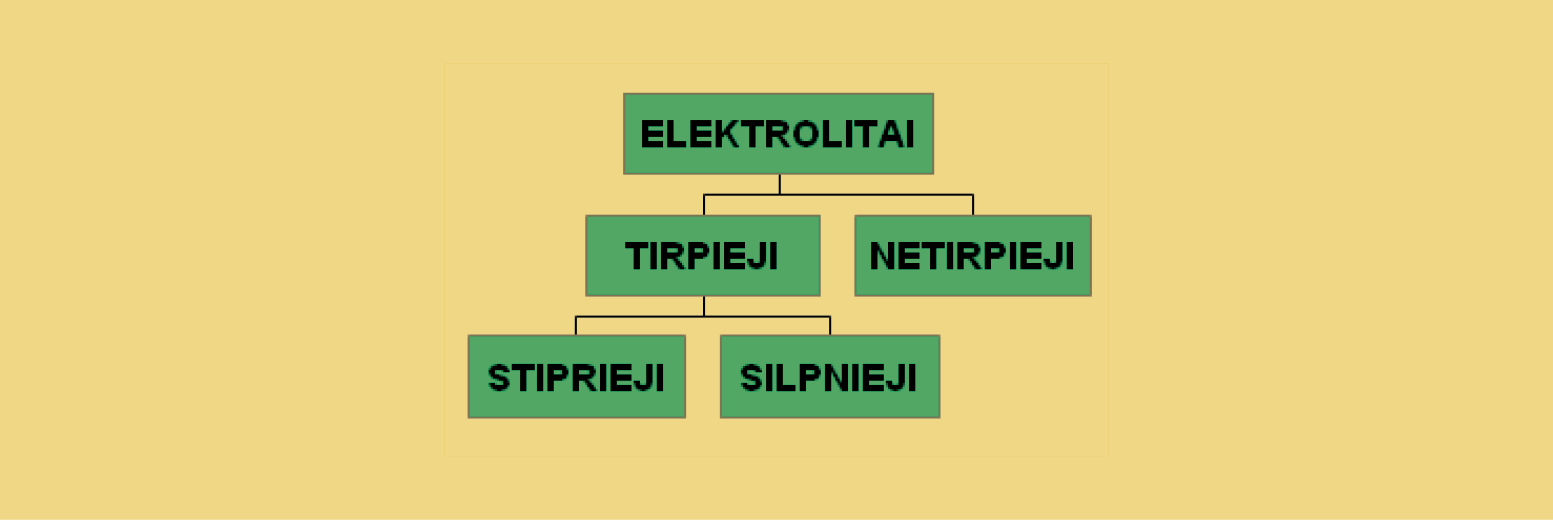
4 pav. Elektrolitų skirstymas
5.2.3. Elektrolitų jonizacija ar disociacija
Tirpinamų ar lydomų joninių junginių skaidymasis į jonus vadinamas disociacija (5 pav.).
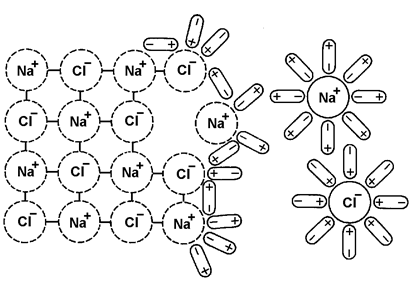
5 pav. Valgomosios druskos NaCl disociacija ir jonų hidratacija (vandens prijungimas)
NaCl disociaciją galima užrašyti taip:
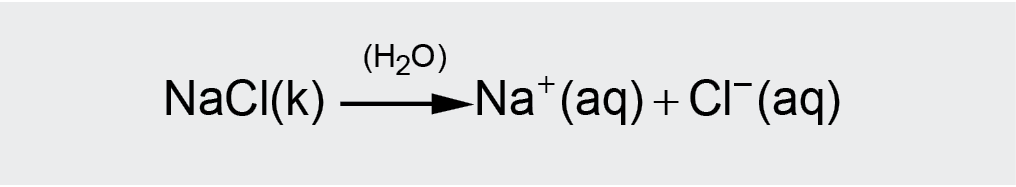
Stiprieji elektrolitai: visos tirpios druskos, dauguma neorganinių rūgščių (H2SO4, HNO3, HCl, HBr, HI, HMnO4, HClO3), šarminių ir šarminių žemių metalų hidroksidai (NaOH, KOH, Ba(OH)2).
Silpnieji elektrolitai: HF, sulfito rūgštis H2SO3, Ca(OH)2, beveik visos organinės rūgštys (pvz., HCOOH ir CH3COOH) ir kai kurios neorganinės rūgštys (H2CO3, H2S, HCN, HClO), daugelio metalų hidroksidai (išskyrus šarminių ir šarminių žemių metalų), amoniakinis vanduo NH3 · H 2O(aq), aminai R-NH2, R-NH-R1 ir kt. (apie aminus žr. temoje „Organiniai junginiai“)
Kadangi absoliučiai netirpių medžiagų nėra, ištirpusi netirpiųjų medžiagų dalis yra laikoma stipriuoju elektrolitu. Pavyzdžiui, 30 °C temperatūroje ištirpsta 10–12 mg/l CaCO3. Vadinasi, ištirpęs CaCO3 disocijuoja:
CaCO3 → Ca2+ + CO32- (žr. 5.2.7 skyriaus 5 uždavinio sprendimą)
Jonizacija yra neutralių molekulių virtimas jonais.
Elektrolitų disociacijos ar jonizacijos laipsnis α rodo, kuri ištirpusios medžiagos dalis suskilo į jonus.

Disociacijos laipsnio vertė kinta nuo 0 iki 1. Neelektrolitų tirpalų α = 0. Jeigu visa medžiaga disocijuoja į jonus, tai α = 1 arba α = 100 %.
Egzaminų lentelėse pateikiamos rūgščių ir bazių disociacijos ar jonizacijos konstantos: rūgštingumo Ka ir bazingumo Kb.
Jonizacijos/disociacijos konstantų vertės, leidžiančios atskirti stipriuosius ir silpnuosius elektrolitus, yra šios:
stipriųjų elektrolitų – kai K ≥ 10-2, vidutinio stiprumo – kai K ~10-2–10-4, silpnųjų – kai K ~10-4–10-10.
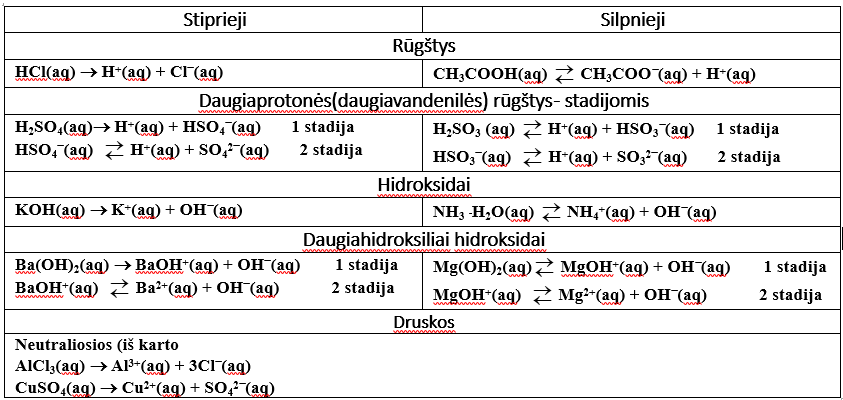
5.2.4. Rūgščių, hidroksidų ir druskų jonizacijos-disociacijos pavyzdžiai
Stiprieji elektrolitai disocijuoja ar jonizuojasi beveik visiškai (→), o silpnųjų elektrolitų disociacija ar jonizacija yra grįžtamoji ( ![]() ).
).
5.2.5. Hidridų ir oksidų bazinės-rūgštinės savybės
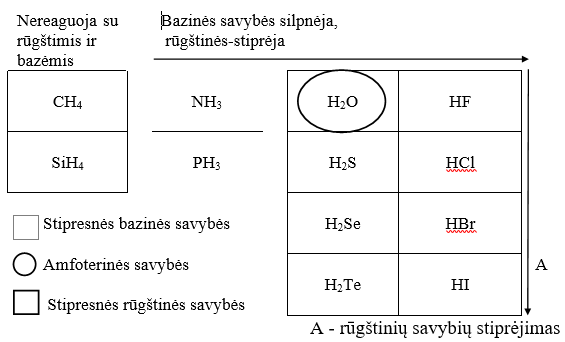
Bazinės-rūgštinės hidridų ir oksidų savybės priklauso nuo šiuos junginius sudarančių cheminių elementų padėties periodinėje lentelėje.
Hidridas – vandenilio junginys su metalu arba su mažesnio negu vandenilio elektrinio neigiamumo nemetalu. Juos tirpinant vandenyje, cheminės jų savybės kinta:
Oksidų savybių kitimas
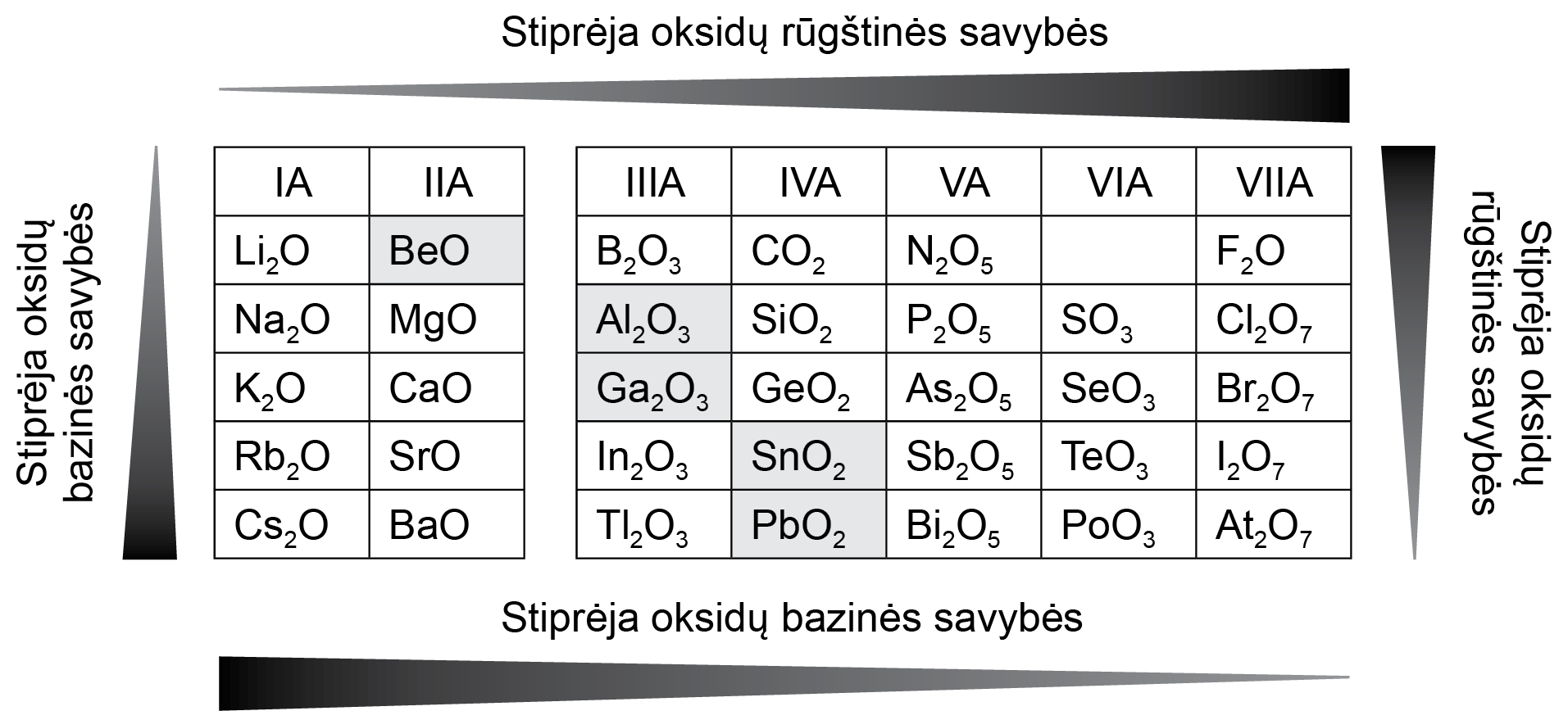
Perioduose didžiausio elementų oksidacijos laipsnio oksidų savybės pamažu kinta nuo bazinių iki rūgštinių.
5.2.6. Elektrolitų pH
Vanduo yra silpnasis elektrolitas ir šiek tiek jonizuojasi į H+ ir OH- jonus:
![]()
Parašome šios grįžtamosios reakcijos (jonizacijos) pusiausvyros konstantos formulę:
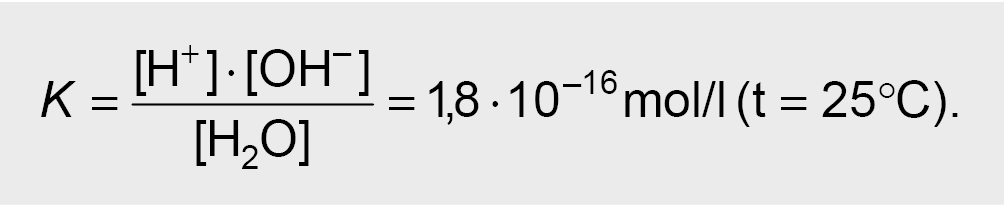
Pertvarkę formulę gauname:
[H+] · [OH–] = K · [H2O].
Kadangi vandens jonizacijos laipsnis labai mažas, tai nedisocijavusių vandens molekulių koncentraciją galima laikyti pastoviu dydžiu:

čia 1000 g yra 1 litro vandens masė.
Pažymėję [H+] ・ [OH-] = KH2O, gauname:
KH2O = K ・ [H2O] = 1,8 ・ 10-16 mol/l・55,55 mol/l = 10-16 mol2/l2
Kai temperatūra pastovi (t = 25 °C), vandens ir praskiestų vandeninių tirpalų vandenilio ir hidroksido jonų koncentracijų sandauga yra pastovus dydis, vadinamas vandens jonų koncentracijų sandauga ir lygus 10-14 mol2/l2 .
Tirpalai, kurių:
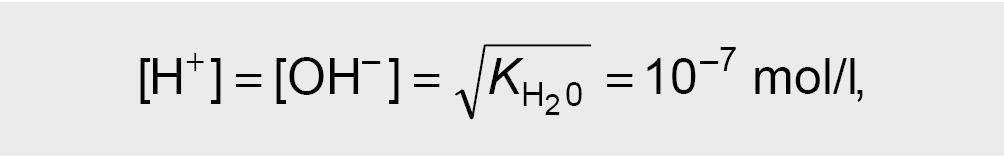
vadinami neutraliaisiais tirpalais.
Žinant vandenilio jonų koncentraciją, apskaičiuojama hidroksido jonų koncentracija, ir atvirkščiai:
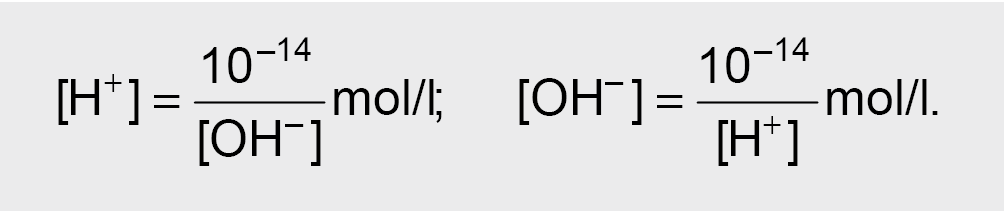
Pavyzdžiui, jei [H+] = 10–3 mol/l, tai
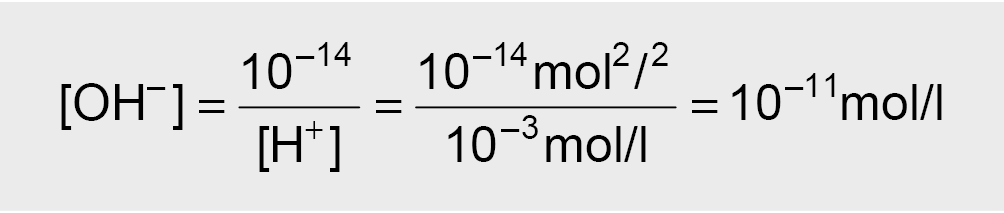 (tirpalas rūgštus);
(tirpalas rūgštus);
jei [H+] = 10–6 mol/l, tai
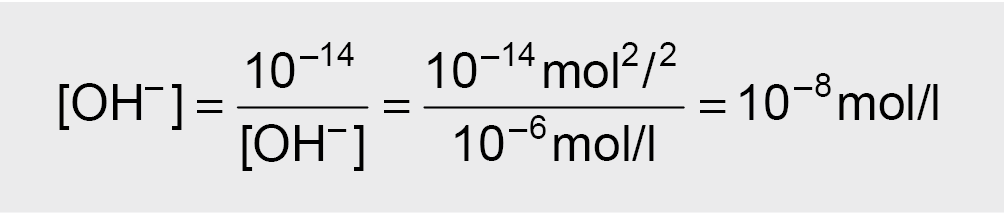 (tirpalas šarminis).
(tirpalas šarminis).
Vandenilio jonų koncentracijos vertė labai maža, todėl, kad būtų patogiau skaičiuoti, vandenilio jonų koncentracija reiškiama vandenilio jonų rodikliu, kuris žymimas pH.
pH yra lygus vandenilio jonų koncentracijos neigiamo ženklo dešimtainiam logaritmui:
pH = –lg[H+].
Kadangi [H+] · [OH-] = 10-14 mol2/l2, tai logaritmuodami gauname:
−lg[H+] · [OH-]) = −lg(10-14 ) Þ −lg[H+] + (−lg[OH-])= −lg10-14 .
pH + pOH = 14
Rūgščiojo tirpalo pH < 7, neutraliojo – pH = 7, šarminio – pH > 7.
Vandenilio jonų koncentracijos ir pH kitimas ir ryšys parodytas 6 ir 7 pav.
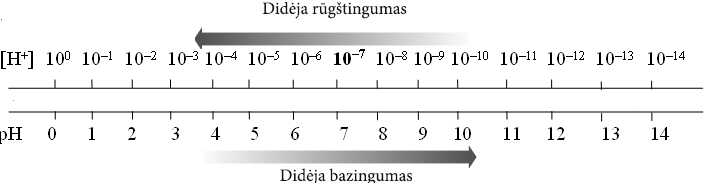
6 pav. Vandenilio jonų koncentracijos ir pH kitimas

7 pav. Vandenilio jonų koncentracijos ir pH ryšys
Tirpalų ir kai kurių maisto produktų pH vertės parodytos 8 pav.
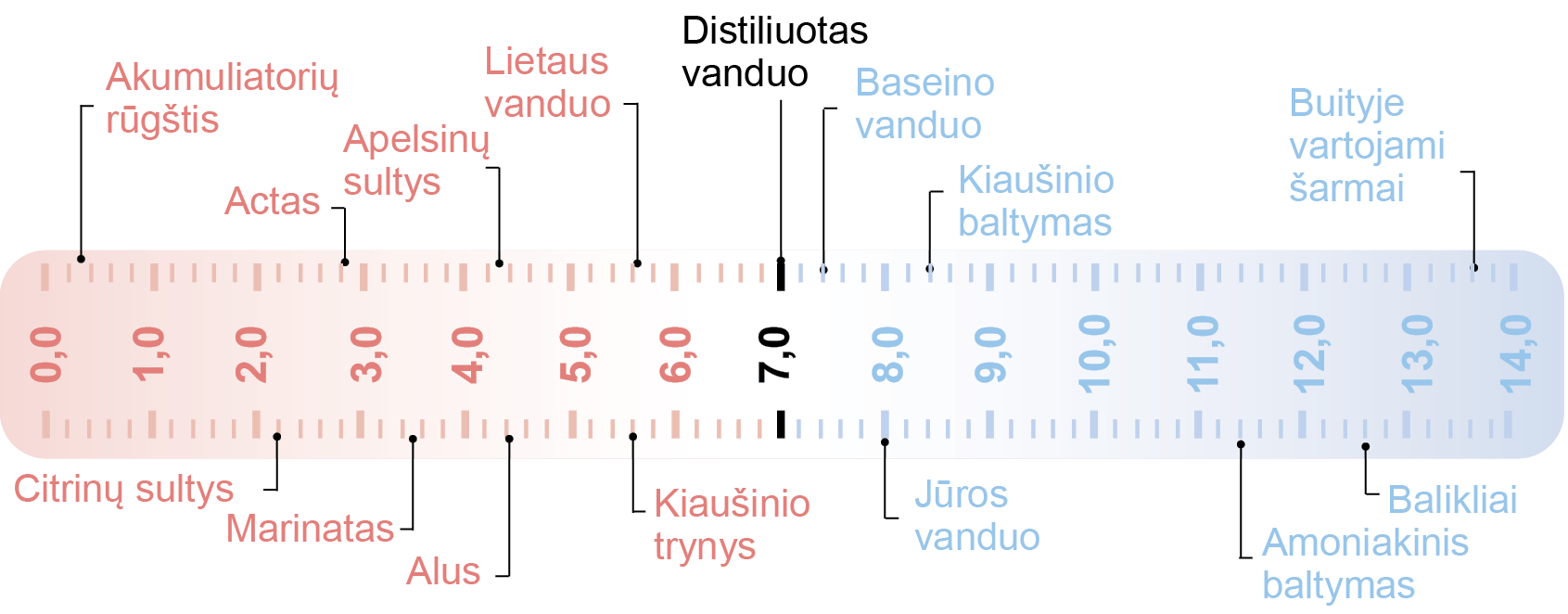
8 pav. Buityje naudojamų tirpalų ir kai kurių maisto produktų pH vertės
5.2.7. pH uždavinių sprendimo pavyzdžiai
1 uždavinys
Nustatyti Na2CO3, KCH3COO, K2SO4 ir NaCl druskų tirpalų apytikrę pH vertę.
Sprendimas
Nurodytos druskos yra gerai tirpūs vandenyje joniniai junginiai. Parašome jų disociacijos lygtis:
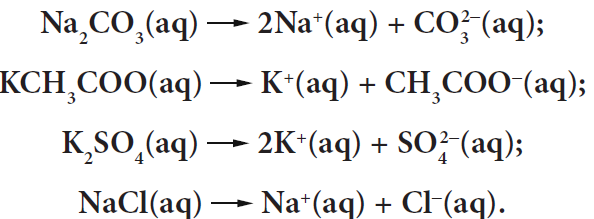
Žinoma, kad silpnųjų rūgščių anijonai hidrolizuojasi*, o stipriųjų rūgščių anijonai nesihidrolizuoja:
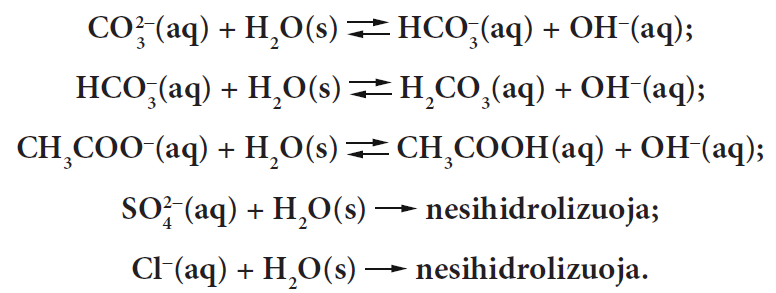
Remdamiesi reakcijų lygtimis, darome išvadą, kad Na2CO3 ir KCH3COO druskų vandeninių tirpalų pH vertė didesnė nei 7, o K2SO4 ir NaCl – pH = ~7
*Hidrolizė – grįžtamoji jonų reakcija su vandeniu
2 uždavinys
Į 200 g 10 % procentų druskos rūgšties tirpalą įpilta 20 g natrio šarmo tirpalo. Kokia gauto tirpalo terpė?
Sprendimas
1. Apskaičiuojame druskos rūgšties molinę koncentraciją:
100 g tirpalo – 10 g HCl
200 g tirpalo – x g
x = 20 g HCl.
2. Apskaičiuojame druskos rūgšties ir natrio šarmo kiekius:
n = m /M(HCl) = 20 g / 36,5 g/mol = 0,548 mol;
n = m / M(NaOH) = 20 g/ 40 g/mol = 0,50 mol.
3. Parašome reakcijos lygtį ir nustatome terpės pobūdį:
1 mol 1 mol
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(s).
0,5 mol 0,5 mol
Gautas rūgšties kiekis yra didesnis nei teoriškai apskaičiuotas (0,548 mol > 0,50 mol), taigi jos yra perteklius. Todėl darome išvadą, kad terpė rūgštinė (pH < 7).
Atsakymas: terpė yra rūgštinė (pH < 7).
3 uždavinys
Apskaičiuokite 0,1 mol/l H2SO4 tirpalo pH.
Sprendimas
Parašykime H2SO4 jonizacijos lygtį, žinodami, kad stiprusis elektrolitas H2SO4 jonizuojasi visiškai (be pakopų) ir susidaro du moliai vandenilio jonų:
H2SO4(aq) ![]() 2H+(aq) + SO42–(aq).
2H+(aq) + SO42–(aq).
1. Iš jonizacijos lygties matyti, kad jonizuojantis H2SO4 susidaro du moliai H+ jonų. Apskaičiuojame vandenilio jonų koncentraciją tirpale:
c(H+) = 0,1 mol/l × 2 = 0,2 mol/l = 2,0 × 10–1 mol/l.
2. Apskaičiuojame 0,1 mol/l H2SO4 tirpalo vandenilio rodiklį:
pH = –lg(2,0 × 10–1) = –(lg 10–1 + lg 2,0) = –(–1 + 0,30) = 0,70.
Vadinasi, šis elektrolitas yra stipriai rūgštus.
Atsakymas: 0,1 mol/l H2SO4 tirpalo pH = 0,70.
4 uždavinys
Viename litre tirpalo ištirpinta 0,56 g kalio šarmo. Apskaičiuokite šio tirpalo pH.
Sprendimas
1. Apskaičiuojame tirpalo molinę koncentraciją:
n = m/M = 0,56 g/l /(56 g/mol × 1l) = 0,01 mol/l.
Kalio šarmo disociacijos lygtis yra tokia:
KOH(aq) → K+(aq) + OH–(aq).
2. Disocijuojant 1 mol KOH susidaro 1 mol OH– jonų. Apskaičiuojame OH– jonų koncentraciją tirpale:
[OH–] = 0,01 mol/l × 1 = 0,01 = 1,0 × 10–2 mol/l.
3. Apskaičiuojame vandenilio jonų koncentraciją 0,01 mol/l KOH:
[H+] = 10–14 / [OH–] = 10–14 mol2/l2 / (1,0 × 10–2 mol/l) = 1,0 × 10–12 mol/l.
4. Apskaičiuojame KOH tirpalo vandenilio rodiklį:
pH = –lg (1,0 × 10–12) = 12.
Vadinasi, šis elektrolitas yra stipriai bazinis.
Atsakymas: KOH tirpalo vandenilio jonų rodiklis pH = 12.
5 uždavinys
Apskaičiuokite kalcio karbonato, kurio tirpumas 20oC vandenyje yra 12 mg/l, tirpalo pH vertę.
Sprendimas
1. Užrašome reakcijos lygtį:
CaCO3(aq) → Ca2+(aq) + CO32–(aq);
CO32–(aq) + H2O(s) ![]() HCO3–(aq) + OH–(aq).
HCO3–(aq) + OH–(aq).
2. Remdamiesi užrašytomis lygtimis darome išvadą:
n(CaCO3) = n(CO32–) = n(OH–) = 12 mg/l / 100000 mg/mol = 1,2 · 10-4 mol/l
[H+] = 10–14 mol2/l2 / 1,2 · 10-4 mol/l = 0,833 · 10-10 mol/l
pH = 10,08
Atsakymas: pH »10,08.
5.2.8. Indikatoriai ir neutralizavimas
Tirpalo pH apytikrė vertė dažniausiai nustatoma kolorimetriniu būdu tirpalą dažant indikatoriais*. Jų yra labai įvairių, bet mokykloje dažniausiai naudojami šie: lakmusas, fenolftaleinas ir metiloranžinis.
*Indikatorius − medžiaga, keičianti spalvą pasikeitus tirpalo tiriamojo komponento koncentracijai.
Iš indikatoriaus spalvos sprendžiama, kokia tirpalo pH vertė:

Tirpalų apytikrei pH vertei nustatyti dažnai naudojami indikatoriniai popierėliai:

Jei neturime indikatorių, tirpalų terpei nustatyti galime vartoti raudongūžių kopūstų sultis:
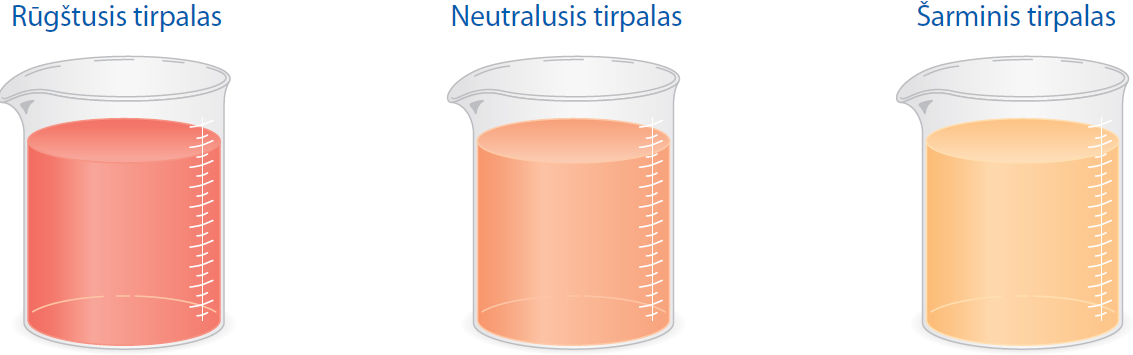
Augalų pigmentų spalvos kitimo rūgštyse ir distiliuotame vandenyje pavyzdžiai pateikiami lentelėje:

Viena iš mainų reakcijų yra neutralizacija. Tai reakcija tarp bazinės ir rūgštinės prigimties medžiagų. Mokyklose nagrinėjama tik stipriųjų elektrolitų neutralizacija: stipriosios rūgšties titravimas* (8 pav.) stipriąja baze ir stipriosios bazės titravimas stipriąja rūgštimi.
Neutralizacijos požymiai:
1) išsiskiria šiluma (tirpalas įšyla);
2) įdėjus indikatoriaus, kintajo spalva;
3) pakinta reakcijos terpės pH. Visiškos neutralizacijos terpės pH vertė yra 7.
*Titravimas – reagento tirpalo pylimas iš biuretės į titruojamąjį tirpalą, kol baigiasi reakcija (pasikeičia indikatoriaus spalva ar staiga padidėja pH vertė).
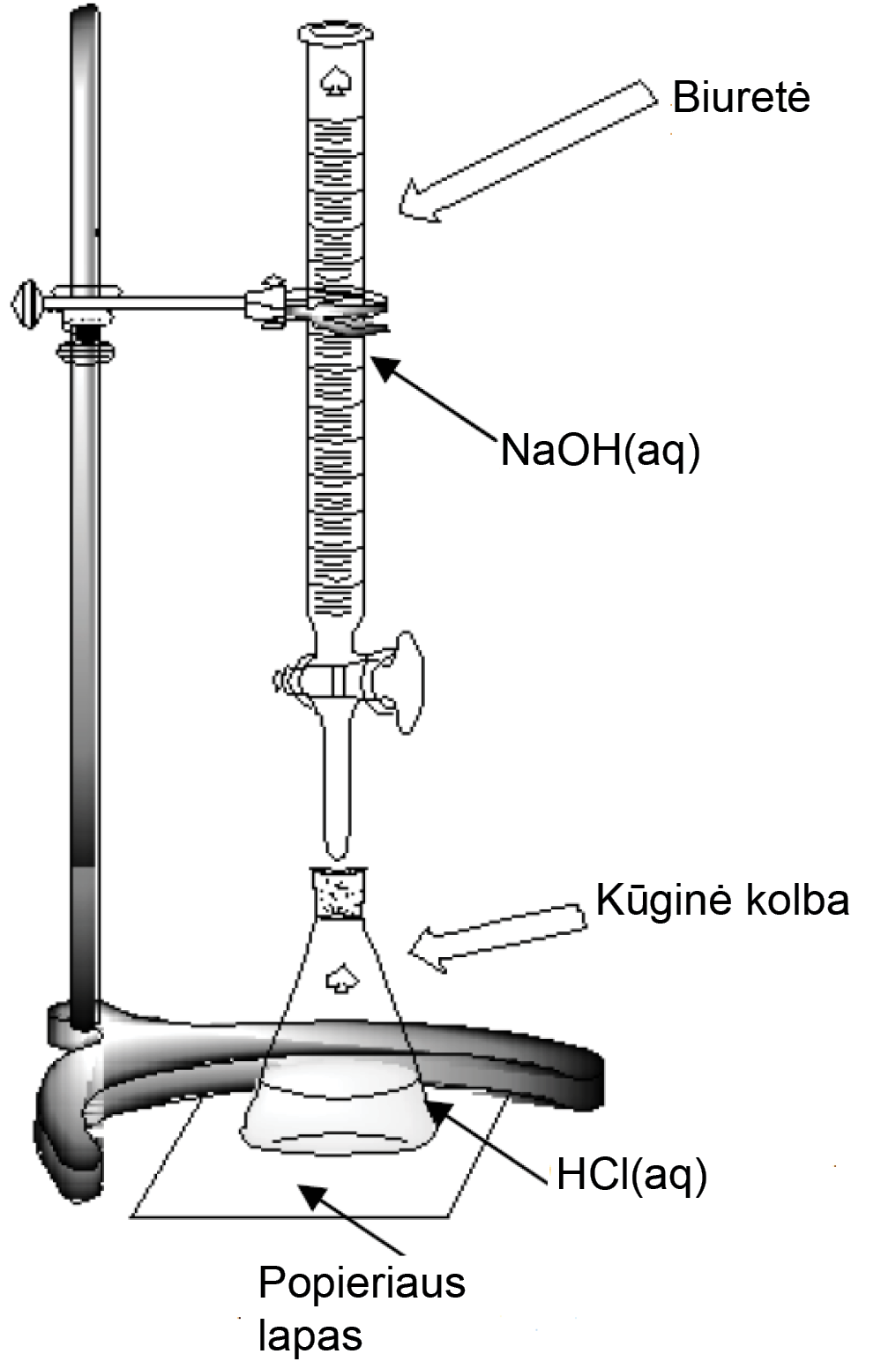
8 pav. HCl(aq) titravimas NaOH tirpalu
Titravimo matavimų tikslumas priklauso nuo daugelio veiksnių: reakciją stebinčio žmogaus regos gebos, vartojamų tirpalų koncentracijos ir kt. HCl titruojant mažesnės koncentracijos NaOH tirpalu (pavyzdžiui ne 0,1 mol/l, bet 0,05 mol/l) titravimo rezultatai būtų tikslesni.
5.2.9. Tirpalų tankio priklausomybė nuo koncentracijos
Tirpiklyje ištirpinus bet kokio tirpinio yra gaunamas tirpalas, kurio savybės skiriasi nuo gryno tirpiklio. Viena iš tokių savybių yra tirpalo tankis. Kadangi dažniausiai susiduriama su įvarių medžiagų vandeniniais tirpalais, todėl čia bus pateiktos kai kurių gerai vandenyje tirpių medžiagų tirpalų tankio priklausomybės nuo ištirpusios medžiagos (tirpinio) masės dalies tirpale. Šios priklausomybės yra nustatomos eksperimentiškai matuojant skirtingos koncntracijos tirpalų tankį esant pastoviai temperatūrai (dažniausiai 20 oC) ir pateikiamos lentelių pavidalu arba atvaizduojamos grafiškai:
Valgomosios druskos vandeninio tirpalo tankio priklausomybė nuo NaCl masės dalies jame (esant 20 oC temperatūrai)
| c, % | 1 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 | 22 | 24 | 26 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Tankis, g/cm3 | 1,005 | 1,012 | 1,027 | 1,041 | 1,056 | 1,071 | 1,086 | 1,101 | 1,116 | 1,132 | 1,148 | 1,164 | 1,180 | 1,197 |
Vadovaujantis šiomis priklausomybėmis galima gan tiksliai surasti tirpinio masės dalį paruoštame tirpale, prieš tai išmatavus nurodytos temperatūros tirpalo tankį areometru: https://www.youtube.com/watch?v=0rj8s6mMAsE
5.2.10. Įvairių medžiagų tirpumo priklausomybė nuo temperatūros
Kai kurių kietųjų medžiagų tirpumo vandenyje priklausomybės nuo temperatūros
Tirpalai – tai vienalyčiai mišiniai. Jie yra skirstomi į:
- Nesočiuosius (tam tikroje temperatūroje, į tirpalą pridėjus dar medžiagos, ji ištirpsta).
- Sočiuosius (tam tikroje temperatūroje, į tirpalą pridėjus dar medžiagos, ji nebetirpsta).
- Persotintuosius (tam tikroje temperatūroje ištirpusios medžiagos yra daugiau, negu jos gali būti sočiajame tirpale).
Bet kuris tirpumo kreivės taškas rodo, kokia didžiausia medžiagos masė ištirpsta 100 g vandens tam tikroje temperatūroje, susidarant sočiajam tirpalui.
- Iš nesotaus sotųjį tirpalą galima gauti ištirpinus tam tikrą kiekį medžiagos arba tirpalą atšaldžius.
- Iš sotaus tirpalo nesotųjį galima gauti tirpalą pašildžius arba įpylus daugiau tirpiklio.
- Persotintas tirpalas susidaro lėtai šaldant sotųjį tirpalą. Jeigu šaldant iškrenta kristalai, gauname sotųjį tirpalą žemesnėje temperatūroje. Persotintieji tirpalai yra labai nepatvarūs, atsiradus kristalizacijos centrui – jie išsikristalizuoja.
1 pav. Kai kurių natrio druskų tirpumo vandenyje priklausomybė nuo temperatūros
2 pav. Kai kurių kalio druskų tirpumo vandenyje priklausomybė nuo temperatūros
3 pav. Kai kurių hidroksidų tirpumo vandenyje priklausomybė nuo temperatūros
4 pav. Kalcio hidroksido tirpumo vandenyje priklausomybė nuo temperatūros
Kai kurių dujų tirpumo vandenyje priklausomybės nuo temperatūros (kai p=101,325 kPa)
Dažniausiai įvairių dujų tirpumo vandenyje priklausomybės nuo temperatūros yra atvaizduojamos grafiškai. Tačiau tikslias dujų tirpumo vertes galima rasti žinynų lentelės.Atkreipkite dėmesį: didėjant temperatūrai daugumos dujų tirpumas vandenyje mažėja!!! Ypač menkai tirpių dujų tirpumas vandenyje beveik nekinta didėjant temperatūrai.
Pagrindinių orą sudarančių dujų (N2, O2) tirpumas vandenyje yra gan mažas. Vandenilio bei visų inertinių dujų tirpumas vandenyje yra ypač mažas.
CO2 ir H2S tirpumas yra gerokai didesnis nei pagrindinių orą sudarančių dujų.
Tačiau tokių dujų, kurios ištirpę vandenyje gana gerai jonizuojasi (NH3, SO2, HCl), tirpumas vandenyje yra ypač didelis.
5 pav. Azoto (N2), deguonies (O2) ir vandenilio (H2) dujų tirpumo vandenyje priklausomybė nuo temperatūros (kai p=101,325 kPa)
6 pav. CO2 ir H2S dujų tirpumo vandenyje priklausomybė nuo temperatūros (kai p=101,325 kPa)
7 pav. NH3, SO2 ir HCl dujų tirpumo vandenyje priklausomybė nuo temperatūros (kai p=101,325 kPa)