Teorinė medžiaga
5.1. Neorganinių junginių tipai
5.1.1. Oksidai
Oksidai − dviejų cheminių elementų, kurių vienas yra deguonis (oksidacijos laipsnis −2), junginys. Bendroji oksidų formulė RxOy. Oksidus sudaro visi cheminiai elementai, išskyrus Po, At, He, Ne, Ar ir F. Oksidai standartinėmis sąlygomis (STP) yra dujos (NO, NO2, SO3), skysčiai (H2O, Cl2O7) ar kietosios medžiagos (SiO2, CaO, P2O5).
Oksidų gavimo būdai
1. Tiesiogiai metalams ir nemetalams reaguojant su deguonimi:
2Mg(k) + O2(d) → 2MgO(k);
S(k) + O2(d) → SO2(d).
2. Deginant sudėtines medžiagas:
CH4(d) + 2O2(d) → CO2(d) + 2H2O(d);
2C2H5OH(s) + 7O2(d) → 4CO2(d) + 6H2O(d);
2H2S(d) + 3O2(d) → 2H2O(s) + 2SO2(d).
3. Termiškai skaidant druskas (karbonatus, nitratus, sulfatus):
2NaHCO3(k) ![]() Na2CO3(k) + CO2(d) + H2O(s);
Na2CO3(k) + CO2(d) + H2O(s);
MgCO3(k) ![]() MgO(k) + CO2(d).
MgO(k) + CO2(d).
4. Dehidratuojant (atskeliant vandenį) bazes ir rūgštis:
2Cr(OH)3(k) ![]() Cr2O3(k) + 3H2O(s);
Cr2O3(k) + 3H2O(s);
Cu(OH)2(k) ![]() CuO(k) + H2O(s);
CuO(k) + H2O(s);
2H3PO4 (aq) ![]() P2O5(k) + 3H2O(s);
P2O5(k) + 3H2O(s);
H2SO3(aq) ![]() SO2(d) + H2O(s).
SO2(d) + H2O(s).
5. Termiškai skaidant didžiausio oksidacijos laipsnio ir oksiduojant mažiausio oksidacijos laipsnio oksidus:
4CrO3(k) ![]() 2Cr2O3(k) + 3O2(d);
2Cr2O3(k) + 3O2(d);
4FeO(k) + O2(d) ![]() 2Fe2O3(k);
2Fe2O3(k);
2CO(d) + O2(d) → 2CO2(d).
6. Aukštoje temperatūroje nelakiu oksidu veikiant lakaus oksido druską:
Na2CO3(k) + SiO2(k) ![]() Na2SiO3(k) + CO2(d).
Na2SiO3(k) + CO2(d).
7. Reaguojant stiprių oksidacinių savybių turinčioms rūgštims su metalais ir kai kuriais nemetalais:
2H2SO4(s) + C(k) ![]() 2SO2(d) + CO2(d) + 2H2O(s).
2SO2(d) + CO2(d) + 2H2O(s).
Pagal chemines savybes oksidai skirstomi į:
1) rūgštinius;
2) bazinius;
3) amfoterinius;
4) neutralius (chemijos brandos egzaminų programoje įrašytas terminas „indiferentinis“ nebevartotinas).
Rūgštinius oksidus sudaro nemetalų oksidai ir didžiausio oksidacijos laipsnio metalų oksidai. Kadangi dauguma rūgštinių oksidų reaguoja su vandeniu ir susidaro atitinkamos rūgštys, tai rūgštiniai oksidai dar vadinami rūgščių anhidridais.
Rūgštiniai oksidai reaguoja:
1) su vandeniu sudarydami rūgštis:
SO2(d) + H2O(s) ![]() H2SO3(aq);
H2SO3(aq);
SO3(d) + H2O(s) → H2SO4(aq);
2) su hidroksidais:
KOH(aq) + CO2(d) → KHCO3(aq);
2KOH(aq) + CO2(d) → K2CO3(aq) + H2O(s);
3) su baziniais oksidais:
CaO(k) + SiO2(k) ![]() CaSiO3(k);
CaSiO3(k);
4) su amfoteriniais oksidais:
Al2O3(k)+ 3SO3(d) → Al2(SO4)3(k).
Kai kurių rūgštinių oksidų pavadinimai
Cl2O7 | Dichloro heptoksidas, arba chloro(VII) oksidas |
N2O5 | Diazoto pentoksidas, arba azoto(V) oksidas |
CO2 | Anglies dioksidas, arba anglies(IV) oksidas |
SO3 | Sieros trioksidas, arba sieros(VI) oksidas |
Bazinius oksidus sudaro tik metalų oksidai, pavyzdžiui, IA ir IIA grupės metalų oksidai (išskyrus BeO). Baziniai oksidai, reaguodami su vandeniu, sudaro hidroksidus.
Baziniai oksidai reaguoja:
1) su vandeniu sudarydami bazes:
CaO(k) + H2O(s) → Ca(OH)2(aq);
2) su rūgštimis:
Fe2O3(k) + 6HCl(aq) → 2FeCl3(aq) + 3H2O(s);
3) su rūgštiniais oksidais:
CaO(k) + CO2(d) → CaCO3(k);
4) su amfoteriniais oksidais:
Al2O3(k) + Li2O(k) ![]() 2LiAlO2(k).
2LiAlO2(k).
Amfoteriniai oksidai turi ir rūgštinių, ir bazinių savybių (ZnO, Al2O3, SnO ir PbO). Šie oksidai reaguoja ir su bazėmis (sudaro kompleksines druskas), ir su rūgštimis:
Al2O3(k) + 6HCl(aq) → 2AlCl3(k) + 3H2O(s);
Al2O3(k) + 2NaOH(aq) + 3H2O(s) → 2Na[Al(OH)4](aq).
Oksidų savybės labai priklauso nuo jų gavimo būdo. Pavyzdžiui, Al2O3, iškaitintas aukštoje temperatūroje, yra inertiškas. Amfoterinės Al2O3 savybės išryškėja tik tada, kai jis nėra ilgą laiką kaitinamas aukštoje temperatūroje ir tada yra blogai susikristalizavęs.
Bazinių ir amfoterinių oksidų pavadinimų pavyzdžiai
|
Pastovaus oksidacijos laipsnio oksidai | ||
|
Al2O3 |
Aliuminio oksidas | |
|
MgO |
Magnio oksidas | |
|
CaO |
Kalcio oksidas | |
|
Kintamo oksidacijos laipsnio oksidai | ||
|
Fe2O3 |
Geležies(III) oksidas | |
|
PbO |
Švino(II) oksidas | |
To paties metalo skirtingo oksidacijos laipsnio oksidams būdingos skirtingos savybės:
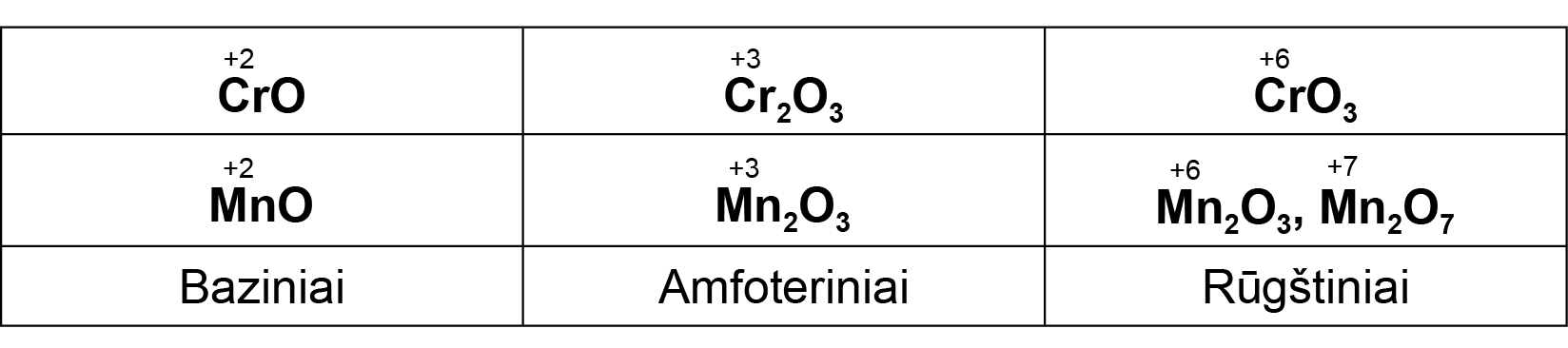
Didėjant oksidacijos laipsniui, stiprėja oksidų rūgštinės savybės.
Neutralieji oksidai (CO, NO, N2O, SiO) – tai oksidai, kuriems nebūdingos bazinės ir rūgštinės savybės reaguojant su vandeniu. Daugelis neutraliųjų oksidų tam tikromis sąlygomis (kaitinant ir esant slėgiui) gali reaguoti su šarmais ir sudaryti druskas. Pavyzdžiui:
CO + NaOH ![]() HCOONa;
HCOONa;
6NO + 4NaOH ![]() 4NaNO2 + N2 + 2H2O
4NaNO2 + N2 + 2H2O
arba 4NO + 2NaOH ![]() 2NaNO2 + N2O + 2H2O;
2NaNO2 + N2O + 2H2O;
SiO + 4NaOH → Na4SiO4 + H2 + H2O.
Oksidų bazines-rūgštines savybes paprasta nustatyti žinant elemento oksidacijos okside laipsnį (OL) ir jo elekrinio neigiamumo (EN) vertę (paimta iš M. Kurushkin, D. Kurushkin. Acid−Base
Behavior of 100 Element Oxides: Visual and Mathematical Representations.- J.
Chem. Educ. 2018, 95, 678−681):
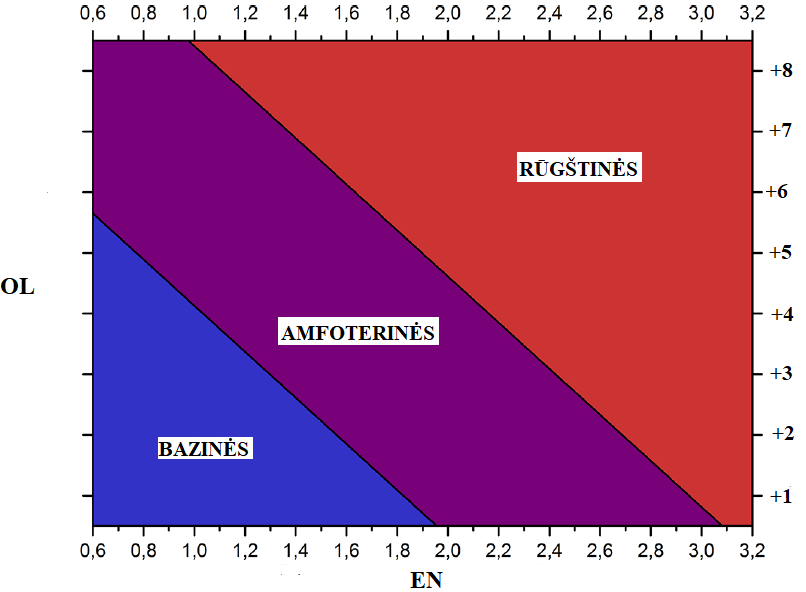
Šios diagramos tikslumas > 94 %. Ji netaikoma neutraliesiems oksidams ir 6 oksidams: rūgštiniams (Nb2O5, SiO2, P4O6) ir baziniams (ThO2, UO2, CrO) oksidams, kurie diagramoje patenka į amfoterinių oksidų sritį.
