Teorinė medžiaga
5.2. Tirpalai
5.2.8. Indikatoriai ir neutralizavimas
Tirpalo pH apytikrė vertė dažniausiai nustatoma kolorimetriniu būdu tirpalą dažant indikatoriais*. Jų yra labai įvairių, bet mokykloje dažniausiai naudojami šie: lakmusas, fenolftaleinas ir metiloranžinis.
*Indikatorius − medžiaga, keičianti spalvą pasikeitus tirpalo tiriamojo komponento koncentracijai.
Iš indikatoriaus spalvos sprendžiama, kokia tirpalo pH vertė:

Tirpalų apytikrei pH vertei nustatyti dažnai naudojami indikatoriniai popierėliai:

Jei neturime indikatorių, tirpalų terpei nustatyti galime vartoti raudongūžių kopūstų sultis:
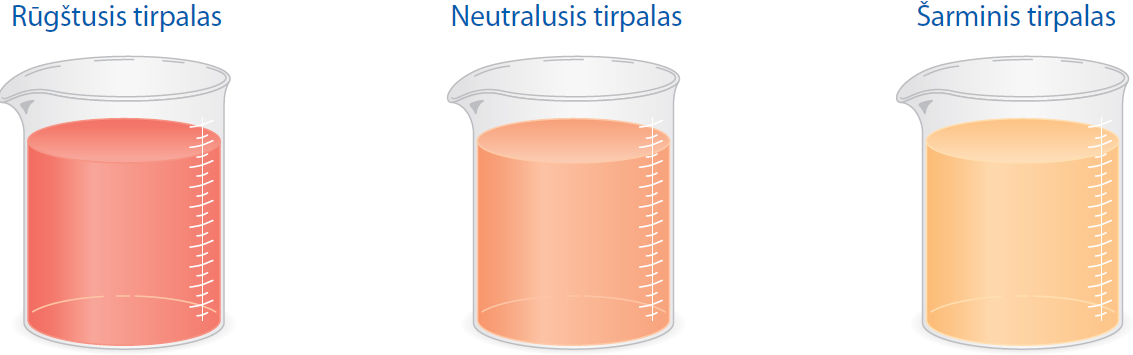
Augalų pigmentų spalvos kitimo rūgštyse ir distiliuotame vandenyje pavyzdžiai pateikiami lentelėje:

Viena iš mainų reakcijų yra neutralizacija. Tai reakcija tarp bazinės ir rūgštinės prigimties medžiagų. Mokyklose nagrinėjama tik stipriųjų elektrolitų neutralizacija: stipriosios rūgšties titravimas* (8 pav.) stipriąja baze ir stipriosios bazės titravimas stipriąja rūgštimi.
Neutralizacijos požymiai:
1) išsiskiria šiluma (tirpalas įšyla);
2) įdėjus indikatoriaus, kintajo spalva;
3) pakinta reakcijos terpės pH. Visiškos neutralizacijos terpės pH vertė yra 7.
*Titravimas – reagento tirpalo pylimas iš biuretės į titruojamąjį tirpalą, kol baigiasi reakcija (pasikeičia indikatoriaus spalva ar staiga padidėja pH vertė).
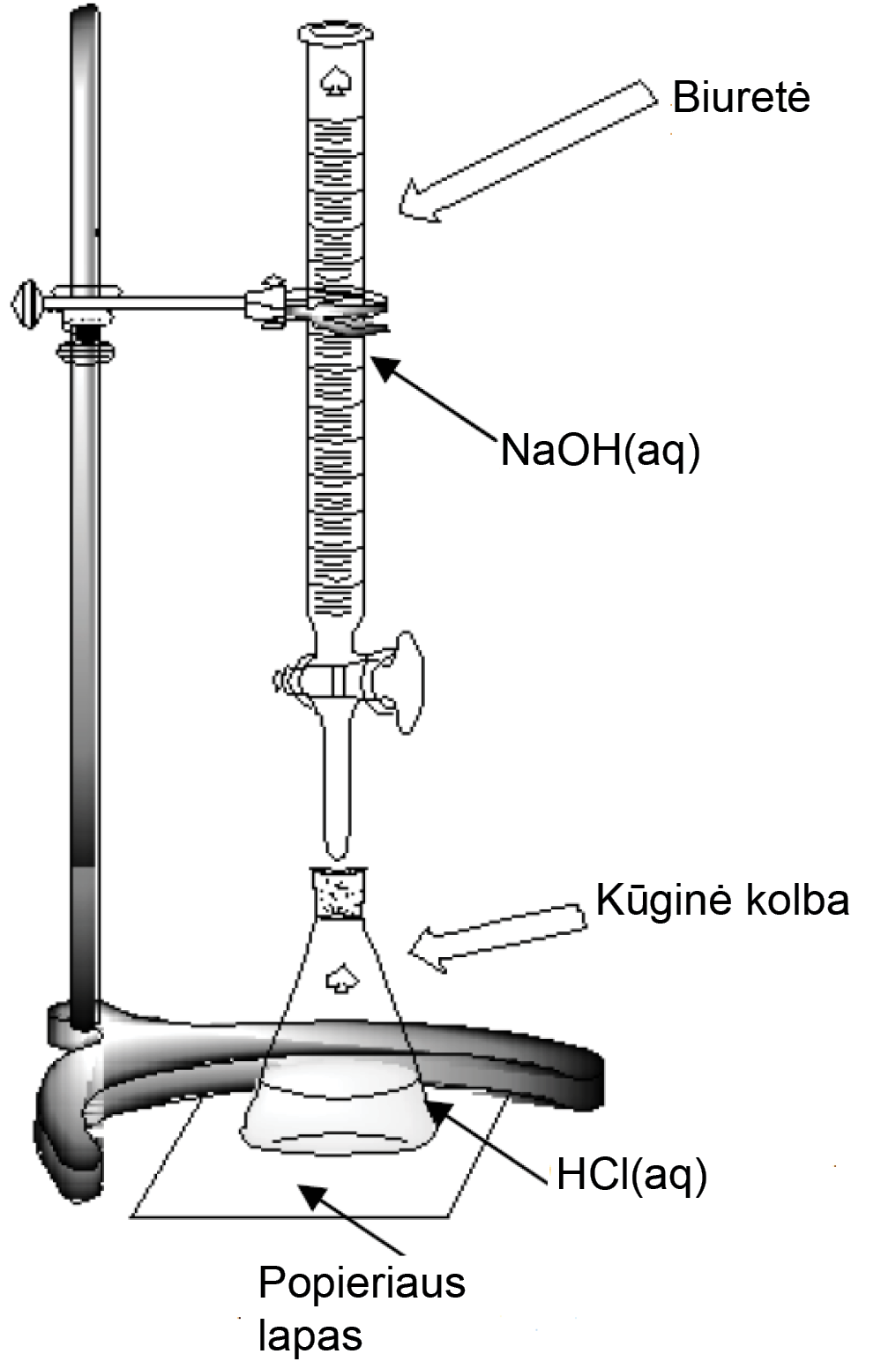
8 pav. HCl(aq) titravimas NaOH tirpalu
Titravimo matavimų tikslumas priklauso nuo daugelio veiksnių: reakciją stebinčio žmogaus regos gebos, vartojamų tirpalų koncentracijos ir kt. HCl titruojant mažesnės koncentracijos NaOH tirpalu (pavyzdžiui ne 0,1 mol/l, bet 0,05 mol/l) titravimo rezultatai būtų tikslesni.
