Teorinė medžiaga
5.2. Tirpalai
5.2.7. pH uždavinių sprendimo pavyzdžiai
1 uždavinys
Nustatyti Na2CO3, KCH3COO, K2SO4 ir NaCl druskų tirpalų apytikrę pH vertę.
Sprendimas
Nurodytos druskos yra gerai tirpūs vandenyje joniniai junginiai. Parašome jų disociacijos lygtis:
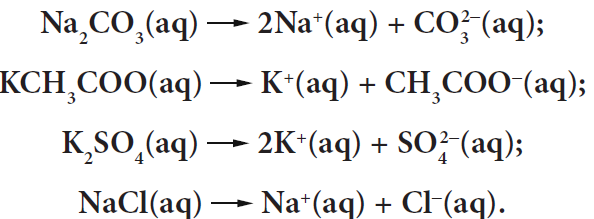
Žinoma, kad silpnųjų rūgščių anijonai hidrolizuojasi*, o stipriųjų rūgščių anijonai nesihidrolizuoja:
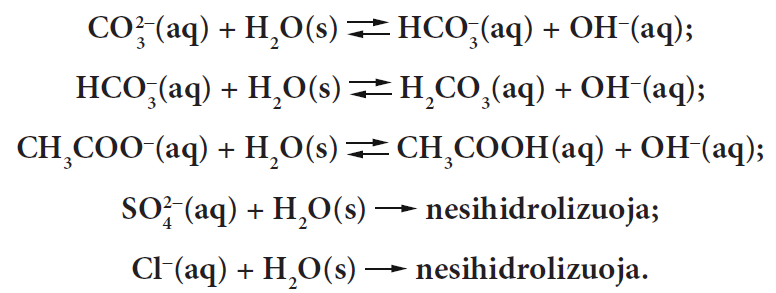
Remdamiesi reakcijų lygtimis, darome išvadą, kad Na2CO3 ir KCH3COO druskų vandeninių tirpalų pH vertė didesnė nei 7, o K2SO4 ir NaCl – pH = ~7
*Hidrolizė – grįžtamoji jonų reakcija su vandeniu
2 uždavinys
Į 200 g 10 % procentų druskos rūgšties tirpalą įpilta 20 g natrio šarmo tirpalo. Kokia gauto tirpalo terpė?
Sprendimas
1. Apskaičiuojame druskos rūgšties molinę koncentraciją:
100 g tirpalo – 10 g HCl
200 g tirpalo – x g
x = 20 g HCl.
2. Apskaičiuojame druskos rūgšties ir natrio šarmo kiekius:
n = m /M(HCl) = 20 g / 36,5 g/mol = 0,548 mol;
n = m / M(NaOH) = 20 g/ 40 g/mol = 0,50 mol.
3. Parašome reakcijos lygtį ir nustatome terpės pobūdį:
1 mol 1 mol
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(s).
0,5 mol 0,5 mol
Gautas rūgšties kiekis yra didesnis nei teoriškai apskaičiuotas (0,548 mol > 0,50 mol), taigi jos yra perteklius. Todėl darome išvadą, kad terpė rūgštinė (pH < 7).
Atsakymas: terpė yra rūgštinė (pH < 7).
3 uždavinys
Apskaičiuokite 0,1 mol/l H2SO4 tirpalo pH.
Sprendimas
Parašykime H2SO4 jonizacijos lygtį, žinodami, kad stiprusis elektrolitas H2SO4 jonizuojasi visiškai (be pakopų) ir susidaro du moliai vandenilio jonų:
H2SO4(aq) ![]() 2H+(aq) + SO42–(aq).
2H+(aq) + SO42–(aq).
1. Iš jonizacijos lygties matyti, kad jonizuojantis H2SO4 susidaro du moliai H+ jonų. Apskaičiuojame vandenilio jonų koncentraciją tirpale:
c(H+) = 0,1 mol/l × 2 = 0,2 mol/l = 2,0 × 10–1 mol/l.
2. Apskaičiuojame 0,1 mol/l H2SO4 tirpalo vandenilio rodiklį:
pH = –lg(2,0 × 10–1) = –(lg 10–1 + lg 2,0) = –(–1 + 0,30) = 0,70.
Vadinasi, šis elektrolitas yra stipriai rūgštus.
Atsakymas: 0,1 mol/l H2SO4 tirpalo pH = 0,70.
4 uždavinys
Viename litre tirpalo ištirpinta 0,56 g kalio šarmo. Apskaičiuokite šio tirpalo pH.
Sprendimas
1. Apskaičiuojame tirpalo molinę koncentraciją:
n = m/M = 0,56 g/l /(56 g/mol × 1l) = 0,01 mol/l.
Kalio šarmo disociacijos lygtis yra tokia:
KOH(aq) → K+(aq) + OH–(aq).
2. Disocijuojant 1 mol KOH susidaro 1 mol OH– jonų. Apskaičiuojame OH– jonų koncentraciją tirpale:
[OH–] = 0,01 mol/l × 1 = 0,01 = 1,0 × 10–2 mol/l.
3. Apskaičiuojame vandenilio jonų koncentraciją 0,01 mol/l KOH:
[H+] = 10–14 / [OH–] = 10–14 mol2/l2 / (1,0 × 10–2 mol/l) = 1,0 × 10–12 mol/l.
4. Apskaičiuojame KOH tirpalo vandenilio rodiklį:
pH = –lg (1,0 × 10–12) = 12.
Vadinasi, šis elektrolitas yra stipriai bazinis.
Atsakymas: KOH tirpalo vandenilio jonų rodiklis pH = 12.
5 uždavinys
Apskaičiuokite kalcio karbonato, kurio tirpumas 20oC vandenyje yra 12 mg/l, tirpalo pH vertę.
Sprendimas
1. Užrašome reakcijos lygtį:
CaCO3(aq) → Ca2+(aq) + CO32–(aq);
CO32–(aq) + H2O(s) ![]() HCO3–(aq) + OH–(aq).
HCO3–(aq) + OH–(aq).
2. Remdamiesi užrašytomis lygtimis darome išvadą:
n(CaCO3) = n(CO32–) = n(OH–) = 12 mg/l / 100000 mg/mol = 1,2 · 10-4 mol/l
[H+] = 10–14 mol2/l2 / 1,2 · 10-4 mol/l = 0,833 · 10-10 mol/l
pH = 10,08
Atsakymas: pH »10,08.
