Teorinė medžiaga
5.2. Tirpalai
5.2.1. Procentinė ir molinė tirpalų koncentracija
Mišinių ir junginių kiekybinė sudėtis nusakoma jų sudedamųjų dalių masės dalimi, kuri reiškiama procentais. Pavyzdžiui, 15 % tirpalas reiškia, kad 100 g šio tirpalo yra 15 gramų ištirpusios medžiagos ir 85 g tirpiklio:
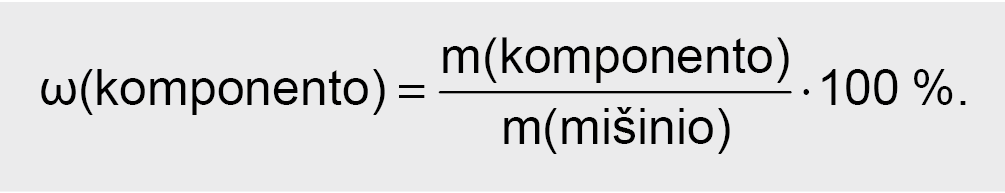
Molinė koncentracija reiškiama ištirpusios medžiagos kiekiu (n) viename litre tirpalo. Molinė koncentracija c matuojama mol/l arba mol/dm3:
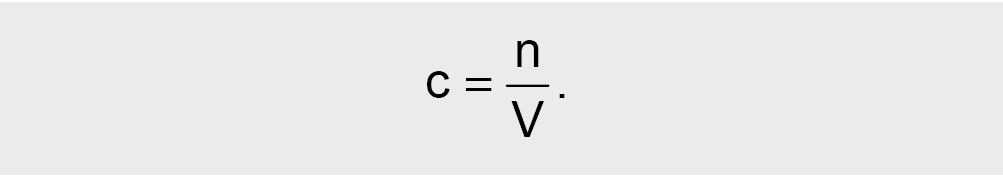
Uždavinių sprendimo pavyzdžiai
1 uždavinys
Praskiedus 800 ml 10 % CuCl2 tirpalo (r = 1,096 g/cm3), pagaminta 3 l tirpalo. Kokia gauto tirpalo molinė koncentracija?
Sprendimas
1. Apskaičiuojame 10 % CuCl2 tirpalo masę:
m(tirpalo) = V × r = 800 ml . 1,096 g/ml = 876,8 g.
2. Apskaičiuojame ištirpusios tirpale druskos masę:
10 g CuCl2 – 100 g tirpalo
x g – 876,8 g
x = 87,68 g CuCl2.
3. Apskaičiuojame tirpale ištirpusios druskos kiekį:
M(CuCl2) = 63,5 + 2 × 35,5 = 134,5 g/mol;
1 mol – 134,5 g
x – 87,68 g
x = 0,652 mol (3-uose litruose).
4. Apskaičiuojame molinę koncentraciją:
0,652 mol – 3 l
x mol – 1 l
x = 0,367 mol.
Atsakymas: 0,217 mol/l.
2 uždavinys
Apskaičiuokite 400 ml 0,2 mol/l Ba(OH)2 tirpalo procentinę koncentraciją, jei tirpalo tankis 1,15 g/ml.
Sprendimas
1. Apskaičiuojame bario hidroksido kiekį, ištirpusį 0,3 l:
1000 ml – 0,2 mol
400 ml – x mol
x = 0,08 mol.
2. Apskaičiuojame 0,08 mol bario hidroksido masę:
n = m/M
m(Ba(OH)2) = n × M = 0,08 mol × 171 g/mol = 13,68 g.
3. Apskaičiuojame 400 ml tirpalo masę:
m = V × r = 400 ml × 1,15 g/ml = 460 g.
4. Apskaičiuojame 400 ml 0,2 mol/l Ba(OH)2 tirpalo procentinę koncentraciją:
460 g tirpalo – 13,68 g Ba(OH)2
100 g tirpalo – y g
x = 2,97 g = 2,97 %.
Atsakymas: 2,97 %.
3 uždavinys
Praleidus vandenilio sulfido dujas pro 174 ml (r = 1,10 g/cm3) vario(II) sulfato tirpalą, iškrito 11,8 g nuosėdų. Apskaičiuokite vario(II) sulfato tirpalo procentinę koncentraciją.
Sprendimas
1. Užrašome ir išlyginame reakcijos lygtį ir pagal ją atliekame skaičiavimus:
CuSO4(aq) + H2S(d) → CuS(k) + H2SO4(aq);
159,5 g CuSO4 – 95,5 g CuS
x g CuSO4 – 11,8 g CuS
x = 19,71 g CuSO4.
2. Apskaičiuojame CuSO4 tirpalo masę:
m(tirpalo) = V × r = 174 ml × 1,10 g/cm3 = 191,4 g.
3. Apskaičiuojame CuSO4 procentinę koncentraciją:
I būdas
Pagal reakcijos lygtį:
191,4 g CuSO4 tirpalo – 19,71 g CuSO4
100 g CuSO4 tirpalo – y g
y = 10,30 g CuSO4 = 10,30 %.
II būdas
ω(CuSO4) = (m(medžiagos)/ m(tirpalo) )· 100 % = (19,71 g /191,4 g) · 100 % = 10,30 %
Atsakymas: 10,01 %.
4 uždavinys
Kokį tūrį 2,8 mol/l koncentracijos H2SO4 tirpalo galima pagaminti, praskiedus 900 ml 75 % H2SO4 tirpalo, kurio tankis 1,669 g/cm3?
Sprendimas
1. Apskaičiuojame pradinio tirpalo, kurio koncentracija yra 75 %, masę:
m = V · d = 900 ml · 1,669 g/ cm3 = 1502,1 g.
Tirpinio (H2SO4) masė šiame tirpale:
75 g H2SO4 – 100 g tirpalo
x g H2SO4 – 1502,1 g tirpalo
x = 1126,6 g H2SO4.
2. Skiedžiant tirpalą, tirpinio masė nekinta, tai ir naujame tirpale yra 1126,6 g H2SO4. Kadangi žinome naujo tirpalo molinę koncentraciją, tai ir tirpinio masę išreiškiame kiekio vienetais. Sieros (sulfato) rūgšties molinė masė:
M(H2SO4) = 2 · 1 + 32 + 4 · 16 = 98 g/mol.
Apskaičiuojame tirpinio kiekį:
1 mol H2SO4 – 98 g
x mol H2SO4 – 1126,6 g
x = 11,5 mol H2SO4.
3. Apskaičiuojame, kokį tūrį 2,8 mol/l H2SO4 tirpalo galima pagaminti iš 11,5 mol sulfato rūgšties:
2,8 mol H2SO4 – 1000 ml tirpalo
11,5 mol H2SO4 – x ml tirpalo
x = 4100 ml
Atsakymas: 4100 ml.
