Teorinė medžiaga su pavyzdžiais
4.2. Cheminė pusiausvyra
4.2.2. Cheminė pusiausvyra ir jos konstanta
Esant grįžtamajai reakcijai ir pusiausvyros būklei, medžiagų koncentracijos nebekinta, nes kiek pradinių medžiagų sureaguoja, tiek jų susidaro vykstant atgalinei reakcijai. Medžiagų koncentracijos, esant pusiausvyros būklei, vadinamos pusiausvyrosiomis koncentracijomis. Užrašome grįžtamąją reakciją schemiškai:
mA + nB sC + pD
Laikome, kad
sistema yra homogeninė. Tuomet tiesioginės ir grįžtamosios reakcijų greičiai
bus: tiesioginei reakcijai vties. = k1[A]m[B]n, o atvirkštinei
reakcijai vatv. = k2[C]s[D]p. Vykstant reakcijai A ir B medžiagų
koncentracijos mažėja, o tai reiškia, kad tiesioginės reakcijos greitis taip
pat mažėja. Kartu didėja susidarančių medžiagų koncentracijos, o tuo pačiu ir
nuo jų priklausantis atvirkštinės reakcijos greitis. Tam tikru momentu abiejų
reakcijų greičiai tampa lygūs, t.y. vties. = vatv.
Cheminio proceso būklė, kai tiesioginės ir atvirkštinės
reakcijų greičiai yra lygūs (2 pav.), o reaguojančių medžiagų ir produktų
koncentracijos nesikeičia (3 pav.) vadinama chemine pusiausvyra.
3 pav. Tiesioginės ir atvirkštinės reakcijų greičių priklausomybė nuo grįžtamosios reakcijos N2O4(d)
2NO2(d) trukmės
4 pav. Reaguojančiosios medžiagos ir
produkto koncentracijų priklausomybė grižtamosios reakcijos N2O4(d)
2NO2(d) trukmės
Taigi, jei vties. = vatv., tai atitinkamai k1[A]m[B]n = k2[C]s[D]p.
Padaliję ši reiškinį iš k2[A]m[B]n gauname:
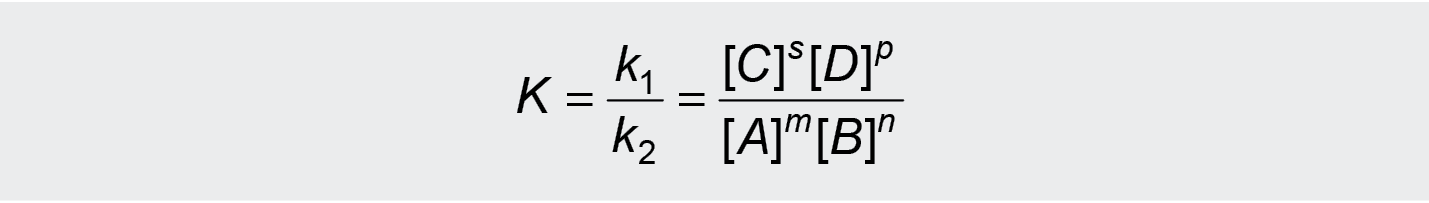
čia K yra cheminės
pusiausvyros konstanta, kai medžiagų koncentracijos išreikštos moliais. Ji
reiškiama dviejų pastovių dydžių k1/k2, arba reakcijos produktų pusiausvyrųjų koncentracijų
ir pradinių medžiagų pusiausvyrųjų koncentracijų sandaugų santykiu. Kuo K
yra didesnė, tuo didesnės reakcijos produktų koncentracijos pusiausvyros metu.
Pusiausvyros konstanta priklauso nuo reaguojančių medžiagų savybių ir
temperatūros, todėl nustatant konstantą reikia nurodyti kokiai temperatūrai ji
yra nustatyta.
Pavyzdys
Apskaičiuokite reakcijos
2CO(d) + O2(d) 2CO2(d)
pusiausvyros konstantą ir pradines SO2 bei O2 koncentracijas, jei pusiausvirosios koncentracijos: [CO] = 4 mol/l, [O2] = 2,5 mol/l, [CO2] = 5 mol/l.
Sprendimas
Apskaičiuojame pusiausvyros konstantą:
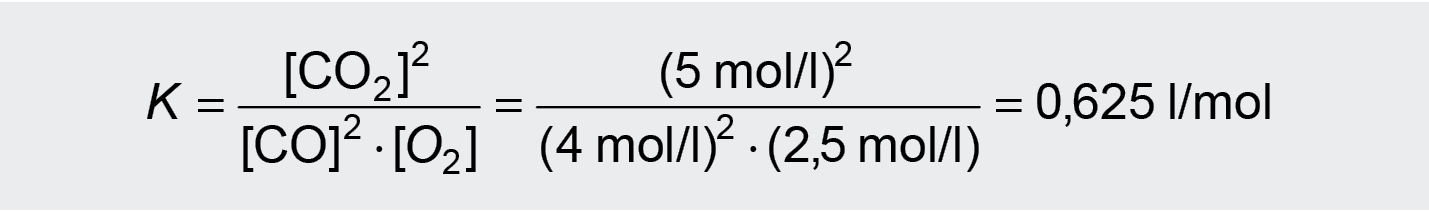
Norint surasti pradinę CO koncentraciją, prie
pusiausvirosios jos koncentracijos reikia pridėti reakcijoje sureagavusiąją CO
koncentraciją:
[CO]prad.= [CO]pus. + [CO]sureag.
Iš reakcijos lygties matyti, kad iš dviejų molių CO
susidarė du moliai CO2. Atitinkamai, penkiems moliams CO2
susidaryti turėjo sureaguoti penki moliai CO. Todėl [CO]prad.= 4 mol/l
+ 5 mol/l = 9 mol/l. Reaguojant vienam deguonies moliui, susidarė du CO2
moliai, t.y. deguonies sunaudojama dvigubai mažiau molių, negu susidaro molių CO2,
todėl [O2]prad.= 4 + (5 : 2) = 6,5 mol/l.
