Teorinė medžiaga su pavyzdžiais
| Svetainė: | KTU atvirieji mokymai |
| Kursas: | ★ CHEMIJA išlyginamieji mokymai |
| Knyga: | Teorinė medžiaga su pavyzdžiais |
| Spausdino: | Svečio paskyra |
| Data: | šeštadienis, 2026 gegužės 30, 14:01 |
Turinys
- 4.1. Cheminė kinetika
- 4.1.1. Homogeninės ir heterogeninės cheminės reakcijos
- 4.1.2. Cheminių reakcijų greitis
- 4.1.3. Veiksniai turintys įtakos reakcijos greičiui
- 4.1.3.1. Dalyvaujančių reakcijoje medžiagų koncentracijų įtaka
- 4.1.3.2. Slėgio įtaka
- 4.1.3.3. Temperatūros įtaka
- 4.1.3.4. Katalizatoriai ir jų įtaka reakcijos greičiui
- 4.2. Cheminė pusiausvyra
- 4.2.1. Grįžtamosios ir negrįžtamosios cheminės reakcijos
- 4.2.2. Cheminė pusiausvyra ir jos konstanta
- 4.2.3. Cheminės pusiauvyros poslinkis ir veiksniai turintys jam įtakos
- 4.2.3.1. Dalyvaujančių reakcijoje medžiagų koncentracijų pokyčio įtaka
- 4.2.3.2. Slėgio pokyčio įtaka
- 4.2.3.3. Temperatūros pokyčio įtaka
4.1. Cheminė kinetika
Cheminė kinetika nagrinėja cheminių reakcijų greitį ir jų mechanizmą. Cheminių reakcijų greitis yra labai skirtingas ir priklauso nuo įvairių veiksnių – reaguojančių medžiagų cheminės prigimties, jų koncentracijos, slėgio, temperatūros, katalizatorių ir inhibitorių. Žinant priklausomybes, cheminių reakcijų greitį galima reguliuoti – reakcijas galima lėtinti arba greitinti.
4.1.1. Homogeninės ir heterogeninės cheminės reakcijos
Cheminės reakcijos skirstomos į homogenines ir heterogenines. Kai reakcijoje dalyvaujančios medžiagos yra vienalytės, t.y. viename agregatiniame būvyje, pvz. dujų mišiniai, skysčių mišiniai, medžiagų tirpalų mišiniai – reakcijos vadinamos homogeninėmis.
H2(d)
+ Cl2(d) 2HCl(d);
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(s);
Jei dalyvaujančios medžiagos sudaro sistemą, kurioje yra
keletas fazių – dalių, atskirtų viena nuo kitos paviršiumi, tai reakcija
vadinama heterogenine.
C(k)
+ O2(d) → CO2(d);
SiO2(k) + 4HF(aq) → SiF4(d) + 2H2O(s);
4.1.2. Cheminių reakcijų greitis
Cheminių reakcijų greitis apibūdinamas reaguojančių medžiagų koncentracijų pokyčiu per laiko vienetą. Koncentracija dažniausiai reiškiama mol/l ir rašoma laužtiniuose skliaustuose [ ] arba žymima raide c, o laikas, priklausomai nuo reakcijos pobūdžio, valandomis, minutėmis, sekundėmis ar kitais laiko vienetais. Taigi, reakcijos greičio išraiška būtų mol/(l·laiko vienetas). Dažniausiai naudojama – mol/(l·s) arba mol·l–1·s–1.
Kuo didesnė medžiagų koncentracija, tuo didesnis šios medžiagos molekulių kiekis tūrio vienete ir tuo daugiau šios molekulės turi galimybių susidurti viena su kita. Tačiau vykstant reakcijai reaguojančių medžiagų molekulių kiekis mažėja, tuo pačiu mažėja jų galimybės susitikti viena su kita ir, tuo pačiu, mažėja reakcijos greitis (1 pav.).
1 pav. Reaguojančios ir susidarančios medžiagų molekulių kiekio kitimas vykstant cheminei reakcijai: A → B
4.1.3. Veiksniai turintys įtakos reakcijos greičiui
Cheminių reakcijų greičiui įtakos turi tokie veiksniai:
- dalyvaujančių reakcijoje medžiagų koncentracijos;
- slėgis (jei viena ar daugiau dalyvaujančių reakcijoje medžiagų yra dujos);
- temperatūra;
- katalizatoriai.
4.1.3.1. Dalyvaujančių reakcijoje medžiagų koncentracijų įtaka
Homogeninėms reakcijoms reaguojančių medžiagų koncentracijų ir reakcijos greičio priklausomybę nusako veikiančiųjų masių dėsnis – cheminės reakcijos greitis, esant pastoviai temperatūrai, tiesiog proporcingas reaguojančių medžiagų koncentracijų sandaugai.
Pvz. reakcijai:
mA + nB → sC + pD
veikiančiųjų masių dėsnis užrašomas taip:
v = k[A]m[B]n
čia v - reakcijos greitis, k – greičio konstanta, kuri priklauso nuo reaguojančių medžiagų savybių ir temperatūros, [A] ir [B] – reaguojančiųjų medžiagų koncentracijos (mol/l), m, n, s ir p – stechiometriniai koeficientai. Jei reaguojančiųjų medžiagų koncentracijos yra lygios 1 mol/l, tai
v = k
Vykstant heterogeninėms reakcijoms medžiagų sąveika vyksta jų sąlyčio vietoje, t.y. fazių paviršiuje. Tai reiškia, kad tokių reakcijų greitis priklauso nuo difuzijos greičio, o pastaroji savo ruožtu nuo sąlyčio ploto, keliant temperatūrą, didinant dujų slėgį, maišant skysčius. Pvz. metalo milteliai greičiau reaguoja su rūgštimis negu metalo gabalas. Taigi, tokioje sistemoje reakcijos greitis priklauso tik nuo miltelių smulkumo, bet nepriklauso nuo metalo koncentracijos. Tai reiškia, kad jei sistemoje yra kietoji, skystoji ir dujinė medžiagos, tai reakcijos greitis priklauso nuo reakcijoje dalyvaujančių skystųjų ir dujinių medžiagų koncentracijų. Taigi jei vyksta reakcija
mA + nB → sC,
kur A kietoji medžiaga, o B ir C dujos, tai pagal veikiančiųjų masių dėsnį heterogeninės reakcijos greitis:
v = k1[A]m[B]n,
kadangi kietosios medžiagos koncentracija pastovi, tai laikydami, kad k = k1[A]m, gauname:
v = k[B]n,
tai reiškia kad heterogeninėms reakcijoms
veikiančiųjų masių dėsnio lygtyje kietųjų medžiagų koncentracijos nenurodomos.
Jų dydis įskaičiuojamas į reakcijos greičio konstantą.
1 pavyzdys
Apskaičiuokite
reakcijos:
2CO(d) + O2(d) 2CO2(d)
greitį, jei reaguojančiųjų medžiagų koncentracijos yra:
[CO] = 4 mol/l; [O2] = 5
mol/l; ![]() .
.
Sprendimas
Pagal
veikiančiųjų masių dėsnį:
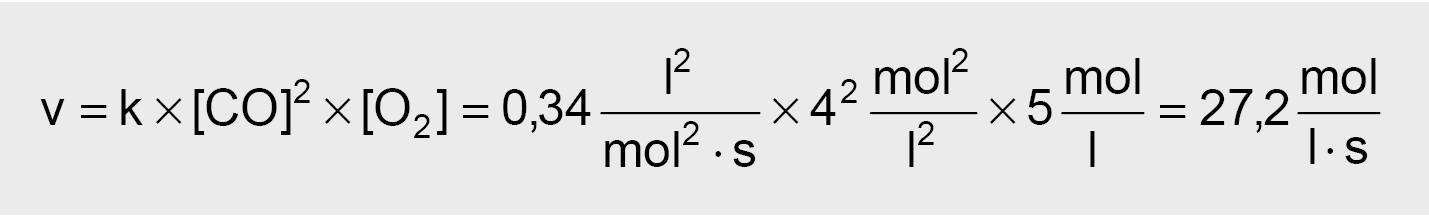
2 pavyzdys
Apskaičiuokite kiek kartų ir kaip pasikeis reakcijos
Al(OH)3 (k) + 3HCl (aq) → AlCl3 (aq) + 3H2O (s)
greitis, jei mišinį praskiesime 3 kartus.
Sprendimas
v1 = k [Al(OH)3]× [HCl]3
v2 = k[1/3Al(OH)3] × [1/3HCl]3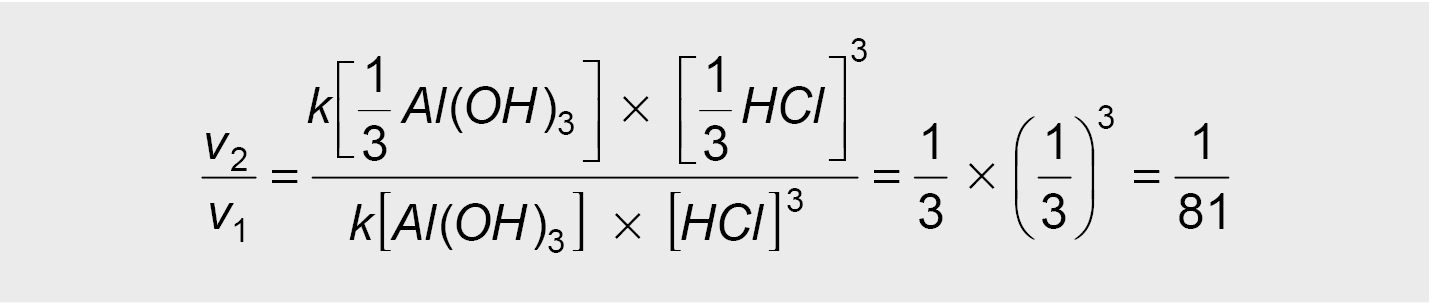
4.1.3.2. Slėgio įtaka
Jei
reaguojančios medžiagos yra dujos, tai reakcijos greitis priklauso nuo slėgio,
nes keičiant slėgį keičiasi sistemos tūris, o tuo pačiu ir reaguojančių
medžiagų koncentracijos, t.y. didinant slėgį mažėja tūris ir didėja medžiagų
koncentracija; slėgį mažinant tūris didėja, o koncentracijos mažėja.
4.1.3.3. Temperatūros įtaka
Ženklios įtakos reakcijos greičiui turi temperatūra. Greičio priklausomybę nuo temperatūros nusako van't Hofo taisyklė – pakėlus temperatūrą 10 ºC, reakcijos greitis padidėja 2-4 kartus. Matematinė šios taisyklės išraiška tokia:
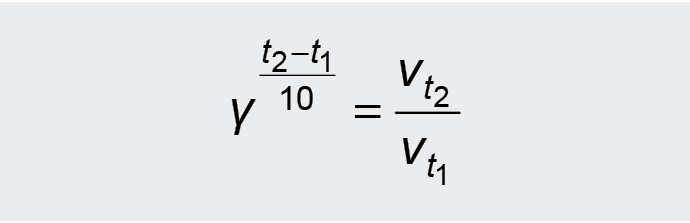
vt2 – reakcijos
greitis, pakėlus temperatūrą iki t2,
vt1 – pradinis reakcijos greitis, esant temperatūrai t1,
γ – temperatūrinis koeficientas parodo kiek kartų padidėja reakcijos greitis pakėlus reaguojančių medžiagų temperatūrą 10 ºC.
Taigi, temperatūra turi žymios įtakos reakcijos greičiui, tačiau šios įtakos negalima paaiškinti vien dėl temperatūros pakėlimo padidėjusiu dalelių judėjimu ir dažnesniu jų susidūrimu. Ne kiekvienas molekulių susidūrimas baigiasi reakcija. Reaguoja tik aktyvios molekulės, kurios turi didesnę kinetinę energiją arba yra sužadintos.
Energija, kuri reikalinga 1 medžiagos molio visoms molekulėms suaktyvinti, vadinama aktyvacijos energija. Didžioji dalis šios energijos suvartojama vidiniams molekuliniams ryšiams suardyti ar susilpninti ir tik nedidelė dalis – dalelių judėjimui paspartinti. Taigi, pakėlus temperatūrą padidėja aktyvių molekulių kiekis, o tuo pačiu žymiai padidėja reakcijos greitis. Aktyvacijos energijos šaltiniu gali būti šilumos, elektros, spinduliavimo ir kitos energijos rūšys.
Taigi, pakilus temperatūrai, padidėja aktyvių molekulių skaičius, o dėl to labai efektingai padidėja ir reakcijos greitis.
Pavyzdys
Apskaičiuokite, kiek kartų padidės reakcijos greitis, pakėlus temperatūrą nuo
30 iki 60 ºC, jei reakcijos temperatūrinis koeficientas γ = 3.
Sprendimas
Panaudojame van’t Hofo taisyklę:
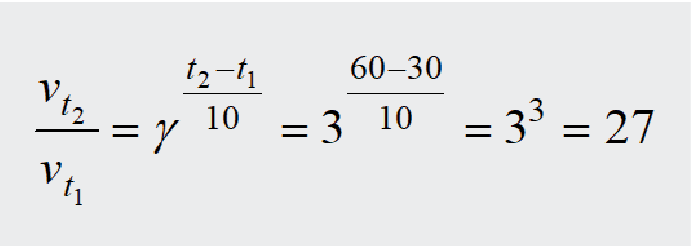
4.1.3.4. Katalizatoriai ir jų įtaka reakcijos greičiui
Katalizė – tai cheminės reakcijos greičio keitimas, naudojant medžiagas, vadinamas katalizatoriais. Reakcijos kurių greitis priklauso nuo katalizatorių, vadinamos katalizinėmis. Katalizatoriai greitina arba lėtina reakcijas. Jie paprastai dalyvauja tik tarpinėse reakcijose, o po cheminės reakcijos išlieka nepakitę.
Katalizatoriai, greitinantys reakcijas, vadinami teigiamaisiais, o lėtinantys – neigiamaisiais arba inhibitoriais.
Dauguma katalizatorių reakcijas pagreitina tūkstančius kartų, nes reakcijai, kurioje dalyvauja katalizatorius, reikia mažesnės aktyvacijos energijos, o kuo aktyvacijos energija mažesnė, tuo reakcijos greitis didesnis. Reikia pažymėti, kad katalizės procesai yra labai paplitę. Dabartiniu metu apie 80 % visų cheminės pramonės procesų yra pagrįsti katalize.
Katalizatorių veikiamas yra labai specifinis - dažnai vienas kuris nors
katalizatorius veikia tik vieną cheminę reakciją, suteikdamas jai tam tikrą
greitį. Pakeitus reakcijai katalizatorių, pasikeičia ne tik reakcijos greitis,
bet gali pasikeisti ir gaunamų produktų sudėtis. Toks katalizatorių veikimas
vadinamas selektyviu.
Katalizė skirstoma į homogeninę ir heterogeninę. Kai reaguojančios medžiagos ir katalizatoriaus fazės
yra vienodos, katalizė vadinama homogenine. Kai katalizatoriaus ir reaguojančių
medžiagų fazės yra skirtingos, katalizė vadinama heterogenine.
Katalizatoriaus veikimas aiškinamas tarpinių reakcijų teorija. Pavyzdžiui,
reakcija vyksta lėtai.
A + B → AB
Įdedama katalizatoriaus K, kuris
su medžiaga A sudaro lengvai reaguojantį tarpinį produktą AK:
A + K → AK.
Tarpinis produktas AK lengvai reaguoja su kita pradine medžiaga B. Susidaro reakcijos produktas AB ir išsiskiria katalizatorius K:
AK + B → AB + K.
Kaip matyti iš reakcijos schemos, katalizatorius lieka chemiškai nepakitęs ir vėl gali dalyvauti reakcijoje. Todėl reakcijoms pagreitinti pakanka nedidelių katalizatoriaus kiekių.
Pašalinės medžiagos, kurios nėra reakcijos katalizatoriai, bet smarkiai
suaktyvina katalizatorių veiklą, vadinamos promotoriais.
Kai kurios medžiagos, nors jų būna labai mažai, mažina katalizatorių aktyvumą. Šios medžiagos vadinamos katalizatorių nuodais.
Medžiagos, kurių nedideli kiekiai labai sulėtina cheminių reakcijų greitį, vadinamos inhibitoriais. Pavyzdžiui, deguonies pėdsakai chloro ir vandenilio dujų mišinyje labai sulėtina HCl susidarymo reakciją.
4.2. Cheminė pusiausvyra
Cheminė pusiausvyra – tai sistemos būsena, kai vykstant grįžtamąjai cheminei reakcijai jos tiesioginės ir atvirkštinės reakcijos greitis yra vienodas. Reaguojančių medžiagų kiekių arba koncentracijų santykis esant cheminės pusiausvyros būsenai nesikeičia ir nusakomas reakcijos pusiausvyros konstanta K. Termodinaminiu požiūriu cheminė pusiausvyra yra stabiliausia būsena.
4.2.1. Grįžtamosios ir negrįžtamosios cheminės reakcijos
Cheminės reakcijos būna negrįžtamosios ir grįžtamosios.
Grįžtamosios reakcijos yra tokios reakcijos, kai reaguojančios medžiagos iki galo nesureaguoja nes reakcijos produktai reaguoja tarpusavyje ar skyla ir vėl susidaro pradinės medžiagos. Kai tiesioginės ir atgalinės reakcijų greičiai susilygina – nusistovi dinaminė cheminė pusiausvyra. Pvz. sintetinant amoniaką, dalis pastarojo skyla vėl susidarant azotui ir vandeniliui:
N2(d) + 3H2(d) 2NH3(d)
2NH3(d) N2(d) + 3H2(d)
CO2 (d) + H2O (s) H2CO3(aq)
Negrįžtamoji reakcija – tai reakcija vykstanti viena kryptimi. Negrįžtamosios reakcijos metu reaguojančios medžiagos pilnai sureaguoja.
Mainų negrįžtamosios reakcijos požymis yra: reaguoja arba susidaro netirpi medžiaga, silpnas elektrolitas, dujos.
Pvz.:
AgNO3 (aq) + KCl(aq) → AgCl(k) + KNO3 (aq)
Ag+(aq) + NO3 –(aq) + K+(aq) + Cl –(aq) → AgCl(k) + K+(aq) +NO3 –(aq)
Ag+(aq) + Cl –(aq) → AgCl(k)
Bendras, bet kurio tipo negrįžtamos reakcijos požymis yra didelis šilumos kiekio išsiskyrimas. Visų degimo reakcijų metu išsiskiria šiluma.
C(k) + O2 (d) → CO2(d) ∆H = -393,5 kJ/mol
Šioje reakcijoje susidaro netirpus sidabro chloridas, ir
galimybė, kad tirpale bus sidabro ir chlorido jonų yra labai maža, o tai savo
ruožtu reiškia, kad atgalinė reakcija nevyksta.

2 pav. A – statinė pusiausvyra, B – dinaminė pusiausvyra
http://www.rakeshkapoor.us/ClassNotes/classnotes.php?notes=Equilibrium_and_elasticity&index=1
http://slideplayer.com/slide/3268383/
4.2.2. Cheminė pusiausvyra ir jos konstanta
Esant grįžtamajai reakcijai ir pusiausvyros būklei, medžiagų koncentracijos nebekinta, nes kiek pradinių medžiagų sureaguoja, tiek jų susidaro vykstant atgalinei reakcijai. Medžiagų koncentracijos, esant pusiausvyros būklei, vadinamos pusiausvyrosiomis koncentracijomis. Užrašome grįžtamąją reakciją schemiškai:
mA + nB sC + pD
Laikome, kad
sistema yra homogeninė. Tuomet tiesioginės ir grįžtamosios reakcijų greičiai
bus: tiesioginei reakcijai vties. = k1[A]m[B]n, o atvirkštinei
reakcijai vatv. = k2[C]s[D]p. Vykstant reakcijai A ir B medžiagų
koncentracijos mažėja, o tai reiškia, kad tiesioginės reakcijos greitis taip
pat mažėja. Kartu didėja susidarančių medžiagų koncentracijos, o tuo pačiu ir
nuo jų priklausantis atvirkštinės reakcijos greitis. Tam tikru momentu abiejų
reakcijų greičiai tampa lygūs, t.y. vties. = vatv.
Cheminio proceso būklė, kai tiesioginės ir atvirkštinės
reakcijų greičiai yra lygūs (2 pav.), o reaguojančių medžiagų ir produktų
koncentracijos nesikeičia (3 pav.) vadinama chemine pusiausvyra.
3 pav. Tiesioginės ir atvirkštinės reakcijų greičių priklausomybė nuo grįžtamosios reakcijos N2O4(d)
2NO2(d) trukmės
4 pav. Reaguojančiosios medžiagos ir
produkto koncentracijų priklausomybė grižtamosios reakcijos N2O4(d)
2NO2(d) trukmės
Taigi, jei vties. = vatv., tai atitinkamai k1[A]m[B]n = k2[C]s[D]p.
Padaliję ši reiškinį iš k2[A]m[B]n gauname:
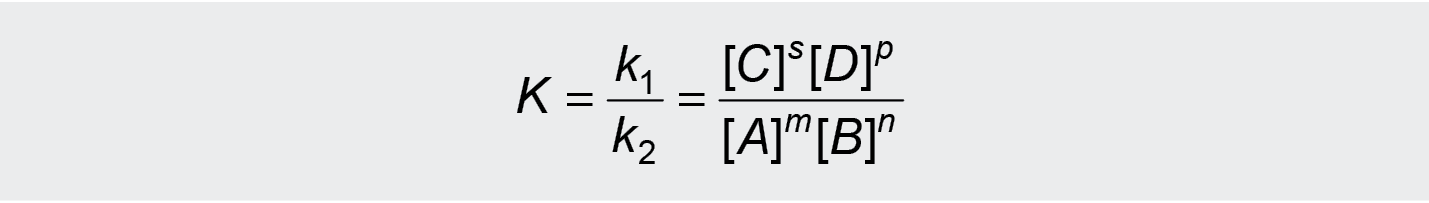
čia K yra cheminės
pusiausvyros konstanta, kai medžiagų koncentracijos išreikštos moliais. Ji
reiškiama dviejų pastovių dydžių k1/k2, arba reakcijos produktų pusiausvyrųjų koncentracijų
ir pradinių medžiagų pusiausvyrųjų koncentracijų sandaugų santykiu. Kuo K
yra didesnė, tuo didesnės reakcijos produktų koncentracijos pusiausvyros metu.
Pusiausvyros konstanta priklauso nuo reaguojančių medžiagų savybių ir
temperatūros, todėl nustatant konstantą reikia nurodyti kokiai temperatūrai ji
yra nustatyta.
Pavyzdys
Apskaičiuokite reakcijos
2CO(d) + O2(d) 2CO2(d)
pusiausvyros konstantą ir pradines SO2 bei O2 koncentracijas, jei pusiausvirosios koncentracijos: [CO] = 4 mol/l, [O2] = 2,5 mol/l, [CO2] = 5 mol/l.
Sprendimas
Apskaičiuojame pusiausvyros konstantą:
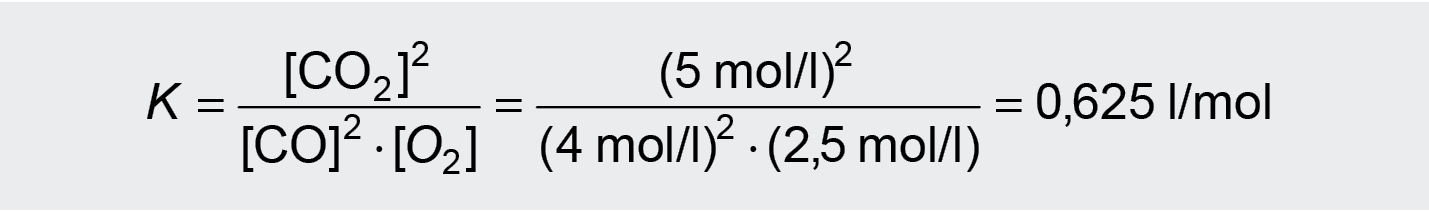
Norint surasti pradinę CO koncentraciją, prie
pusiausvirosios jos koncentracijos reikia pridėti reakcijoje sureagavusiąją CO
koncentraciją:
[CO]prad.= [CO]pus. + [CO]sureag.
Iš reakcijos lygties matyti, kad iš dviejų molių CO
susidarė du moliai CO2. Atitinkamai, penkiems moliams CO2
susidaryti turėjo sureaguoti penki moliai CO. Todėl [CO]prad.= 4 mol/l
+ 5 mol/l = 9 mol/l. Reaguojant vienam deguonies moliui, susidarė du CO2
moliai, t.y. deguonies sunaudojama dvigubai mažiau molių, negu susidaro molių CO2,
todėl [O2]prad.= 4 + (5 : 2) = 6,5 mol/l.
4.2.3. Cheminės pusiauvyros poslinkis ir veiksniai turintys jam įtakos
Esant pusiausvyrai ir pakeitus nors vienos medžiagos koncentraciją, temperatūrą ar slėgį, pakinta ir kitų medžiagų koncentracijos. Tada nusistovi nauja, bet jau kita pusiausvyros būklė, kuri atitinka naujas sąlygas. Tai įvyksta dėl to, kad pasikeitus sąlygoms tiesioginės ir atgalinės reakcijų greičiai pasikeičia nevienodai ir kuri nors reakcija įgauna persvarą. Padidėjus persveriančios reakcijos dėka susidarančių produktų koncentracijoms ir sumažėjus pradinių medžiagų koncentracijoms vėl nusistovi pusiausvyra.
Įvairių veiksnių įtaką pusiausvyrai apibūdina Le Šatelje principas: pakeitus vieną iš
sąlygų – koncentraciją, temperatūrą, slėgį, sistemos cheminė pusiausvyra
pasislenka tos reakcijos kryptimi, kuriai vykstant yra priešinamasi sąlygų
pokyčiui.
4.2.3.1. Dalyvaujančių reakcijoje medžiagų koncentracijų pokyčio įtaka
Medžiagų koncentracijų įtaka cheminei pusiausvyrai, nusakoma taip: padidinus kurios nors medžiagos koncentraciją, cheminė pusiausvyra pasislenka tos reakcijos kryptimi, kuriai vykstant ši medžiaga yra suvartojama arba kuriai vykstant šios medžiagos koncentracija sumažėja, ir, atvirkščiai, sumažinus kurios nors medžiagos koncentracija, pusiausvyra pasislenka tos reakcijos kryptimi, kuriai vykstant šios medžiagos koncentracija padidėja.
N2(d) + 3H2(d) 2NH3(d)
Vykstant šiai reakcijai ir padidinus azoto ir (ar) vandenilio koncentracijas, reakcijos pusiausvyra pasislinks amoniako susidarymo kryptimi, padidinus amoniako koncentraciją - pradinių medžiagų susidarymo kryptimi. Taigi, kad ši reakcija greitai vyktų reikia didinti pradinių medžiagų koncentracijas ir mažinti susidarančio amoniako koncentraciją.
Pavyzdys
Reakcija 2SO2(d) + O2(d) 2SO3(d), ΔHr0 = –197,8 kJ; yra pusiausvyroje. Kokiais koncentracijų pokyčiais galima pasiekti, kad susidarytų daugiau produktų,
tai yra pusiausvyra pasislinktų į dešinę pusę (tiesioginės reakcijos kryptimi).
Sprendimas
Didinant
reaguojančiųjų medžiagų koncentracijas, pusiausvyra pasislenka produkto
susidarymo kryptimi. Todėl aukščiau užrašytoje sieros trioksido (produkto)
išeigą galima padidinti didinant reaguojančiųjų medžiagų, t.y. deguonies, o
ypač – sieros dioksido, koncentracijas. Mažinant produkto koncentraciją
(šalinant jį iš reakcijos mišinio), pusiausvyra taip pat pasislenka produkto
susidarymo kryptimi.
4.2.3.2. Slėgio pokyčio įtaka
Nuo slėgio priklauso tik dujinių medžiagų reakcijos pusiausvyra. Priklausomybė tokia – didinant slėgį reakcijos pusiausvyra pasislenka tos reakcijos kryptimi, kuriai vykstant susidaro mažesnis dujinių molekulių kiekis ir, atvirkščiai, mažinant slėgį – kryptimi, kur susidaro didesnis dujinių molekulių kiekis. Jei kaip pvz. paimsime amoniako sintezės reakciją, tai didinant slėgi reakcijos pusiausvyra pasislinks amoniako susidarymo kryptimi, o mažinant – amoniako skilimo į pradinius produktus, kryptimi. Jei vyksta reakcija, kur pradinių ir susidariusių medžiagų molekulių kiekis vienodas, tai tokios reakcijos pusiausvyrai slėgis įtakos neturės.
Pavyzdys
Reakcija 2SO2(d) + O2(d) 2SO3(d), ΔHr0 = –197,8 kJ; yra pusiausvyroje. Kokiais slėgio pokyčiais galima pasiekti, kad susidarytų daugiau produktų,
tai yra pusiausvyra pasislinktų į dešinę pusę (tiesioginės reakcijos kryptimi).
Sprendimas
Slėgis įtakos
turi tik dujinėms medžiagoms. Didinant slėgį cheminė pusiausvyra pasislenka į
tą pusę, kurioje susidaro mažiau dujinių medžiagų molekulių ir sumažėja slėgis.
Taigi, didinant slėgį, aukščiau užrašytoje sistemoje susidarys daugiau sieros
trioksido, nes kairėje reakcijos pusėje yra 3 moliai dujų, o dešinėje – tik 2 moliai dujų.
4.2.3.3. Temperatūros pokyčio įtaka
Temperatūros įtaką pusiausvyrai nusako van't Hofo dėsnis: keliant pusiausvyroje esančios sistemos temperatūrą, intensyviau ima vykti endoterminė reakcija, ir atvirkščiai, žeminant temperatūrą – egzoterminė reakcija. Pvz. reakcijoje
N2(d) + 3H2(d) 2NH3(d), ΔHro = –92 kJ,
keliant temperatūrą reakciją pasislinks amoniako skilimo į pradines medžiagas kryptimi, ir atvirkščiai – žeminant – amoniako susidarymo kryptimi.
Pavyzdys
Reakcija 2SO2(d) + O2(d) 2SO3(d), ΔHr0 = –197,8 kJ; yra pusiausvyroje. Kokiais temperatūros pokyčiais galima pasiekti, kad susidarytų daugiau produkto,
tai yra pusiausvyra pasislinktų į dešinę pusę – tiesioginės reakcijos kryptimi.
Sprendimas
Neigiama
reakcijos entalpijos pokyčio vertė parodo, kad tiesioginė reakcija yra
egzoterminė. Taigi siekiant, kad tiesioginė reakcija vyktų dar intensyviau,
išsiskiriančią šiluminę energiją reikia šalinti (sistemos temperatūrą reikia
žeminti), tuomet susidarys daugiau produkto.