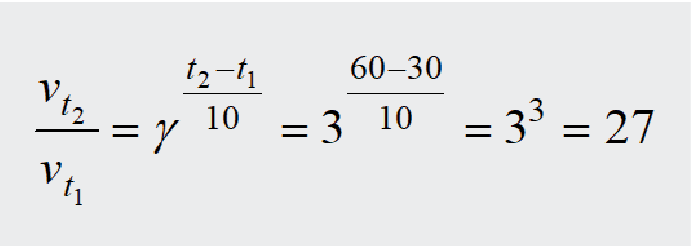Teorinė medžiaga su pavyzdžiais
4.1. Cheminė kinetika
4.1.3.3. Temperatūros įtaka
Ženklios įtakos reakcijos greičiui turi temperatūra. Greičio priklausomybę nuo temperatūros nusako van't Hofo taisyklė – pakėlus temperatūrą 10 ºC, reakcijos greitis padidėja 2-4 kartus. Matematinė šios taisyklės išraiška tokia:
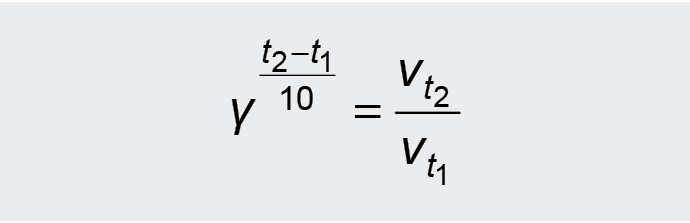
vt2 – reakcijos
greitis, pakėlus temperatūrą iki t2,
vt1 – pradinis reakcijos greitis, esant temperatūrai t1,
γ – temperatūrinis koeficientas parodo kiek kartų padidėja reakcijos greitis pakėlus reaguojančių medžiagų temperatūrą 10 ºC.
Taigi, temperatūra turi žymios įtakos reakcijos greičiui, tačiau šios įtakos negalima paaiškinti vien dėl temperatūros pakėlimo padidėjusiu dalelių judėjimu ir dažnesniu jų susidūrimu. Ne kiekvienas molekulių susidūrimas baigiasi reakcija. Reaguoja tik aktyvios molekulės, kurios turi didesnę kinetinę energiją arba yra sužadintos.
Energija, kuri reikalinga 1 medžiagos molio visoms molekulėms suaktyvinti, vadinama aktyvacijos energija. Didžioji dalis šios energijos suvartojama vidiniams molekuliniams ryšiams suardyti ar susilpninti ir tik nedidelė dalis – dalelių judėjimui paspartinti. Taigi, pakėlus temperatūrą padidėja aktyvių molekulių kiekis, o tuo pačiu žymiai padidėja reakcijos greitis. Aktyvacijos energijos šaltiniu gali būti šilumos, elektros, spinduliavimo ir kitos energijos rūšys.
Taigi, pakilus temperatūrai, padidėja aktyvių molekulių skaičius, o dėl to labai efektingai padidėja ir reakcijos greitis.
Pavyzdys
Apskaičiuokite, kiek kartų padidės reakcijos greitis, pakėlus temperatūrą nuo
30 iki 60 ºC, jei reakcijos temperatūrinis koeficientas γ = 3.
Sprendimas
Panaudojame van’t Hofo taisyklę: