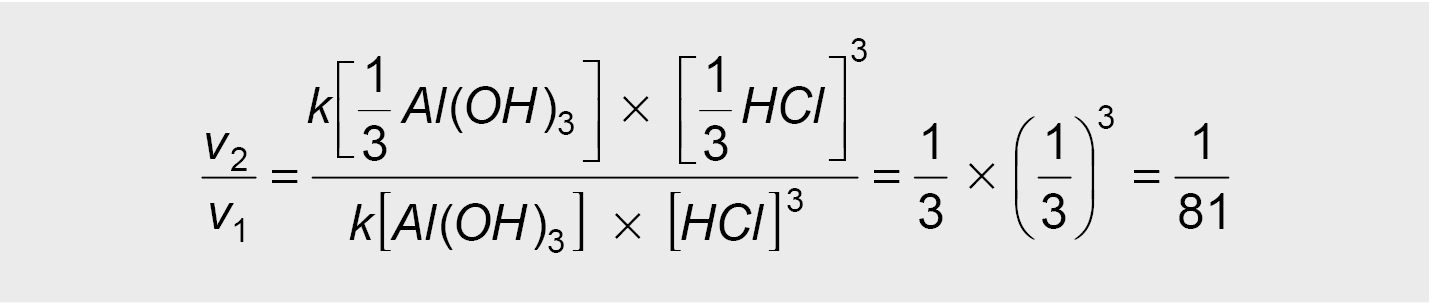Teorinė medžiaga su pavyzdžiais
4.1. Cheminė kinetika
4.1.3.1. Dalyvaujančių reakcijoje medžiagų koncentracijų įtaka
Homogeninėms reakcijoms reaguojančių medžiagų koncentracijų ir reakcijos greičio priklausomybę nusako veikiančiųjų masių dėsnis – cheminės reakcijos greitis, esant pastoviai temperatūrai, tiesiog proporcingas reaguojančių medžiagų koncentracijų sandaugai.
Pvz. reakcijai:
mA + nB → sC + pD
veikiančiųjų masių dėsnis užrašomas taip:
v = k[A]m[B]n
čia v - reakcijos greitis, k – greičio konstanta, kuri priklauso nuo reaguojančių medžiagų savybių ir temperatūros, [A] ir [B] – reaguojančiųjų medžiagų koncentracijos (mol/l), m, n, s ir p – stechiometriniai koeficientai. Jei reaguojančiųjų medžiagų koncentracijos yra lygios 1 mol/l, tai
v = k
Vykstant heterogeninėms reakcijoms medžiagų sąveika vyksta jų sąlyčio vietoje, t.y. fazių paviršiuje. Tai reiškia, kad tokių reakcijų greitis priklauso nuo difuzijos greičio, o pastaroji savo ruožtu nuo sąlyčio ploto, keliant temperatūrą, didinant dujų slėgį, maišant skysčius. Pvz. metalo milteliai greičiau reaguoja su rūgštimis negu metalo gabalas. Taigi, tokioje sistemoje reakcijos greitis priklauso tik nuo miltelių smulkumo, bet nepriklauso nuo metalo koncentracijos. Tai reiškia, kad jei sistemoje yra kietoji, skystoji ir dujinė medžiagos, tai reakcijos greitis priklauso nuo reakcijoje dalyvaujančių skystųjų ir dujinių medžiagų koncentracijų. Taigi jei vyksta reakcija
mA + nB → sC,
kur A kietoji medžiaga, o B ir C dujos, tai pagal veikiančiųjų masių dėsnį heterogeninės reakcijos greitis:
v = k1[A]m[B]n,
kadangi kietosios medžiagos koncentracija pastovi, tai laikydami, kad k = k1[A]m, gauname:
v = k[B]n,
tai reiškia kad heterogeninėms reakcijoms
veikiančiųjų masių dėsnio lygtyje kietųjų medžiagų koncentracijos nenurodomos.
Jų dydis įskaičiuojamas į reakcijos greičio konstantą.
1 pavyzdys
Apskaičiuokite
reakcijos:
2CO(d) + O2(d) 2CO2(d)
greitį, jei reaguojančiųjų medžiagų koncentracijos yra:
[CO] = 4 mol/l; [O2] = 5
mol/l; ![]() .
.
Sprendimas
Pagal
veikiančiųjų masių dėsnį:
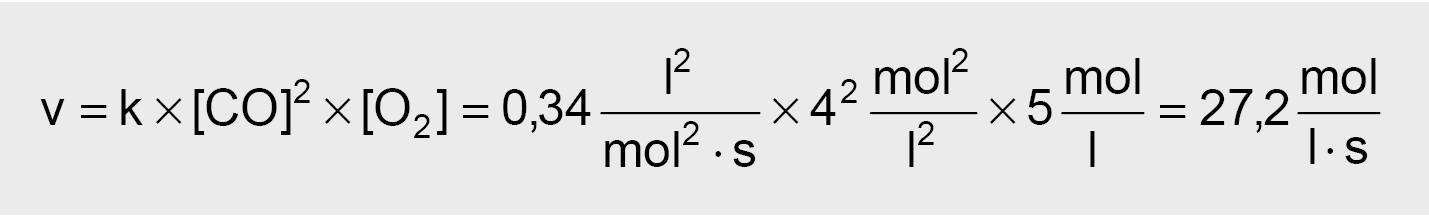
2 pavyzdys
Apskaičiuokite kiek kartų ir kaip pasikeis reakcijos
Al(OH)3 (k) + 3HCl (aq) → AlCl3 (aq) + 3H2O (s)
greitis, jei mišinį praskiesime 3 kartus.
Sprendimas
v1 = k [Al(OH)3]× [HCl]3
v2 = k[1/3Al(OH)3] × [1/3HCl]3