Teorinė medžiaga su pavyzdžiais
3.5. Skaičiavimai pagal reakcijų lygtis
1. Kiek gramų NaOH reikia paimti, kad pilnai sureaguotų 40 gramų FeCl3?
● Parašome ir išlyginame reakcijos lygtį:
3NaOH + FeCl3 →3NaCl + Fe(OH)3
● Virš reakcijos lygties surašome ką turime ir ką reikia rasti:
![]()
● Po reakcijos lygtimi parašome kokiais molių kiekiais reaguoja medžiagos pagal reakcijos lygtį:

● Tada suskaičiuojame molines mases NaOH ir FeCl3:
M(NaOH) = 23 + 16 + 1 = 40g/mol
M(FeCl3) = 56 + 35,5 x 3 = 162,5 g/mol
I būdas:
m = n x M
m(NaOH) = 3 mol x 40 g/mol = 120 g
m(FeCl3) = 1 mol x 162,5 g/mol = 162,5 g
● Statome proporciją:X g NaOH – 40 g FeCl3
120 g NaOH – 162,5 g FeCl3
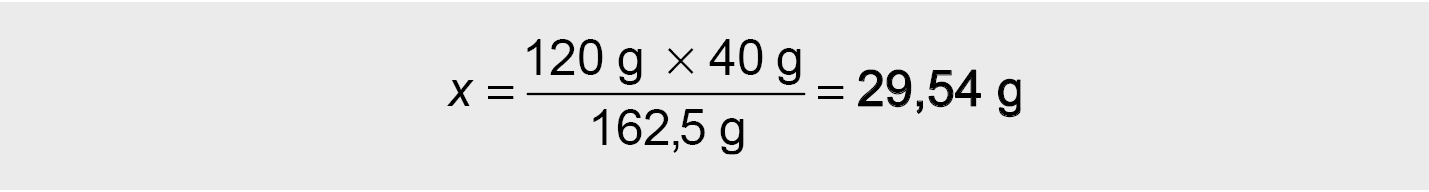
II būdas:

● Parašome reakcijos lygtį ir virš lygties surašome kas duota ir ką reikia rasti moliais:

● Statome proporciją:
X mol NaOH – 0,246 mol FeCl3
3 mol NaOH – 1 mol FeCl3
● Suskaičiuojame masę:
m = n x M = 0,738 mol x 40 g/mol = 29,52 g
2. Kiek gramų neutraliosios druskos susidarys reaguojant 125 ml 16 % ( d=1,109 g/cm3) sulfatinės rūgšties su 200 ml 0,5 mol/l kalio šarmo.
● Rašome reakcijos lygtį:
H2SO4 + KOH → K2SO4 + H2O
● Tada išlyginame reakcijos lygtį:
H2SO4 + 2KOH → K2SO4 + 2H2O
● Tada virš lygties surašome kas yra duota ir ką reikia rasti:
![]()
● Po reakcijos lygtimi surašome kokiais molių ir gramų kiekiais reaguoja medžiagos:
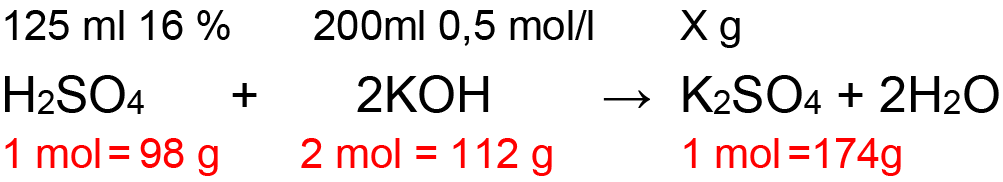
● Suskaičiuojame medžiagų molines mases:
M(H2SO4) = 1 x 2 +32 x 1+16 x 4 = 98 g/mol
M(KOH) = 39 x 1 +16 x 1 + 1 x 1 = 56 g/mol
M(K2SO4) = 39 x 2 + 32 x 1 + 16 x 4 = 174 g/mol
● Žinome kiek paimta H2SO4 tirpalo. Reikia perskaičiuoti kiek grynos sieros rūgšties paimta. Pirmiausia suskaičiuojame masę tirpalo:
m = V x d = 125 ml x 1,109 g/ml = 138,625 g
● Tada skaičiuojame proporciją kiek grynos medžiagos:
100 g tirpalo yra 16 g H2SO4
138,625 g tirpalo – x g H2SO4
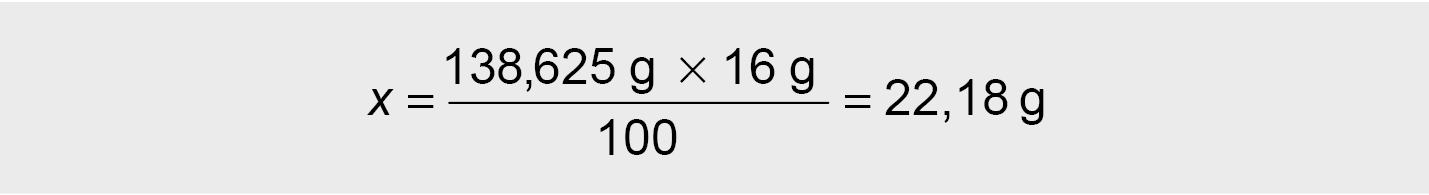
● Arba grynos medžiagos masę galime surasti iš formulės:

● Išsivedam m(medžiagos) kam lygi:
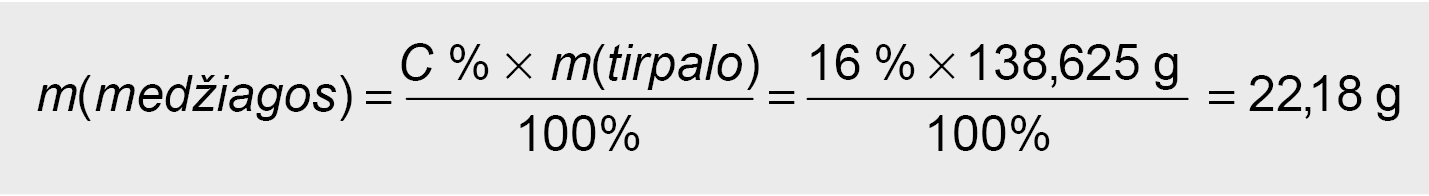
● Apskaičiuojame kiek gryno KOH turime:
n = CM x V = 0,5 mol/l x 0,2 l = 0,1 mol
m = n x M = 0,1 mol x 56 g/mol = 5,6 g
● Vieną iš medžiagų pažymime X, ir patikriname, kurios medžiagos yra perteklius. Sakykime pasirinkome X H2SO4:
X g H2SO4 – 5,6 g KOH
98 g H2SO4 – 112 g KOH
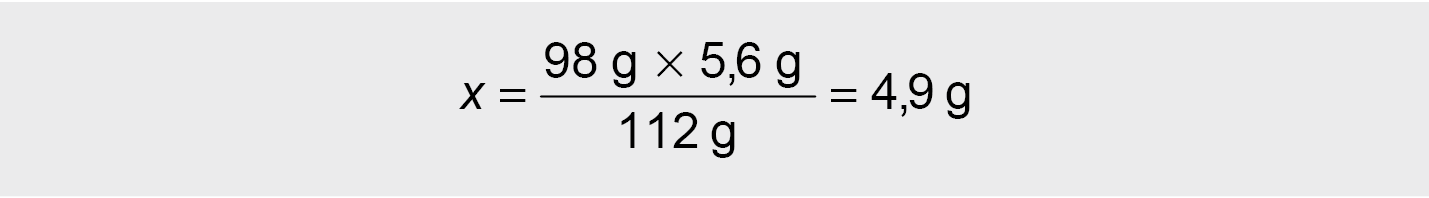
● Mums reikia 4,9 g, o turime 22,18 g. Tai reiškia, kad H2SO4 turime perteklių ir kiek susidarė druskos skaičiuosime pagal KOH.
5,6 g KOH – x g K2SO4
112 g KOH – 174 g K2SO4
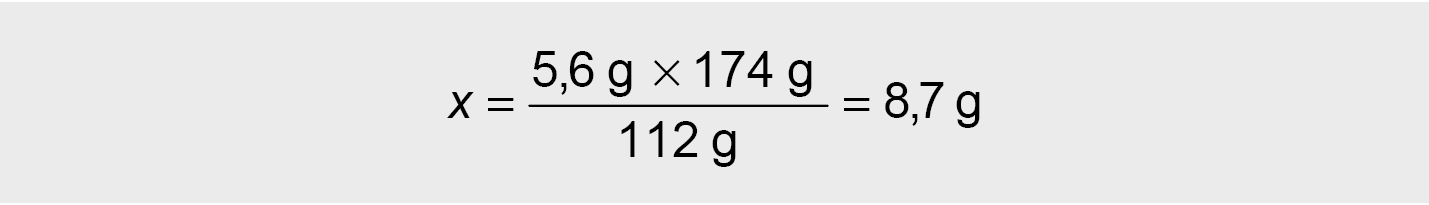
Ats.: Susidarys 8,7 g K2SO4
3. Koks dujų tūris išsiskirs reaguojant 300 g 25 % druskos rūgšties tirpalo su CaCO3?
● Parašome reakcijos lygtį:
2HCl(aq) + CaCO3 (k) → CaCl2(aq) + H2O(s) + CO2(d)
● Virš reakcijos lygties surašome kas duota ir ką reikia rasti, po reakcijos lygtimi, kokiais molių kiekiais reaguoja:
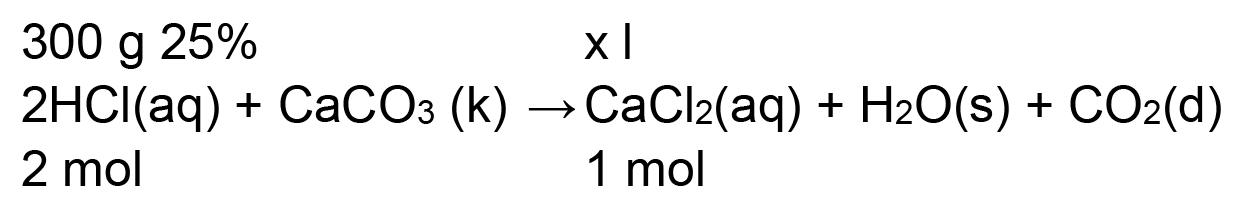
● Suskaičiuojame kiek grynos HCl turime:
100 g tirpalo yra 25 g HCl
300 g tirpalo yra x g HCl
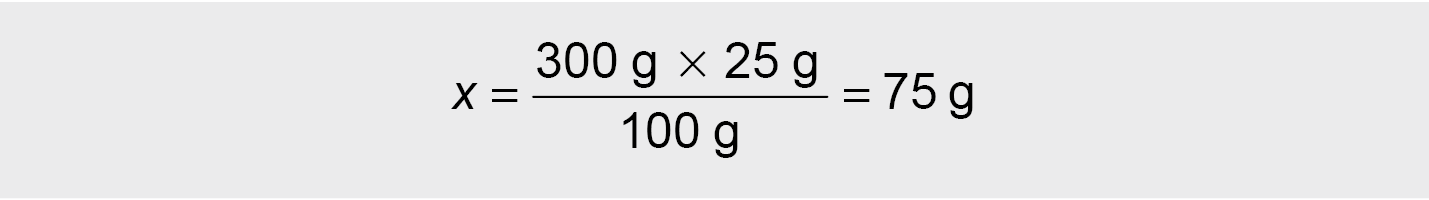
● Arba grynos medžiagos masę galime surasti iš formulės:

● Išsivedam m(medžiagos) kam lygi:

● Skaičiuojame molinę masę:
M(HCl) = 1 + 35,5 = 36,5 g/mol
● Masę perskaičiuojame moliais:

● Tada statome vėl proporciją pagal reakcijos lygtį:
2,05 mol HCl reaguoja ir susidaro x mol CO2
2 mol HCl – 1 mol CO2
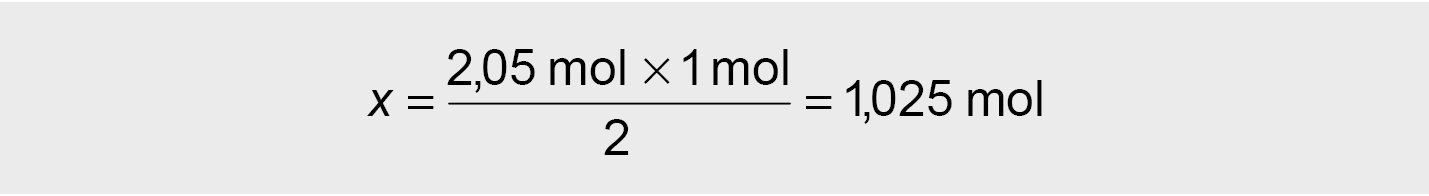
● Molius perskaičiuojame litrais:
V = VM x n = 22,4 l/mol x 1,025 mol = 22,96 l
Ats.: Išsiskirs 22,96 l CO2 dujų.
