Teorinė medžiaga su pavyzdžiais
| Tipărit de: | Utilizator vizitator |
| Dată: | sâmbătă, 30 mai 2026, 14:00 |
3.1. Pagrindiniai cheminių reakcijų tipai
Cheminė reakcija – tai procesas, kai vienos medžiagos virsta kitomis. Cheminė reakcija (cheminis procesas arba virsmas) aprašomas reakcijos lygtimi. Cheminė lygtis tai cheminė reakcija užrašyta cheminėmis formulėmis.
Pavyzdžiui: medžiaga A reaguoja su medžiaga B ir susidaro medžiaga C ir D. Prie kiekvienos medžiagos skliausteliuose rašome agregatinę būseną. Kieta medžiaga – (k), tirpalas – (aq), skystis – (s), dujos – (d). Tai cheminė lygtis užrašoma taip:
A (aq) + B (aq) → C (k) + D (s).
Cheminių reakcijų tipai yra:
1. Jungimosi reakcijos;
2. Skilimo reakcijos;
3. Mainų reakcijos;
4. Pavadavimo reakcijos.
3.1.1. Jungimosi reakcijos
Jungimosi reakcija – tai reakcija, kuriai vykstant iš dviejų ar daugiau skirtingų vieninių ar sudėtinių medžiagų susidaro viena sudėtinė medžiaga.
A+B → AB
2Fe(k) + O2(d) → 2FeO(k)
C(k) + O2(d) → CO2(d)
HCl(aq) + NH3(d) → NH4 Cl (k)
3.1.2. Skilimo reakcijos
Skilimo reakcija – tai reakcija kurios metu iš vienos sudėtinės medžiagos susidaro dvi ar daugiau medžiagų.
A → B + C + D
CaCO3(k) ![]() CaO(k) + CO2(d);
CaO(k) + CO2(d);
2H2O2(s) → 2H2O(s) + O2(d);
Cu(OH)2(k) → CuO(k) + H2O(s).
3.1.3. Mainų reakcijos
Mainų reakcija – reakcija, tarp dviejų sudėtinių medžiagų, kurios vykstant reakcijai pasikeičia sudedamosiomis dalimis.
AB + CD → CB + AD
Dažniausiai pasitaikančios mainų reakcijos yra jonų mainų reakcijos tirpaluose:
BaCl2(aq) + 2AgNO3(aq)→ 2AgCl(k) + Ba(NO3)2(aq);
CaCO3(k) + 2HCl(aq) → CaCl2(aq) + H2CO3(aq) ;
Al(NO3)3(aq) + 3NaOH(aq) →3NaNO3(aq)+ Al(OH)3(k)
Jei jonų mainų reakcijos metu nesiskiria dujos, nesusidaro silpnieji elektrolitai (pvz. H2O, silpnoji rūgštis arba bazė) ar reakcijos produktai neiškrenta nuosėdomis, sakoma, kad jonų mainų reakcija nevyksta.
KNO3(aq) + Na2SO4(aq) → nevyksta;
H2SO4(aq) + KCl(aq) → nevyksta
3.1.4. Pavadavimo reakcijos
Pavadavimo reakcija – tai reakcija, vykstanti tarp vieninės ir sudėtinės medžiagos, kai vieninės medžiagos atomai pakeičia vieno iš sudėtinės medžiagos elementų atomus.
Fe(k) + 2HCl(aq) → FeCl2(aq)+ H2(d)
Fe (k) + CuSO4 (aq) → FeSO4(aq) + Cu(aq)
Cu(k) + 2 AgNO3(aq) → 2Ag(k) + Cu(NO3)2(aq)
3.2. Cheminių reakcijų skirstymas pagal medžiagų savybių pokyčius
Pagal reakcijų metu vykstančius medžiagų savybių pokyčius bei kitus stebimus reiškinius jos skirstomos į:
1) neutralizacijos reakcijas;
2) oksidacijos-redukcijos reakcijas;
3) termochemines reakcijas.
3.2.1. Neutralizacijos reakcijos
Viena iš mainų reakcijų yra neutralizacijos reakcija. Neutralizacijos reakcija, tai reakcija, kuri vyksta tarp bazinės ir rūgštinės prigimties medžiagų. Neutralizacijos metu dažniausia susidaro druska ir vanduo.
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(s);
CuO (k) + H2SO4(aq) → CuSO4(aq) + H2O(s);
Ca(OH)2(aq) + CO2(d) → CaCO3(k) + H2O(s).
Labai svarbu yra tai, kad vykstant mainų reakcijai reaguojančiuose ir susidarančiuose junginiuose esančių to paties elemento atomų oksidacijos laipsnis nekinta.
3.2.2. Oksidacijos – redukcijos reakcijos
Reakcijos kurioms vykstant vienas elementas atiduoda elekronus, o kitas – prisijungia elektronus yra vadinamos oksidacijos – redukcijos reakcijomis.
Jungimosi, skilimo ir pavadavimo reakcijos gali būti priskiriamos prie oksidacijos – redukcijos reakcijų.
Oksidatorius – atomas, jonas ar molekulė, prisijungianti elektronus. Svarbiausi oksidatoriai:
1) vieninės medžiagos, kurių atomų elektrinis neigiamumas yra didelis. Tai ViA ir VIIA grupių elementai(Br2, O2, Cl2);
2) sudėtiniai anijonai, kurių elementas turi didžiausią ar didelį teigiamąjį oksidacijos laipsnį (MnO4−, CrO42−,SO42-, ClO−)
3) Katijonai, kurių oksidacijos laipsnis yra didelis arba didžiausias ( Fe3+, Sn4+, Pb4+)
4) Metalų peroksidai (BaO2, Na2O2, K2O2)
Reduktorius – atomas, jonas ar molekulė, atiduodanti elektronus. Svarbiausi reduktoriai yra:
1) elementai, kurių atomų elektrinis neigiamumas yra labai mažas ( IA ir IIA grupių elementai);
2) paprastieji anijonai ( Br-, S2-, Cl-);
3) sudėtiniai anijonai, kurių elementas turi nedidelį teigiamą oksidacijos laipsnį ( SO32-, NO2-; CrO2-);
4) katijonai, kurių oksidacijos laipsnis yra mažas ir gali padidėti ( Sn2+, Fe2+; Pb2+);
5) kai kurios medžiagos aukštoje temperatūroje (H2, C, CO)
Nustatant oksidatorius ir reduktorius galime taikyti žodį-akronimą OPERA:
O – oksidatorius
P – prisijungia
E – elektronus
R – reduktorius
A – atiduoda
Oksidacijos – redukcijos reakcijos lyginamos elektronų balanso metodu.
3.2.3. Termocheminės reakcijos
Termocheminė lygtis – cheminė lygtis, kurioje nurodytas šiluminis reakcijos efektas. Bet kurio kuro degimas yra termocheminė reakcija.
Pagal šiluminį efektą reakcijos skirstomos į egzotermines ir endotermines.
Egzoterminės reakcijos – tai reakcijos, kurioms vykstant išsiskiria šiluma, o endoterminėms reakcijoms vykstant yra sunaudojama šiluma.
Pvz.:2H2(d) + O2 (d) → 2H2O(s) ∆H=-285,83 kJ/mol
C8H18(s) + O2 (d) → CO2(d) + 2H2O(s) ∆H= -5468 kJ/mol
C(k) + O2 (d) → CO2(d) ∆H=-393,5 kJ/mol
3.3. Organinių medžiagų reakcijų pagrindiniai tipai.
Organinių medžiagų reakcijos klasifikuojamos:
- Prijungimo reakcija – reakcija, kuriai vykstant kelios molekulės susijungia į vieną molekulę. Prijungimo reakcijoms taikoma Markovnikovo taisyklė, kuri sako: jungiantis HX molekulei prie alkeno, H atomas jungsis prie labiausiai hidrinto anglies atomo.
Prijungimo reakcijos, kuriose prijungiamas H2, vadinamos hidrinimo reakcijomis, o kuriose prijungiamas H2O – hidratacijos reakcijomis. - Eliminavimo reakcija, atskėlimo reakcija – atomų grupės atskėlimas nuo molekulės. Eliminavimo reakcijos, kai atskeliamas H2O, vadinamos dehidratacijos reakcijomis, o kai H2 – dehidrinimo reakcijomis.
- Pakaitų reakcija tai reakcija, kuriai vykstant, atomą ar atomų grupę molekulėje pakeičia kitas atomas ar atomų grupė.
- Persigrupavimas – reakcija, kuriai vykstant prisijungimo vietoje atsiduria vandenilio atomas, alkilpakaitalas ar kita grupė. Persigrupavimas tai virtimas kitu junginiu ar izomeru.
- Oksidacijos – redukcijos reakcijos – reakcijos, kuriose vienas elementas elektronus atiduodsa, o kitas pasiima. Organinėje chemijoje organinių junginių oksidacija siejama su deguonies masės dalies organinėje medžiagoje padidėjimu, arba C-O ryšių skaičiaus padidėjimu. Organinių junginių redukcija siejama su vandenilio masės dalies organinėje medžiagoje padidėjimu, arba C-O ryšių skaičiaus sumažėjimu.
3.4. Reakcijų lygčių lyginimas
Mainų reakcijų (kai elementai nekeičia oksidacijos laipsnio) lygčių lyginimas.
- Parašome reakcijos lygtį.
- Lyginimą pradedame nuo didžiausią krūvį turinčio jono ir kur jo yra daugiau.
- Prieš reakciją ir po reakcijos turi būti vienodas atomų skaičius.
Jungimosi, skilimo ir pavadavimo (oksidacijos – redukcijos) reakcijų lygčių lyginimas
- Nustatome kiekvieno elemento oksidacijos laipsnį;
- Parašome elementus, kurie keitė oksidacijos laipsnį.
Krūvių skirtumus išlyginame parašę elektronus.
Prisijungtų elektronų skaičius turi būti lygus atiduotų elektronų skaičiui, todėl parenkami daugikliai. - Perkeliame koeficientus į reakcijos lygtį.
3.4.1. Kaip reikia lyginti jonų mainų reakcijų lygtis: bendrųjų lygčių rašymas
1. Parašome reakcijos lygtį:
CaCl2 + Na3PO4 → Ca3(PO4)2 + NaCl
Lyginimą pradedame nuo didžiausią krūvį turinčio jono ir kur jo yra daugiau.
Tai gi Ca2+ po rekcijos jo yra 3, tai prieš reakciją prie CaCl2 reikia parašyti 3
3CaCl2 + Na3PO4 → Ca3(PO4)2 + NaCl
Tada prieš reakciją Cl- turime 6, po reakcijos 1, todėl po reakcijos prie NaCl parašome 6
3CaCl2 + Na3PO4 → Ca3(PO4)2 + 6 NaCl
Na+ prieš reakciją turime 3, po reakcijos 6, todėl preš Na3PO4 rašome 2
3CaCl2 + 2Na3PO4 → Ca3(PO4)2 + 6NaCl
2. Parašome reakcijos lygtį:
Al2(SO4)3 + NaOH →Na2SO4 + Al(OH)3
Lyginimą pradedame nuo didžiausią krūvį turinčio jono ir kur jo yra daugiau.
Tai gi Al3+ prieš rekciją jo yra 2, tai po reakcijos prie Al(OH)3 reikia parašyti 2
Al2(SO4)3 + NaOH →Na2SO4 + 2Al(OH)3
Tada prieš reakciją SO42- turime 3, po reakcijos 1, todėl po reakcijos prie Na2SO4 parašome 3
Al2(SO4)3 + NaOH →3Na2SO4 +2 Al(OH)3
Na+ prieš reakciją turime 1, po reakcijos 6, todėl preš NaOH rašome 6
Al2(SO4)3 + 6NaOH →3Na2SO4 + 2Al(OH)3
3. Parašome reakcijos lygtį:
BaCl2(aq) +AgNO3(aq) → Ba(NO3)2(aq) + AgCl(k)
Pradedame lyginti nuo didžiausią krūvį turinčio jono. Tai vadinasi nuo Ba2+. Prieš reakciją Ba2+ yra 1 ir po reakcijos Ba2+ yra 1.
Tada prieš reakciją Cl- yra 2, o po rekcijos 1, todėl prieš AgCl rašome 2:
BaCl2(aq) +AgNO3(aq) → Ba(NO3)2(aq) + 2AgCl(k)
Ag+ prieš reakciją yra 1, o po reakcijos yra 2, todėl prieš AgNO3, rašome 2:
BaCl2(aq) + 2AgNO3(aq) → Ba(NO3)2(aq) + 2AgCl(k)
NO3- prieš reakciją ir po reakcijos yra po 2.
3.4.2. Kaip reikia lyginti jonų mainų reakcijų lygtis: joninių lygčių rašymas
Rašant jonines lygtis reikia atkreipti dėmesį į tai, koks yra medžiagos tirpumas (tirpi/mažai tirpi/netirpi), kaip medžiaga (gerai/silpnai) disocijuoja į jonus / jonizuojasi.
Informaciją apie medžiagų tirpumą randama tirpumo lentelėje (žr. 1.5 sk.)
Silpnai į jonus disocijuoja / jonizuojasi silpni elektrolitai, kurių disociacijos / jonizacijos laipsnis α<30% (žr. 1.6. sk.)
1. Bendroji lygtis:
CH3COONa(aq) + HCl(aq) → CH3COOH(aq) + NaCl(aq)
Joninė lygtis:
CH3COO-(aq) + Na+(aq) + H+(aq) + Cl-(aq) →CH3COOH(aq) + Na+(aq) + Cl-(aq)
Išbraukiame jonus, kurie yra ir prieš reakciją ir po reakcijos. Ir rašome sutrumpintą joninę lygtį:
CH3COO-(aq) + H+(aq) →CH3COOH(aq).
2. Bendroji lygtis:
Al(OH)3(k) + 3HCl(aq) → AlCl3(aq) + 3H2O(s)
Joninė lygtis:
Al(OH)3(k) + 3H+(aq) + 3Cl-(aq) → Al3+(aq) + 3Cl-(aq) + 3H2O(s)
Išbraukiame jonus, kurie yra ir prieš reakciją ir po reakcijos. Ir rašome sutrumpintą joninę lygtį:
Al(OH)3(k) + 3H+(aq) → Al3+(aq) + 3H2O(s)
3. Bendroji lygtis:
3Ba(NO3)2 (aq) + Al2(SO4)3(aq) → 2Al(NO3)3(aq) + 3BaSO4(k)
Joninė lygtis:
3Ba2+(aq) + 6NO3-(aq) + 2Al3+ + 3SO42-(aq) → 2Al3+(aq) + 6NO3-(aq) + 3BaSO4(k)
Išbraukiame jonus, kurie yra ir prieš reakciją ir po reakcijos. Ir rašome sutrumpintą joninę lygtį:
3Ba2+(aq) + 3SO42-(aq) → 3BaSO4(k)
3.4.3. Oksidacijos – redukcijos lygčių lyginimas elektronų balanso metodu
Išlyginti reakcijos lygtys, nustatyti oksidatorių ir reduktorių.
1 pavyzdys
a) nustatome kiekvieno elemento oksidacijos laipsnį;
b) parašome elementus, kurie keitė oksidacijos laipsnį:
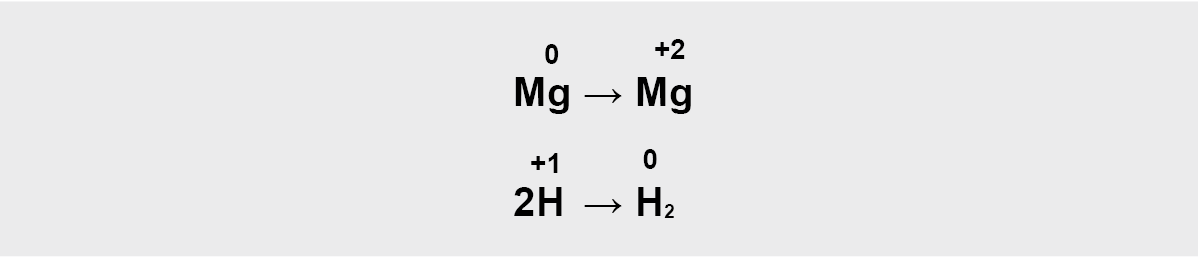
Krūvių skirtumus išlyginame parašę elektronus.
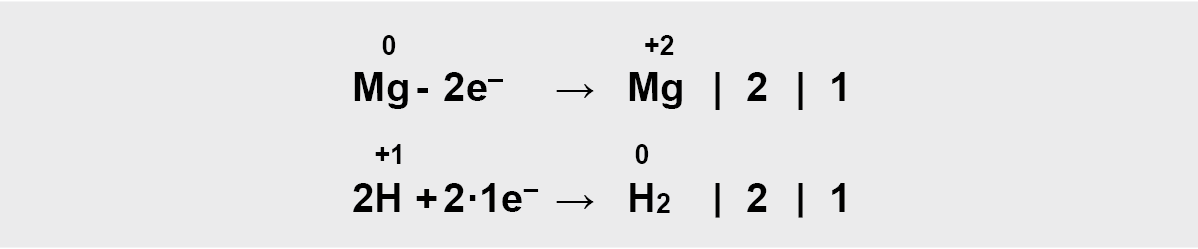
Prisijungtų elektronų skaičius turi būti lygus atiduotų elektronų skaičiui, todėl parenkami daugikliai (šiuo atveju 1)
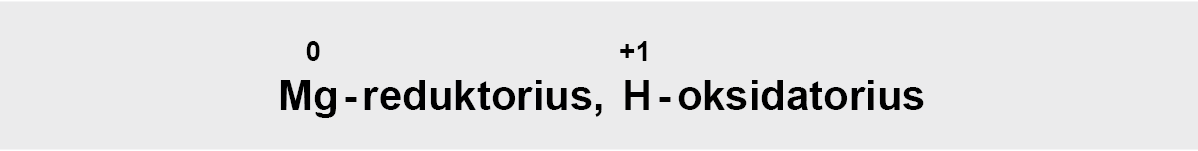
c) perkeliame koeficientus į reakcijos lygtį:
![]()
2 pavyzdys
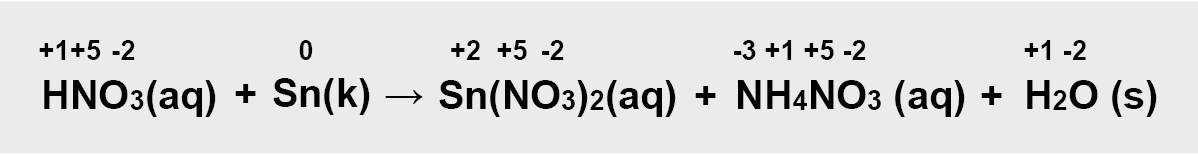
a) nustatome kiekvieno elemento oksidacijos laipsnį;
b) parašome elementus, kurie keitė oksidacijos laipsnį:
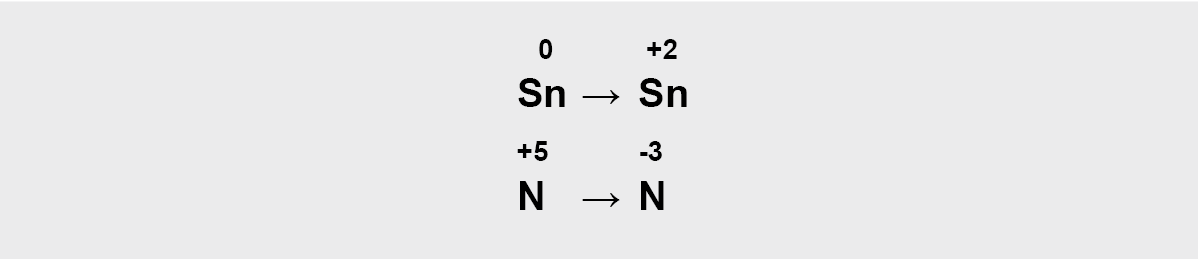
Krūvių skirtumus išlyginame parašę elektronus.
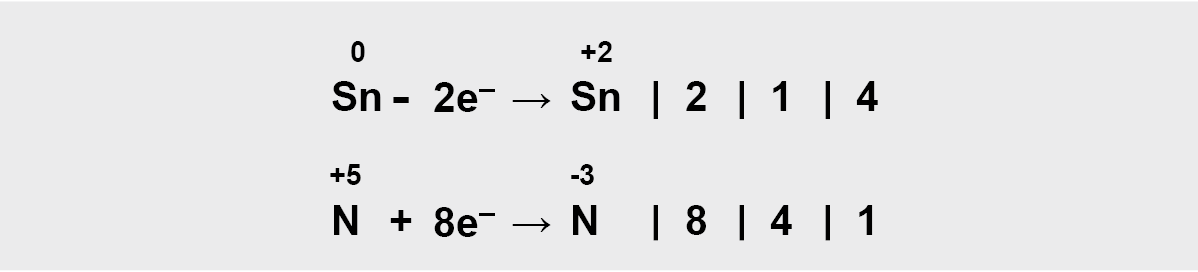
Prisijungtų elektronų skaičius turi būti lygus atiduotų elektronų skaičiui, todėl parenkami daugikliai (šiuo atveju 4 rašome prie Sn, o 1 prie N po reakcijos)
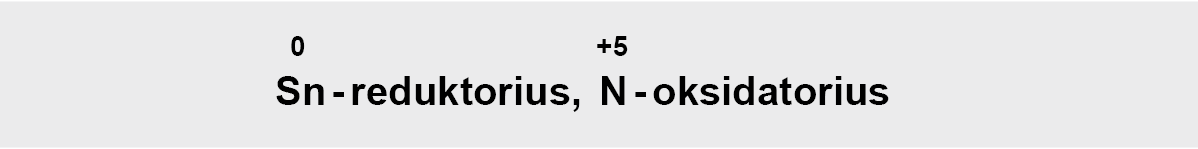
c) perkeliame koeficientus į reakcijos lygtį:
![]()
3 pavyzdys
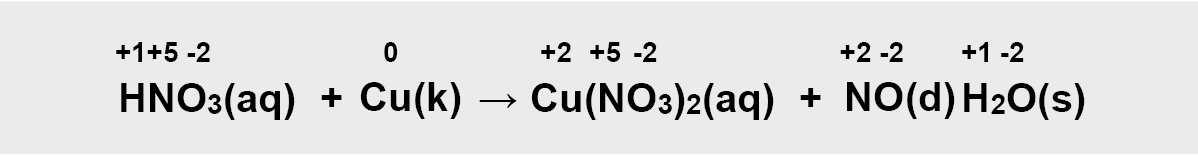
a) nustatome kiekvieno elemento oksidacijos laipsnį;
b) parašome elementus, kurie keitė oksidacijos laipsnį:
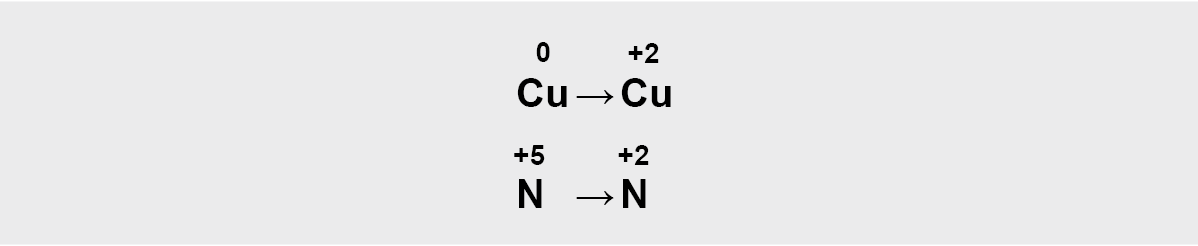
Krūvių skirtumus išlyginame parašę elektronus.
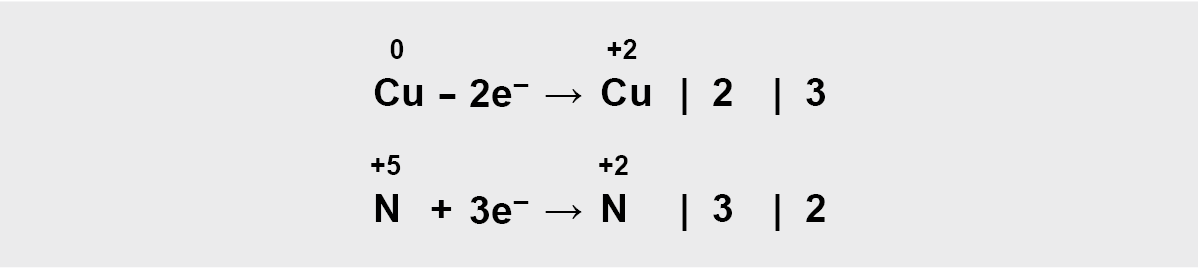
Prisijungtų elektronų skaičius turi būti lygus atiduotų elektronų skaičiui, todėl parenkami daugikliai (šiuo atveju 3 ir 2)
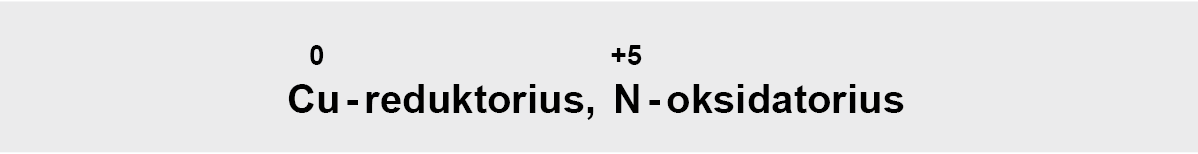
c) perkeliame koeficientus į reakcijos lygtį:
![]()
3.5. Skaičiavimai pagal reakcijų lygtis
1. Kiek gramų NaOH reikia paimti, kad pilnai sureaguotų 40 gramų FeCl3?
● Parašome ir išlyginame reakcijos lygtį:
3NaOH + FeCl3 →3NaCl + Fe(OH)3
● Virš reakcijos lygties surašome ką turime ir ką reikia rasti:
![]()
● Po reakcijos lygtimi parašome kokiais molių kiekiais reaguoja medžiagos pagal reakcijos lygtį:

● Tada suskaičiuojame molines mases NaOH ir FeCl3:
M(NaOH) = 23 + 16 + 1 = 40g/mol
M(FeCl3) = 56 + 35,5 x 3 = 162,5 g/mol
I būdas:
m = n x M
m(NaOH) = 3 mol x 40 g/mol = 120 g
m(FeCl3) = 1 mol x 162,5 g/mol = 162,5 g
● Statome proporciją:X g NaOH – 40 g FeCl3
120 g NaOH – 162,5 g FeCl3
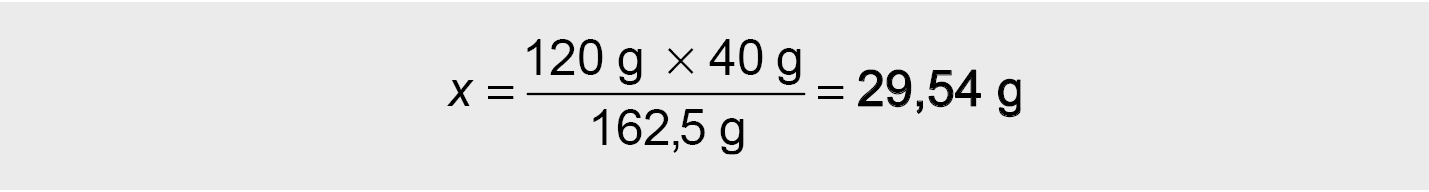
II būdas:

● Parašome reakcijos lygtį ir virš lygties surašome kas duota ir ką reikia rasti moliais:

● Statome proporciją:
X mol NaOH – 0,246 mol FeCl3
3 mol NaOH – 1 mol FeCl3
● Suskaičiuojame masę:
m = n x M = 0,738 mol x 40 g/mol = 29,52 g
2. Kiek gramų neutraliosios druskos susidarys reaguojant 125 ml 16 % ( d=1,109 g/cm3) sulfatinės rūgšties su 200 ml 0,5 mol/l kalio šarmo.
● Rašome reakcijos lygtį:
H2SO4 + KOH → K2SO4 + H2O
● Tada išlyginame reakcijos lygtį:
H2SO4 + 2KOH → K2SO4 + 2H2O
● Tada virš lygties surašome kas yra duota ir ką reikia rasti:
![]()
● Po reakcijos lygtimi surašome kokiais molių ir gramų kiekiais reaguoja medžiagos:
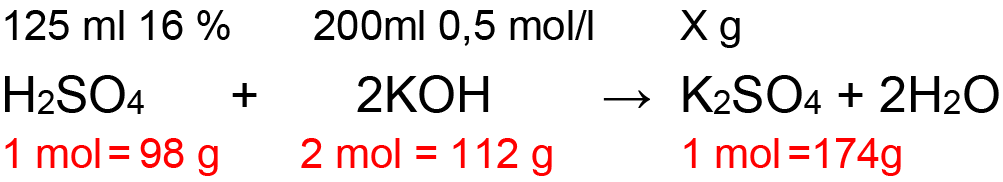
● Suskaičiuojame medžiagų molines mases:
M(H2SO4) = 1 x 2 +32 x 1+16 x 4 = 98 g/mol
M(KOH) = 39 x 1 +16 x 1 + 1 x 1 = 56 g/mol
M(K2SO4) = 39 x 2 + 32 x 1 + 16 x 4 = 174 g/mol
● Žinome kiek paimta H2SO4 tirpalo. Reikia perskaičiuoti kiek grynos sieros rūgšties paimta. Pirmiausia suskaičiuojame masę tirpalo:
m = V x d = 125 ml x 1,109 g/ml = 138,625 g
● Tada skaičiuojame proporciją kiek grynos medžiagos:
100 g tirpalo yra 16 g H2SO4
138,625 g tirpalo – x g H2SO4
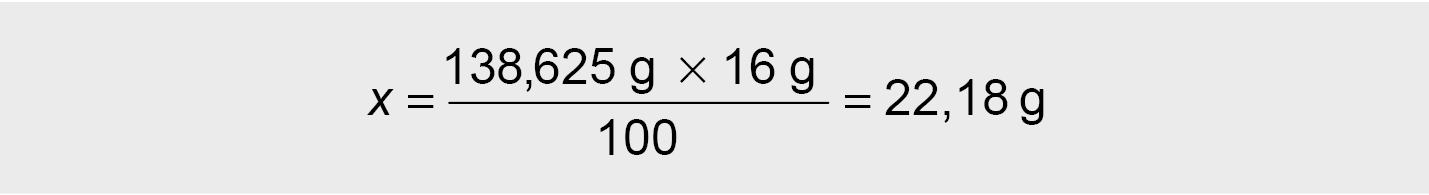
● Arba grynos medžiagos masę galime surasti iš formulės:

● Išsivedam m(medžiagos) kam lygi:
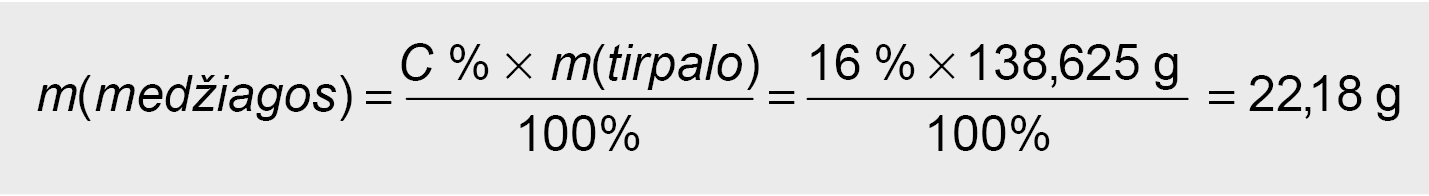
● Apskaičiuojame kiek gryno KOH turime:
n = CM x V = 0,5 mol/l x 0,2 l = 0,1 mol
m = n x M = 0,1 mol x 56 g/mol = 5,6 g
● Vieną iš medžiagų pažymime X, ir patikriname, kurios medžiagos yra perteklius. Sakykime pasirinkome X H2SO4:
X g H2SO4 – 5,6 g KOH
98 g H2SO4 – 112 g KOH
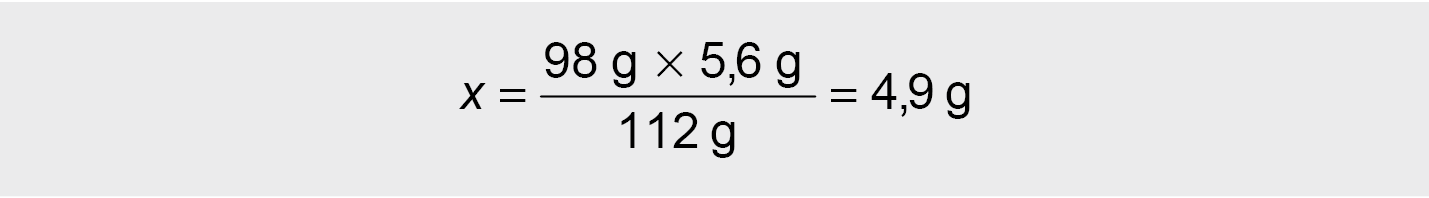
● Mums reikia 4,9 g, o turime 22,18 g. Tai reiškia, kad H2SO4 turime perteklių ir kiek susidarė druskos skaičiuosime pagal KOH.
5,6 g KOH – x g K2SO4
112 g KOH – 174 g K2SO4
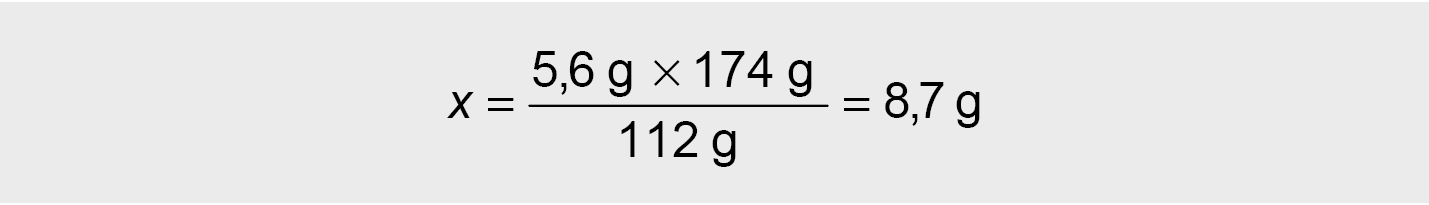
Ats.: Susidarys 8,7 g K2SO4
3. Koks dujų tūris išsiskirs reaguojant 300 g 25 % druskos rūgšties tirpalo su CaCO3?
● Parašome reakcijos lygtį:
2HCl(aq) + CaCO3 (k) → CaCl2(aq) + H2O(s) + CO2(d)
● Virš reakcijos lygties surašome kas duota ir ką reikia rasti, po reakcijos lygtimi, kokiais molių kiekiais reaguoja:
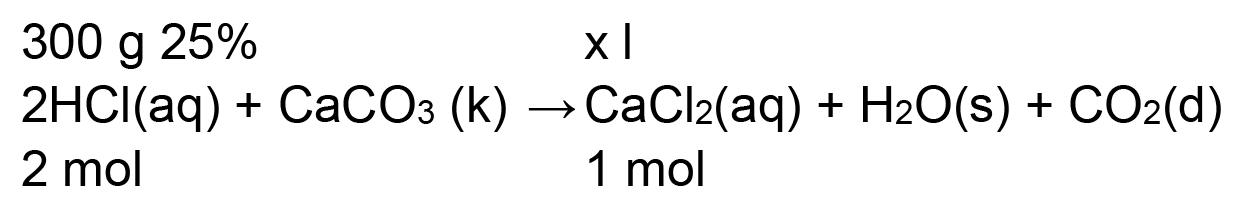
● Suskaičiuojame kiek grynos HCl turime:
100 g tirpalo yra 25 g HCl
300 g tirpalo yra x g HCl
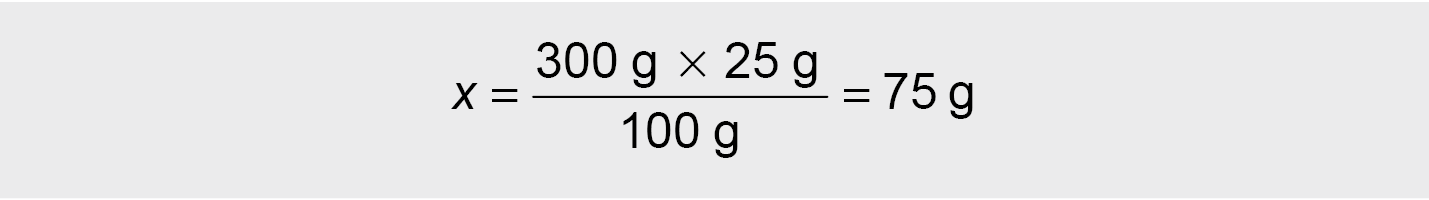
● Arba grynos medžiagos masę galime surasti iš formulės:

● Išsivedam m(medžiagos) kam lygi:

● Skaičiuojame molinę masę:
M(HCl) = 1 + 35,5 = 36,5 g/mol
● Masę perskaičiuojame moliais:

● Tada statome vėl proporciją pagal reakcijos lygtį:
2,05 mol HCl reaguoja ir susidaro x mol CO2
2 mol HCl – 1 mol CO2
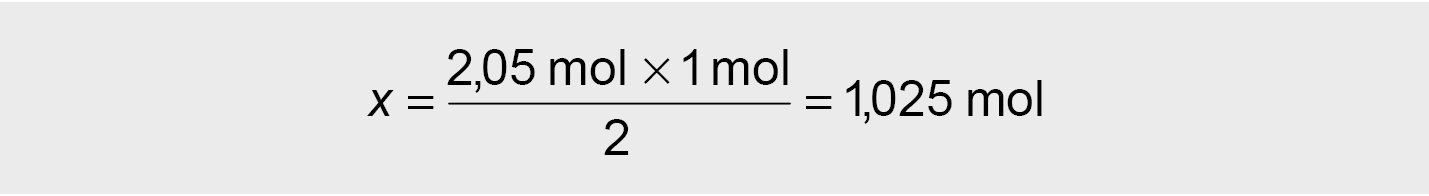
● Molius perskaičiuojame litrais:
V = VM x n = 22,4 l/mol x 1,025 mol = 22,96 l
Ats.: Išsiskirs 22,96 l CO2 dujų.