Teorinė medžiaga su pavyzdžiais
2.3. Cheminiai ryšiai
2.3.3. Metališkasis ryšys
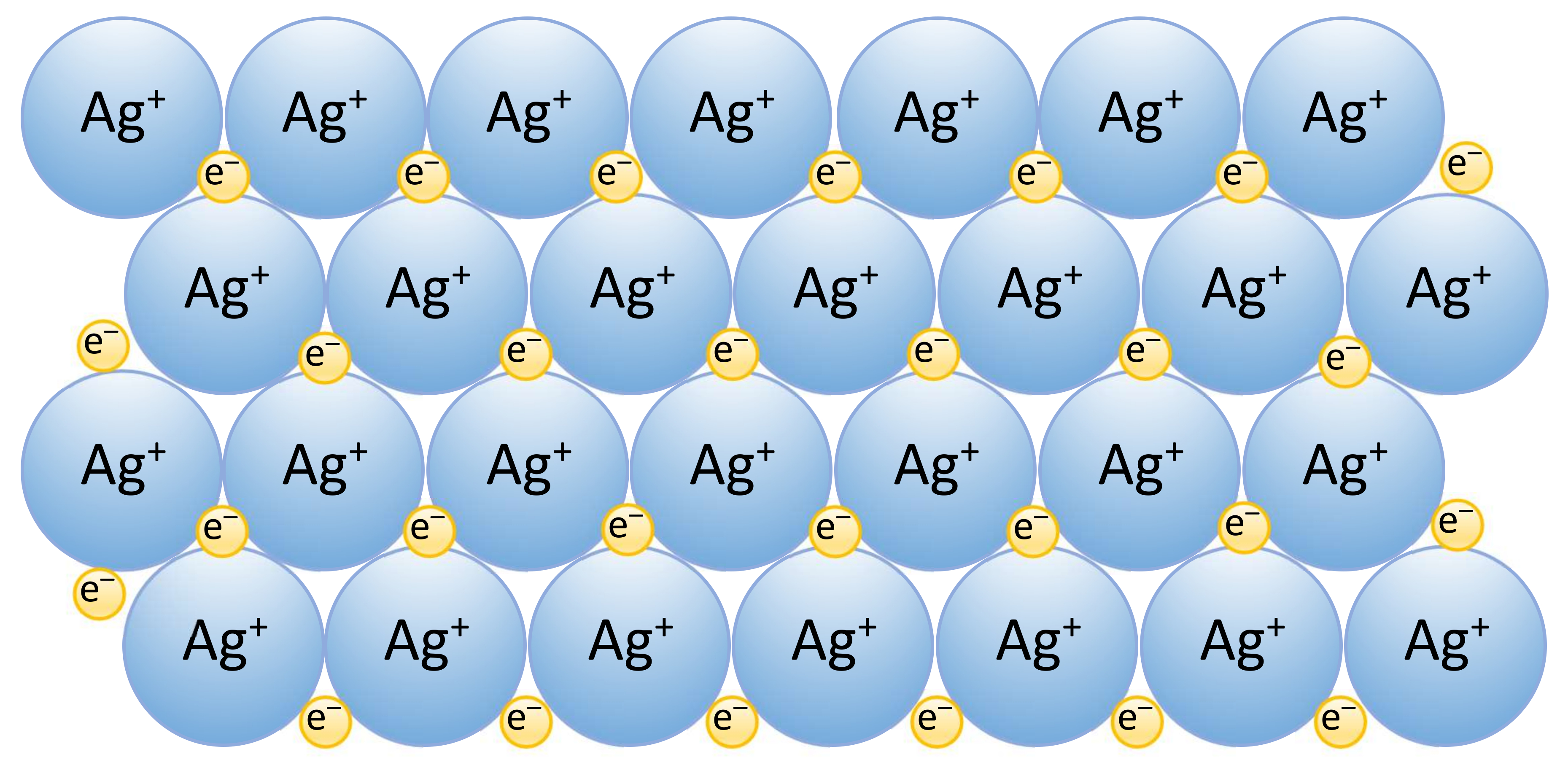
Metališkasis ryšys pasireiškia tik tarp metalo atomų ir jonų. Šis ryšys jungia metalų jonus metalų kristaluose. Metalai yra geri šilumos ir elektros laidininkai, plastiški. Daugumos jų lydymosi ir virimo temperatūros yra aukštos arba labai aukštos. Dėl savo vidinės struktūros metalai, išskyrus Hg, įprastinėmis sąlygomis yra kietos kristalinės medžiagos. Jų gardelėse taisyklingai išsidėstę teigiamieji jonai, o tarp jų juda elektronai. Metalų atomuose yra daug laisvųjų orbitalių, kurios susinėrusios su gretimų atomų laisvosiomis orbitalėmis sudaro daugiacentrines atomines orbitales, apimančias visą metalo kristalą. Taigi kiekvieno metalo atomo valentiniai elektronai yra susiję ne su vienu branduoliu, o yra bendri visiems metalo atomams ir laisvai juda visame metalo tūryje (ne tik atskiruose kristaluose, bet ir tarp besiliečiančių kristalų!!!). Ši laisvųjų elektronų ir atomų teigiamųjų jonų elektrostatinė sąveika ir lemia stiprias ryšio jėgas tarp metalų atomų, būdingas metališkajam ryšiui. Metališkasis ryšys būdingas tik kietosios ir skystosios būsenos metalams. Dėl bendrų elektronų judėjimo metalų kristaluose jie yra kieti, tačiau lengvai plastiškai deformuojasi juos tempiant, gniuždant, lenkiant ar kitaip veikiant mechaniškai.