Teorinė medžiaga su pavyzdžiais
| Gedruckt von: | Utilizator vizitator |
| Datum: | Samstag, 30. Mai 2026, 14:01 |
2.1. Atomo sandara
Ką reikia žinoti apie atomo sandarą?
2.1.1. Elementariosios dalelės, atominis skaičius ir masės skaičius
Atomas sudarytas iš teigiamą krūvį turinčio branduolio ir aplink jį skriejančių neigiamą krūvį turinčių elektronų. Atomo branduolį sudaro protonai ir neutronai. Protonai, neutronai ir elektronai yra elementariosios dalelės:
- protonai (žymimi p+) – teigiamo krūvio dalelės, kurių masė 1 a.m.v., santykinis krūvis +1;
- neutronai (žymimi no) – elektros krūvio neturinčios dalelės, kurių masė 1 a.m.v.;
- elektronai (žymimi e-) – neigiamo krūvio dalelės, kurių masė ~0,00055 a.m.v., santykinis krūvis -1.
Atomas yra neutralus, nes bendras branduolio krūvis yra lygus bendram neigiamam elektronų krūviui, t.y. elektronų skaičius yra lygus teigiamąjį krūvį turinčių protonų skaičiui.
Atominis skaičius (žymimas raide Z) – protonų skaičius atomo branduolyje (elemento numeris periodinėje elementų lentelėje).
Masės skaičius (žymimas raide A) – bendras protonų ir neutronų skaičius atomo branduolyje.
Cheminis elementas – visuma atomų, turinčių vienodą branduolio krūvį, t.y. tą patį atominį skaičių Z.
Visi cheminiai elementai yra surašyti į periodinę elementų lentelę jų atominio skaičiaus, t.y. branduolio krūvio, didėjimo tvarka.
Neutronų skaičius branduolyje žymimas raide N. Jis yra lygus elemento masės skaičiaus ir atominio skaičiaus skirtumui:
![]()
Taigi
Masės skaičius (A) = Atominis skaičius (Z) + neutronų skaičius (N).
Apibūdinant elemento sudėtį, reikia nurodyti, kiek atome yra protonų, neutronų ir elektronų. Todėl periodinėje elementų lentelėje vartojami specialūs simboliai:
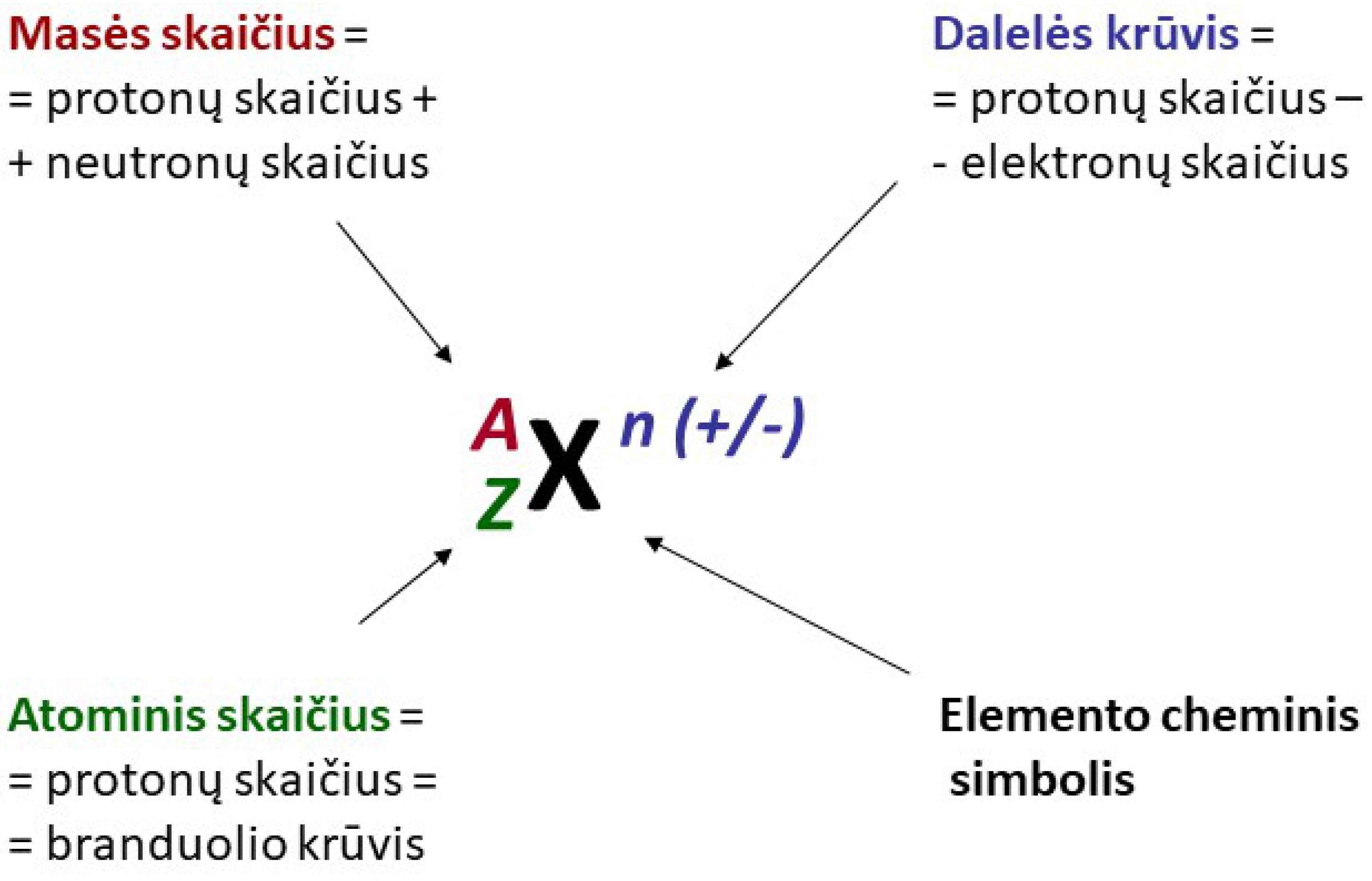
2.1.1. pav. Atomo ar dalelės žymėjimas
2.1.2. Izotopai
Izotopai – tai to paties cheminio elemento atomai, turintys vienodą branduolio krūvį, bet skirtingą masės skaičių. Jų branduoliuose yra vienodas protonų, bet skirtingas neutronų skaičius.
Daugumos vandenilio atomų branduoliuose yra 1 protonas ir 0 neutronų. Tačiau gamtoje egzistuoja ir tokie vandenilio atomai, kurių branduoliuose yra neutronų. Trys vandenilio izotopai yra protis (jo branduolyje yra tik 1 protonas), deuteris (jo branduolį sudaro 1 protonas ir 1 neutronas; kartais jis žymimas simboliu D) ir tritis (jo branduolį sudaro 1 protonas ir 2 neutronai; kartais jis žymimas simboliu T). Visų šių atomų branduoliuose yra tik po 1 protoną – visi jie yra to paties cheminio elemento atomai. Cheminės izotopų savybės yra vienodos.
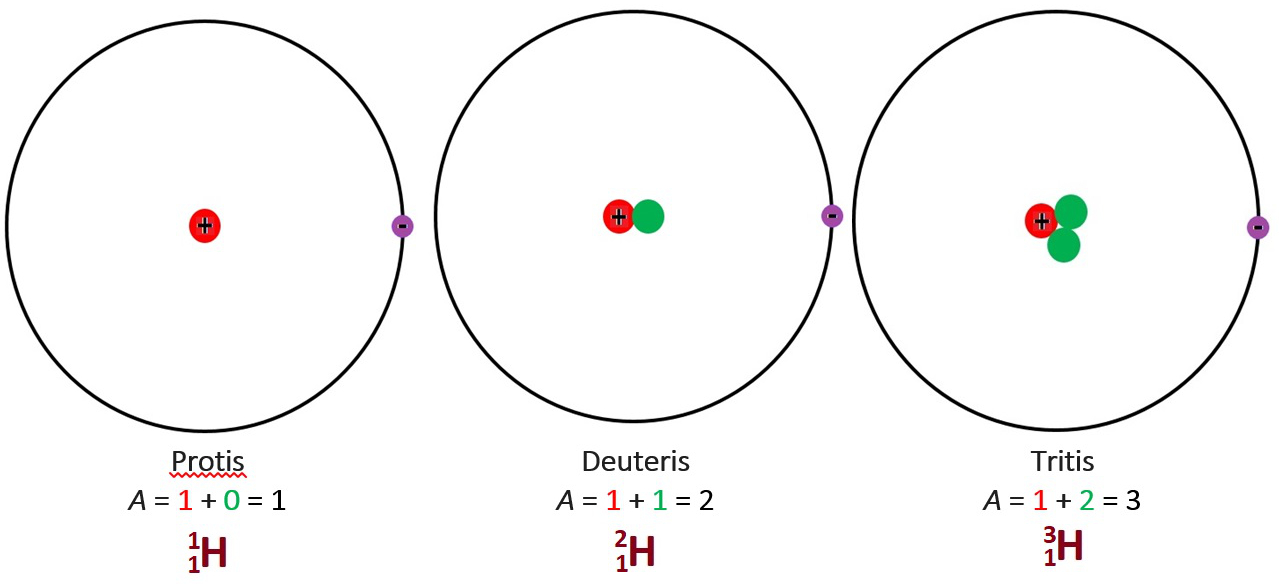
2.1.2. pav. Vandenilio (Z = 1) izotopai
Dauguma cheminių elementų gamtoje egzistuoja kaip izotopų mišiniai. Periodinėje elementų lentelėje yra nurodytos gamtinių izotopų mišinių vidutinės santykinės atominės masės. Jos apskaičiuojamos, įvertinant kiekvieno izotopo masės skaičių ir santykinį paplitimą gamtoje. Egzistuoja du anglies izotopai

Anglies vidutinė santykinė atominė masė yra
![]()
Jei cheminis elementas neegzistuoja gamtoje, periodinėje elementų lentelėje nurodoma jo stabiliausio izotopo santykinė atominė masė, kuri rašoma skliausteliuose.
2.1.3. Elektronai atome
Elektronai, esantys aplink branduolį, sudaro elektronų apvalkalą. Jame elektronai išsidėsto sluoksniais, atitinkančiais atstumus, kuriais elektronai yra nutolę nuo branduolio. Kiekvienas toks sluoksnis, supantis atomo branduolį su jam priklausančiais elektronais, vadinamas energijos lygmeniu.
Erdvė, kur yra didžiausia tikimybė būti elektronui, vadinama orbitale. Orbitalėje gali būti ne daugiau nei du elektronai, turintys priešingus sukinius. Elektrono sukinys vaizduojamas kaip į viršų (↑) arba į apačią (↓) nukreipta rodyklė. Aplink besisukantį elektros krūvį susidarančio magnetinio lauko kryptis priklauso nuo krūvio sukimosi krypties. Elektronas įsivaizduojamas kaip besisukantis aplink savo ašį rutuliukas, t. y. mažas magnetas. Orbitalėje priešingų sukinių elektronai traukia vienas kitą ir taip susidaro elektronų pora. Dėl šios priežasties vienoje orbitalėje gali būti tik du elektronai.
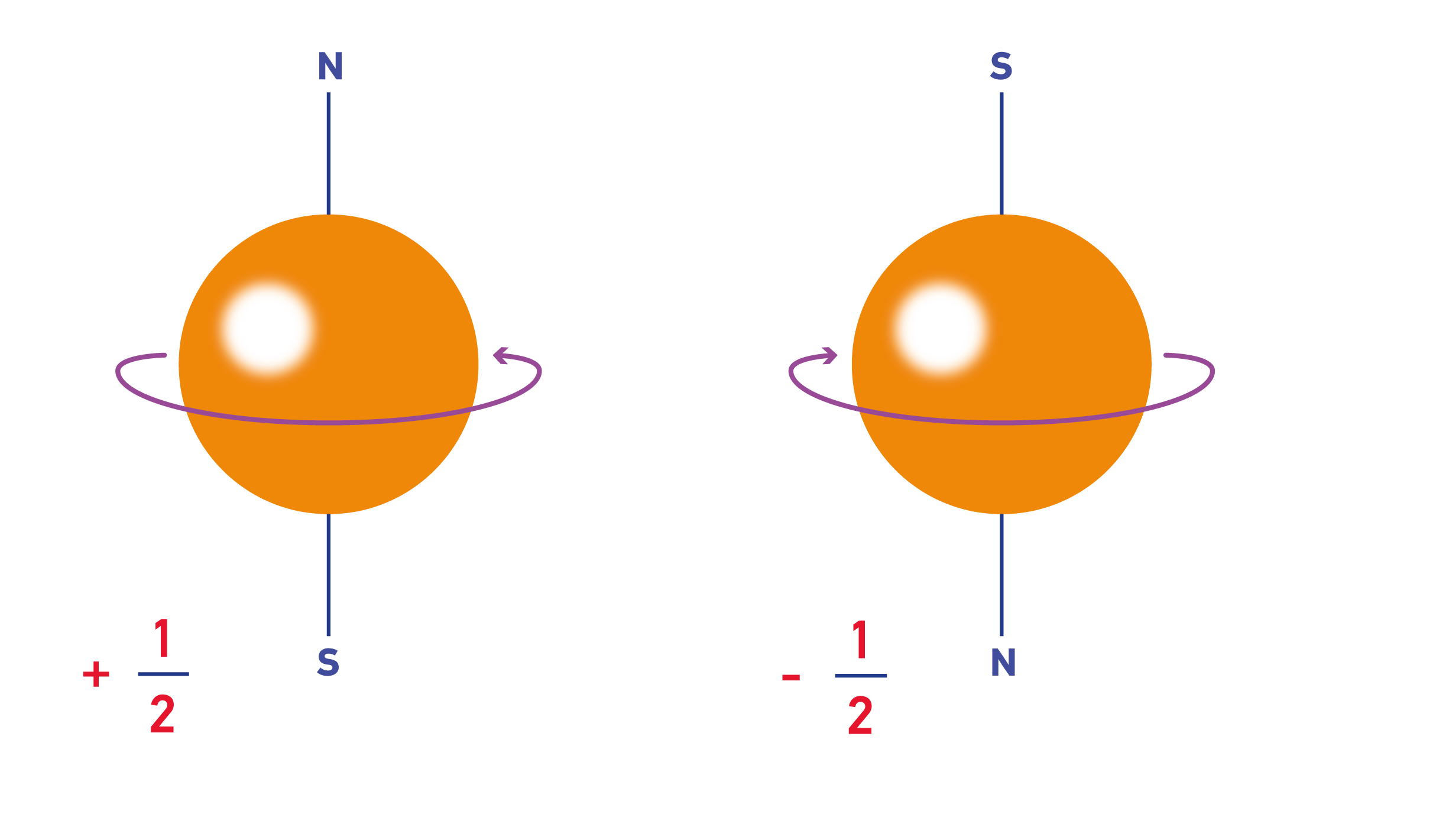
2.1.3. pav. Elektrono sukiniai
Du paprasčiausi orbitalių tipai yra s ir p.
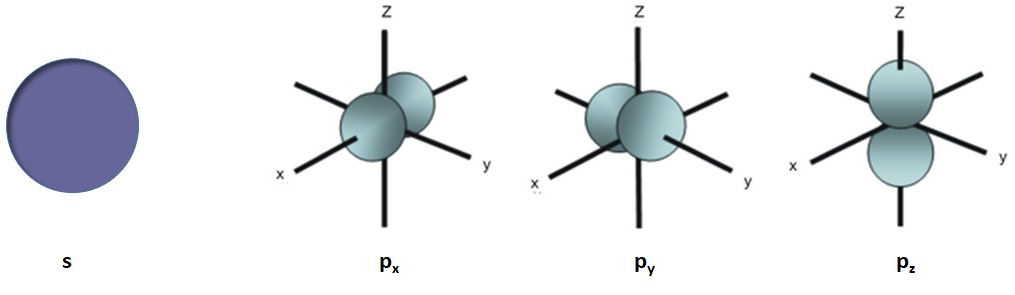
2.1.4. pav. s ir p orbitalės
Tame pačiame energetiniame lygmenyje yra viena s orbitalė,
kuri dviem elektronais yra užpildoma pirmiausiai, ir trys p orbitalės (px, py,
pz), kurios iš pradžių užpildomos po vieną elektroną, o po to jau ir po antrą.
Pirmame energijos lygmenyje yra tik viena s orbitalė, antrame energijos lygmenyje yra dviejų tipų orbitalės – s ir p. Supaprastintai orbitales galima vaizduoti kaip polygmenis.

2.1.5. pav. Energijos lygmuo ir polygmeniai
Vandenilio (H) atomo branduolyje yra 1 protonas ir atitinkamai aplink branduolį skrieja 1 elektronas. Antrasis elementas pirmajame energijos lygmenyje yra helis (He), kurio atomo branduolyje yra 2 protonai ir aplink branduolį yra 2 elektronai s orbitalėje (2.1.6. pav.).

2.1.6. pav. Vandenilio ir helio elektronų išsidėstymas atomų energijos lygmenyje
Didėjant elementų atominiam skaičiui (protonų skaičiui branduolyje), elektronai užpildo vis naujas orbitales. Užsipildžius orbitalėms viename energijos lygmenyje (sluoksnyje), elektronai pildo orbitales didesnės energijos lygmenyje (toliau nuo branduolio nutolusiame sluoksnyje). Atomai, turintys pilnai užpildytus energijos lygmenis, yra stabiliausi.
Ličio (Li), kurio atominis skaičius Z = 3, du elektronai užpildo pirmojo energijos lygmens s orbitalę, o trečiasis elektronas pradeda pildyti antrojo energijos lygmens s orbitalę (2.1.7. pav.). Berilio (Be) ketvirtasis elektronas tampa antruoju elektronu toje pačioje antrojo energijos lygmens s orbitalėje. Boro (B) penktasis elektronas pradeda pildyti antrojo energijos lygmens p orbitales (antrąjį polygmenį). Anglies (C) ir azoto (N) atitinkamai šeštasis ir septintasis elektronai pildo vis kitą p orbitalę, o deguonies (Z=8) atomo aštuntasis elektronas tampa antruoju elektronu pirmoje p orbtalėje, nes daugiau laisvų orbitalių nėra. Atitinkamai fluoro (F) ir neono (Ne) devintasis ir dešimtasis elektronai užpildo kitas dvi p orbitales. Neono elektrono konfigūracija yra stabiliausia, nes užpildytos visos elektronų orbitalės.
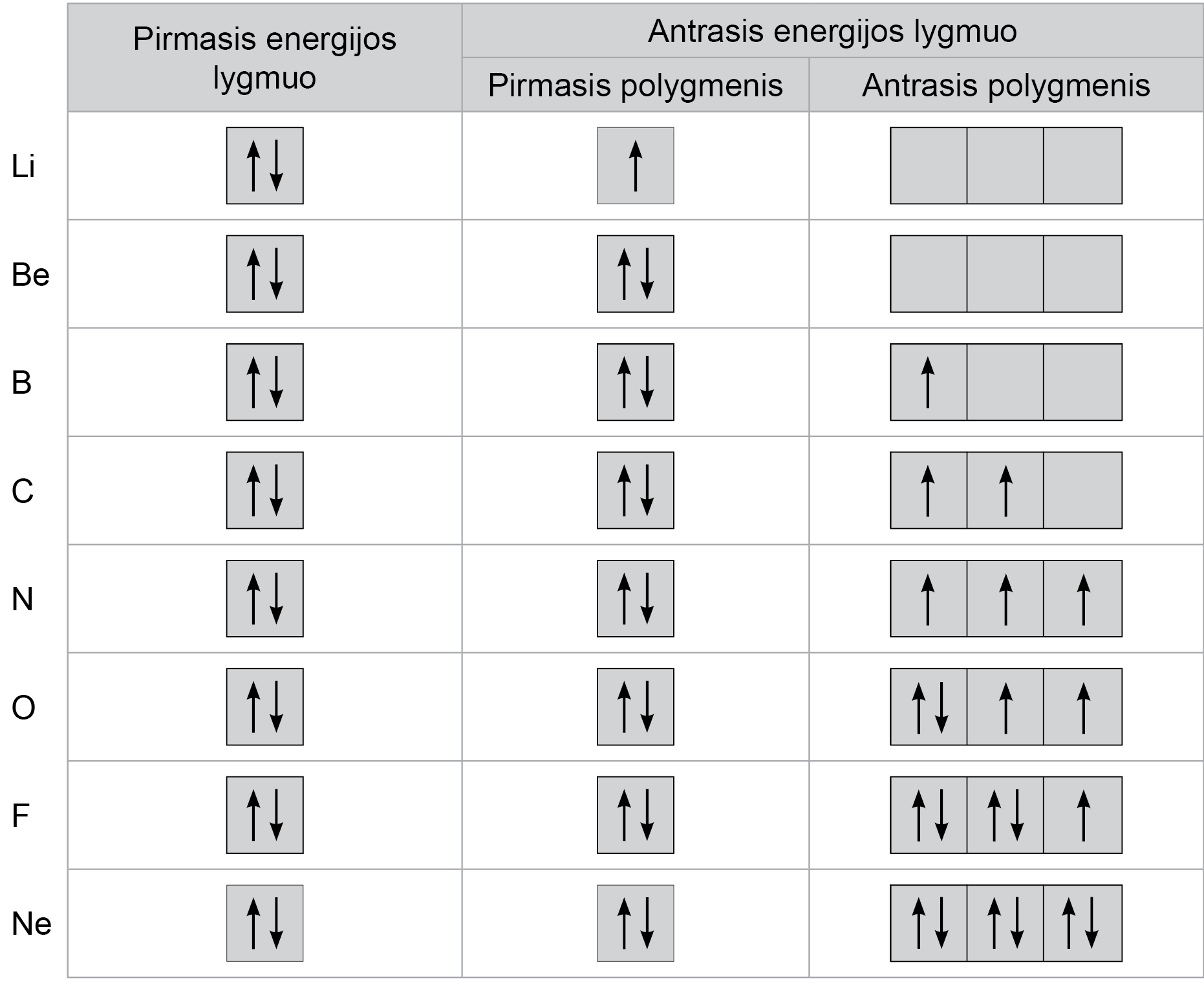
2.1.7. pav. Elementų nuo ličio iki neono elektronų išsidėstymas atomų energijos lygmenyse ir polygmeniuose
Atomai gali jungtis tarpusavyje tik pasikeitus jų elektroninei sandarai. Arčiau branduolio esančių ir jo stipriau traukiamų vidinių energijos lygmenų elektronai negali dalyvauti susidarant cheminiams ryšiams. Labai svarbūs yra valentiniai elektronai, kuriems priskiriami didžiausios energijos orbitalėse esantys elektronai.
2.1.4. Valentiniai elektronai ir valentingumas
Valentiniai elektronai – tai elektronai, galintys dalyvauti susidarant cheminiam ryšiui. Jie yra aukščiausiame energijos lygmenyje.
Valentingumas – tai cheminio elemento atomo ryšių, sudaromų su kitais atomais, skaičius. Valentingumas lygus atomus jungiančių elektronų porų skaičiui.
Jei toliausiai nuo branduolio esančiame energijos lygmenyje yra laisvų orbitalių, elektronai gali peršokti iš tos orbitalės, kurioje jau yra du suporuoti elektronai, į laisvą orbitalę. Tokia būsena vadinama sužadintąja. Peršokus elektronams į laisvas orbitales, pasikeičia valentinių elektronų skaičius, o tuo pačiu ir cheminių ryšių, kuriuos atomas gali sudaryti su kitais atomais, skaičius. Normaliosios būsenos anglies (Z=6) atome yra 2 valentiniai (nesuporuoti) elektronai, tačiau yra ir 2 laisvos p orbitalės. Sužadintosios būsenos C atome yra 4 nesuporuoti elektronai ir anglis tampa keturvalente (2.1.8. pav.).

2.1.8. pav. Elektronų išsidėstymas sužadintosios būsenos anglies atomo energijos lygmenyse ir polygmeniuose.
2.1.5. Atomų ir jonų elektronų konfigūracijos
Svarbu: Atkreipkite dėmesį, jog neigiamų karbido C4-, nitrido N3-, oksido O2-, fluorido F- jonų bei teigiamų natrio Na+, magnio Mg2+ bei aliuminio Al3+ jonų elektroninės konfigūracijos yra vienodos ir sutampa su neutralaus neono (Ne) atomo elektronine konfigūracija. Tokią pačią vienodą jonų elektronų konfigūraciją su VIIIA grupės elementu galime sudaryti ir su kitų periodų elementais.
Vandenilio atomo ir jono elektronų konfigūracija
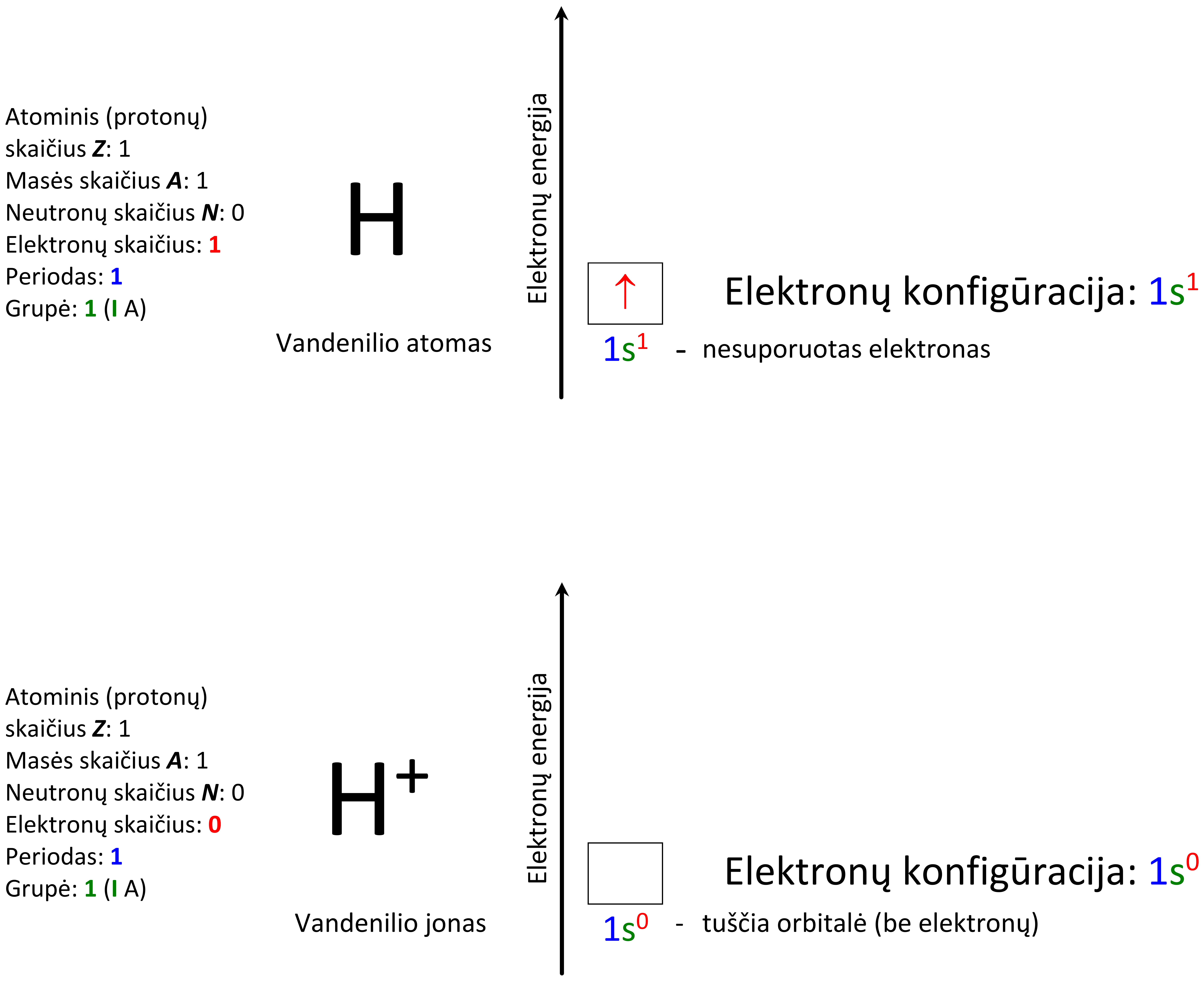
Helio atomo elektronų konfigūracija
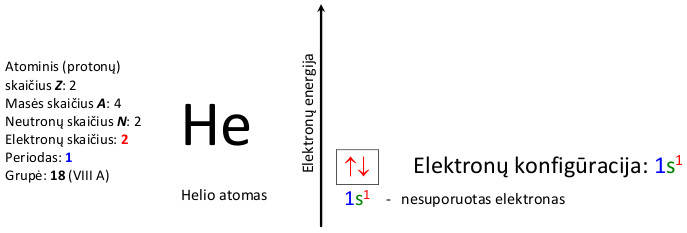
Ličio atomo ir jono elektronų konfigūracija
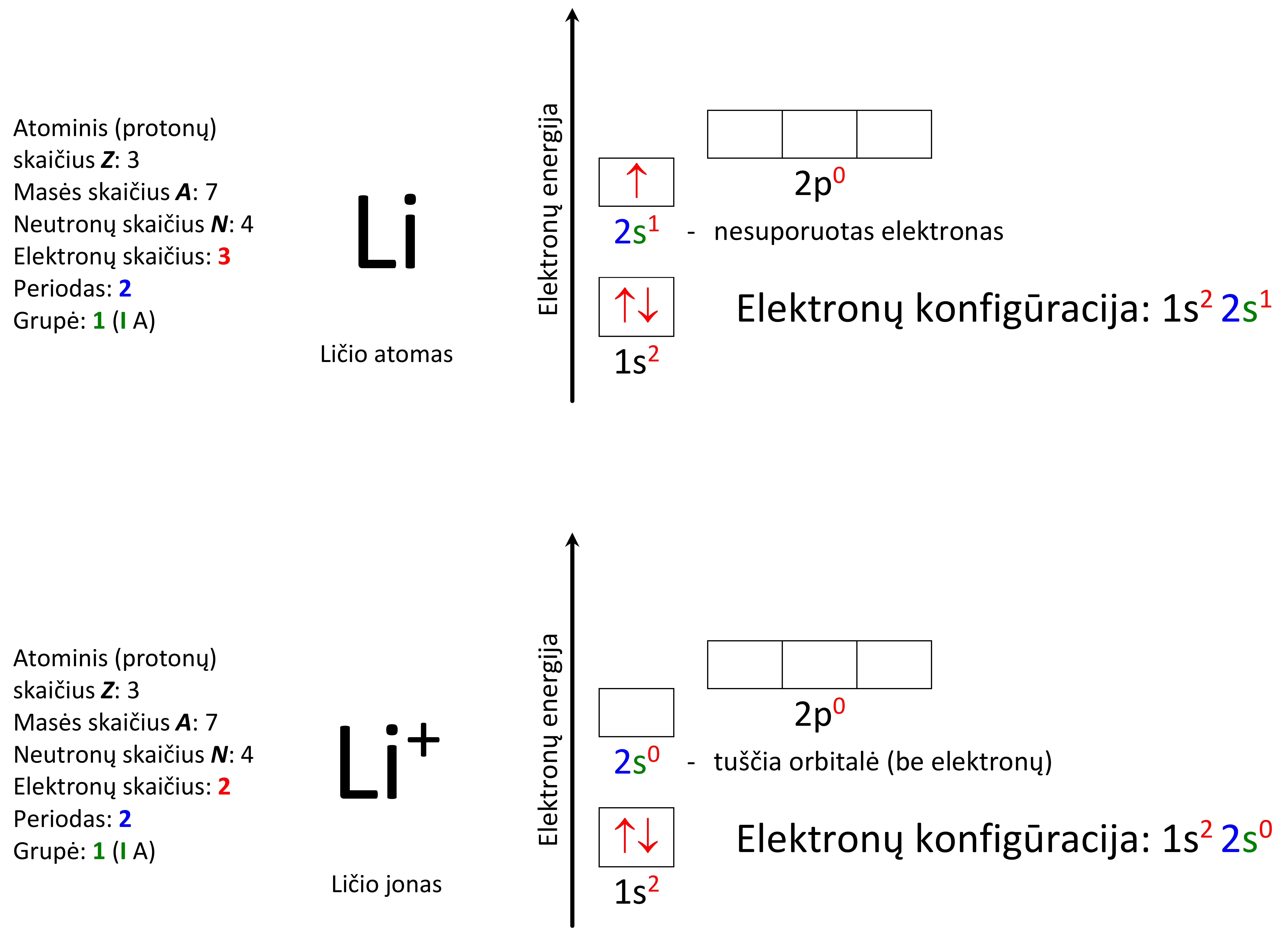
Berilio atomo ir jono elektronų konfigūracija
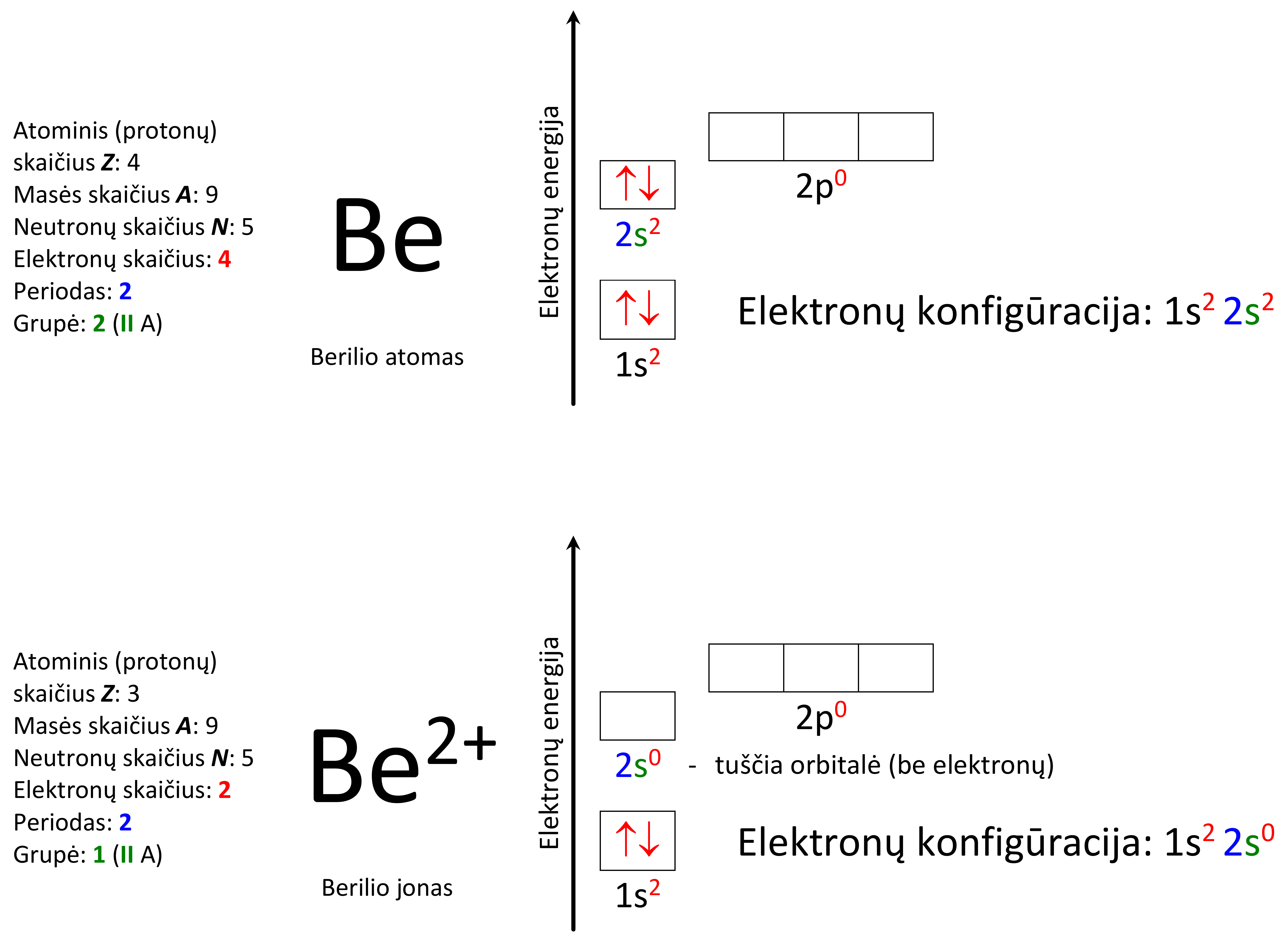
Anglies atomo ir karbido jono elektronų konfigūracija
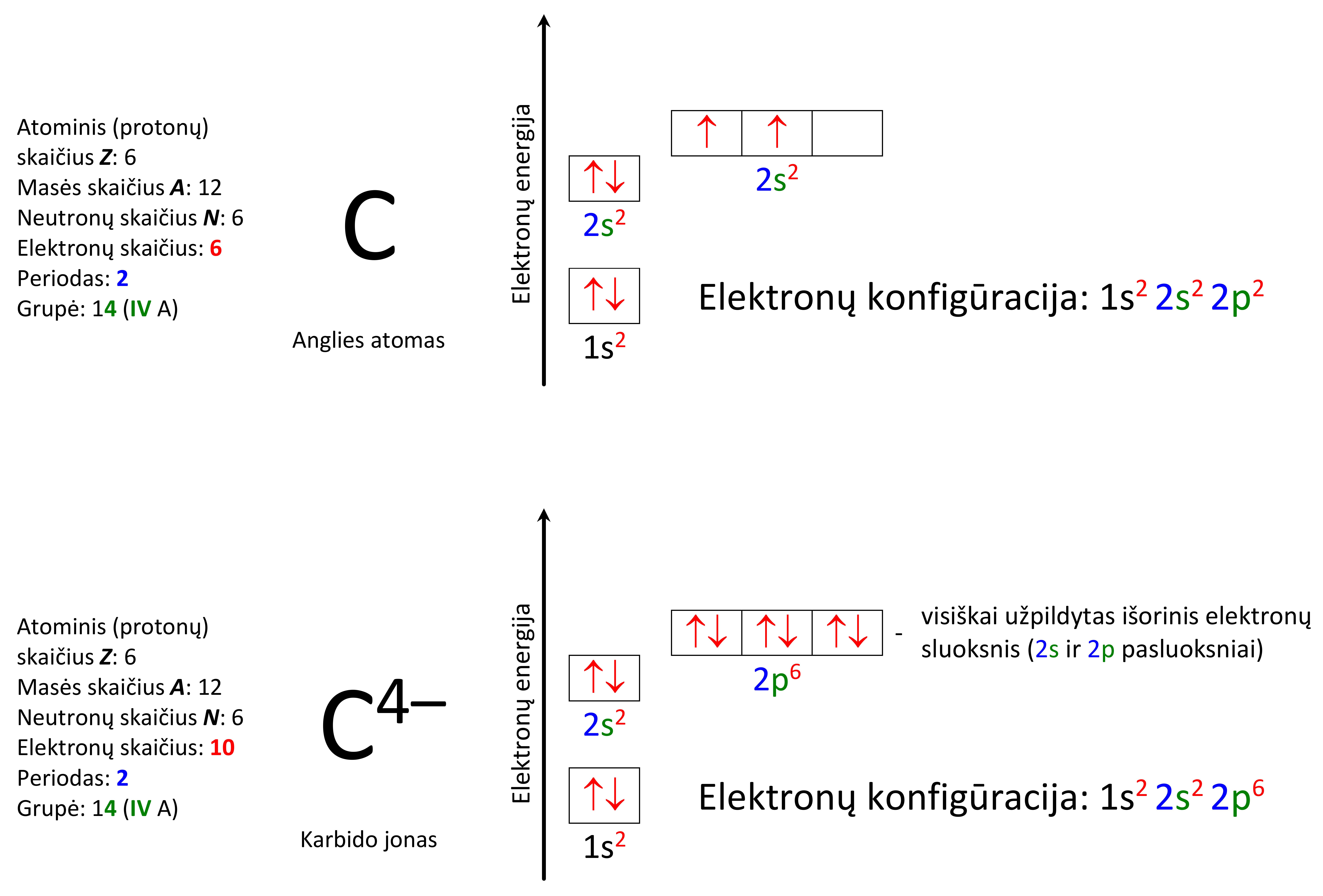
Azoto atomo ir nitrido jono elektronų konfigūracija
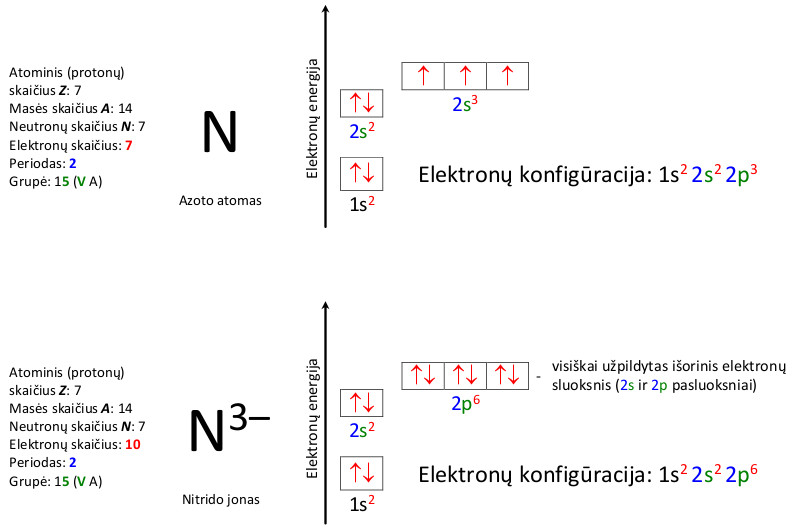
Deguonies atomo ir oksido jono elektronų konfigūracija
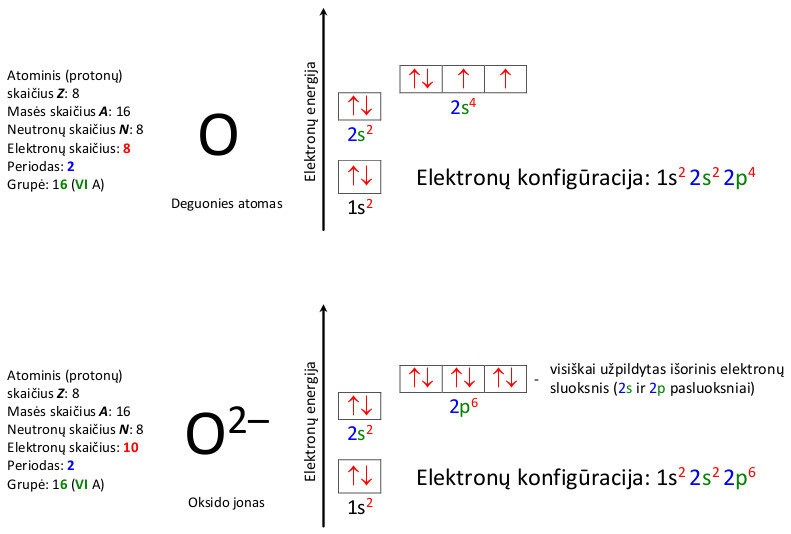
Fluoro atomo ir fluorido jono elektronų konfigūracija
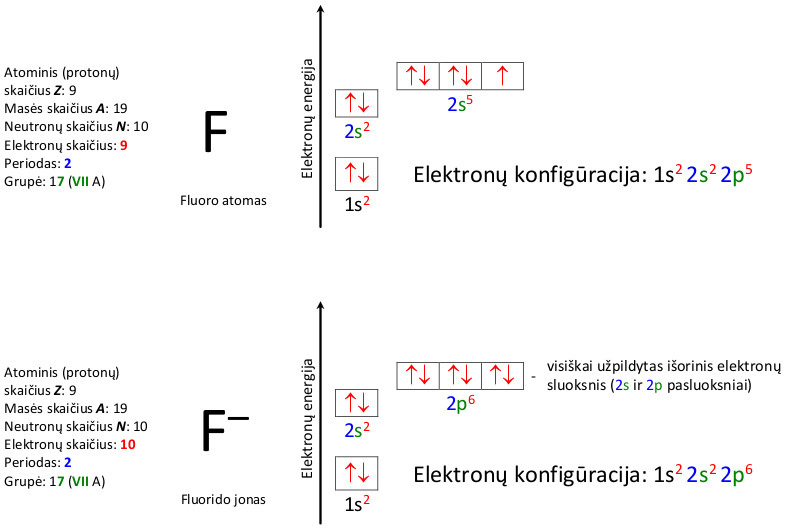
Natrio atomo ir jono elektronų konfigūracija
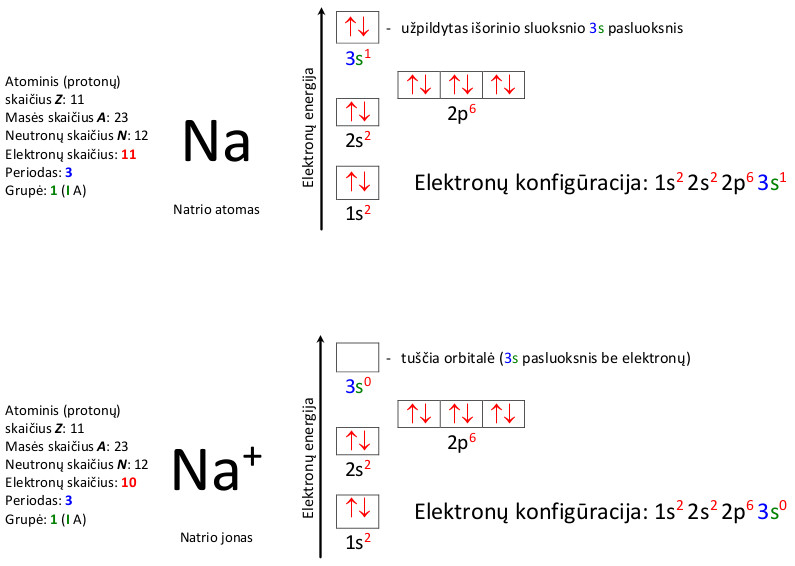
Magnio atomo ir jono elektronų konfigūracija

Aliuminio atomo ir fluorido jono elektronų konfigūracija
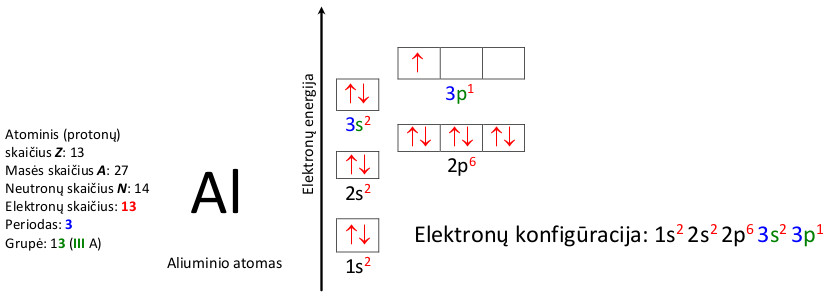
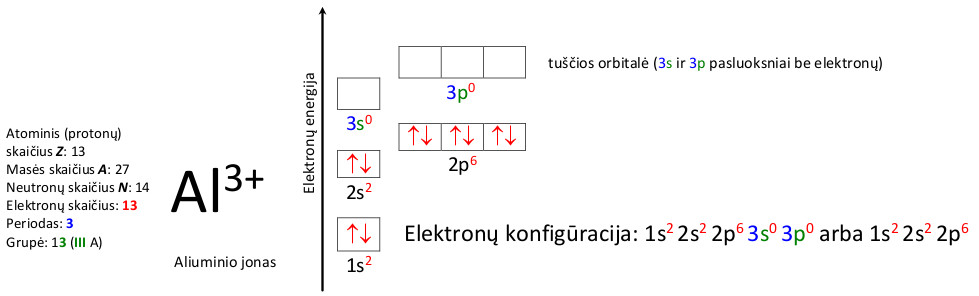
2.2. Periodinis dėsnis ir periodinė elementų lentelė
Periodinis dėsnis: cheminių elementų ir jų junginių savybės periodiškai kinta, priklausomai nuo elemento branduolio krūvio.
Periodinė elementų lentelė yra vizuali periodinio dėsnio – pačio svarbiausio chemijos dėsnio – išraiška. Kiekvienoje grupėje esančių cheminių elementų atomų išorinio sluoksnio elektroninė konfigūracija yra panaši, o tai sąlygoja ir panašias elementų chemines savybes.
Apie periodinę elementų lentelę plačiau skaitykite 2.2.1. poskyryje. Čia pateikiamoje periodinėje elementų lentelėje galite rasti kiekvieno elemento atomo elektroninę konfigūraciją – elektronų pasiskirstymo orbitalėse tvarką.
https://www.ptable.com/?lang=lt#Orbital
Periodinė elementų lentelė lietuviškai
2.2.1. Periodiškai kintančios cheminių elementų savybės periodinėje lentelėje
Periodinėje elementų lentelėje cheminiai elementai išdėstyti jų atominio skaičiaus didėjimo tvarka. Periodinės elementų lentelės horizontaliosios eilės vadinamos periodais, o vertikalūs stulpeliai – grupėmis.
Periodas prasideda šarminiu metalu ir baigiasi inertinėmis dujomis. Visi vieno periodo elementai turi tokį pat elektronų energijos lygmenų skaičių. Didėjant periodo numeriui, elementų atomai įgyja vienu energijos lygmeniu daugiau negu prieš tai esančio periodo elementų atomai. Kiekvieno periodo elemento atomai, einant iš kairės į dešinę, išoriniame energijos lygmenyje turi vienu elektronu daugiau negu prieš tai esančio elemento atomai.
Periode iš kairės į dešinę silpnėja metališkosios ir stiprėja nemetališkosios savybės. Kiekvieno periodo pradžioje esantys elementai pasižymi metališkosiomis savybėmis, o esantys periodo gale arti inertinių dujų – nemetališkosiomis savybėmis. Kiekviename periode, didėjant atomo elektronų skaičiui, atomo spindulys trumpėja.
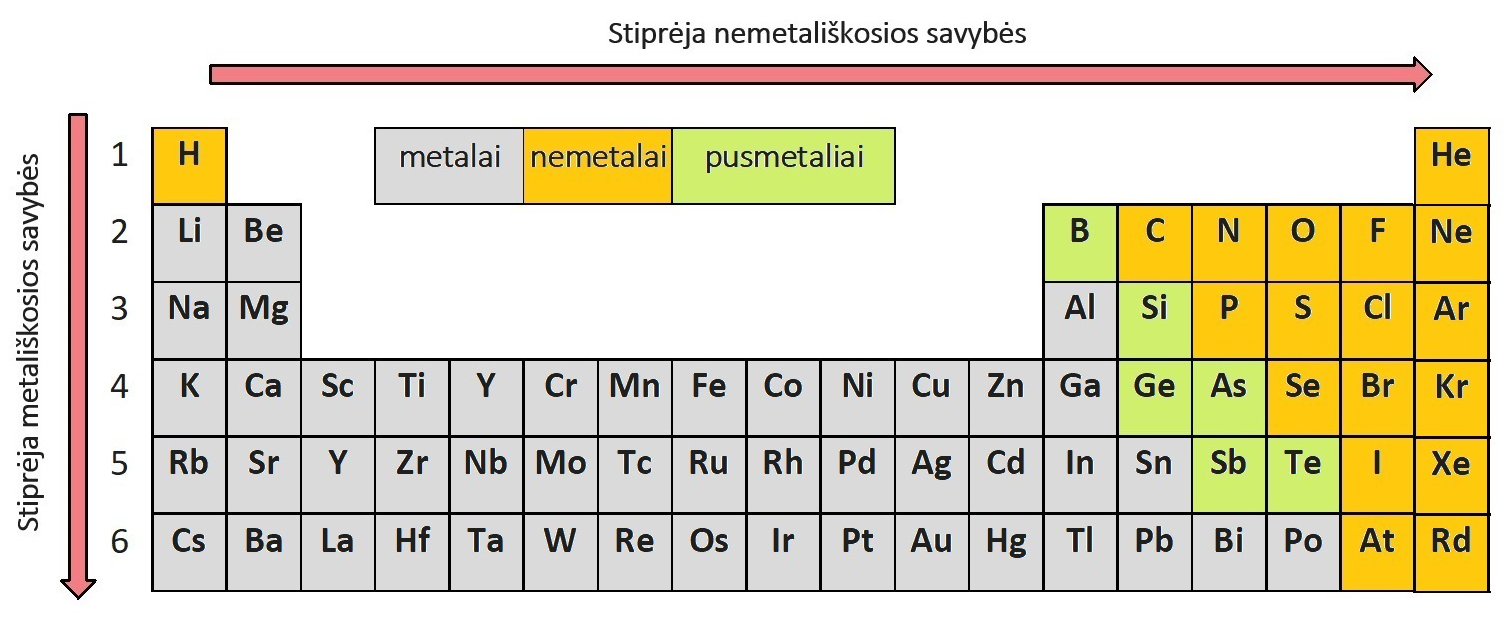
2.2.1. pav. Elementų metališkųjų ir nemetališkųjų savybių kitimas grupėse ir perioduose
Grupėse visi tos pačios grupės elementai išoriniame energijos lygmenyje turi vienodą skaičių elektronų, todėl jų cheminės savybės panašios. Grupės numeris rodo elektronų, galinčių sudaryti cheminius ryšius, skaičių.
Grupėse iš viršaus į apačią stiprėja metališkosios savybės ir silpnėja nemetališkosios savybės. Grupėse iš viršaus į apačią didėjant atomo branduolio krūviui ir elektronų lygmenų skaičiui, A grupių elementų atomų spinduliai ilgėja sparčiau negu B grupių elementų.
Grupės gali būti žymimos romėniškaisiais (nuo I iki VIII, prie kurių rašoma A arba B raidė) ar arabiškaisiais (nuo 1 iki 18) skaitmenimis. A raide žymimos pagrindinės grupės – tos, į kurias įeina 1-7 periodo elementai. Šalutines grupes sudaro tik 4–7 periodo elementai.
IA grupės elementai (išskyrus H) vadinami šarminiais metalais. IIA grupės metalai (išskyrus Be ir Mg) vadinami šarminių žemių metalais. VIIA grupės elementai – halogenais, o VIIIA grupės elementai – inertinėmis dujomis.

2.2.2.pav. Elementų atomų spindulių kitimas cheminių elementų sistemoje.
Metalų atomai yra didesni už nemetalų atomus. Kuo didesnis atomas, tuo toliau nuo branduolio yra valentiniai elektronai ir tuo lengviau atomas gali jų netekti. Visų cheminių elementų atomai, susidarant junginiams, stengiasi savo išoriniame energetiniame lygmenyje įgyti tokį elektronų skaičių, kokį turi arčiausiai jų periodinėje sistemoje esančios inertinės dujos.
Cheminiai elementai skirstomi į metalus, nemetalus ir pusmetalius.
Metalams būdinga aukšta lydymosi temperatūra, jie yra blizgus, kalūs, plastiški, laidūs elektrai ir šilumai. Visi metalai (išskyrus Hg, kuris yra skystas) kambario temperatūroje yra kieti. Chemiškai reaguodami metalai atiduoda elektronus ir virsta teigiamaisiais jonais (katijonais).
Nemetalai yra mažai laidūs elektrai ir šilumai, neblizgūs. Kambario temperatūroje nemetalai yra dujos (vandenilis, deguonis, azotas, floras, chloras), skysčiai (bromas) ar kietos medžiagos (anglis, jodas). Chemiškai reaguodami nemetalai prisijungia elektronus ir virsta neigiamaisiais jonais (anijonais).
Pusmetaliai – tai kristalinės medžiagos, pagal savitąjį elektroninį laidumą esančios tarp metalų ir puslaidininkių. Išvaizda pusmetaliai panašesni į metalus – tipiški pusmetaliai yra blizgūs. Jų cheminės savybės labiau panašios į nemetalų savybes.
2.2.2. Elektrinis neigiamumas
Elektrinis neigiamumas – dydis, nusakantis atomo gebėjimą prisitraukti atomo, su kuriuo jis yra sudaręs ryšį, elektronus.
Tai dar viena periodiškai kintanti cheminių elementų savybė.
Elektrinis neigiamumas tiesiogiai neišmatuojamas. Plačiausiai naudojama Polingo santykinio elektronų neigiamumo skalė.
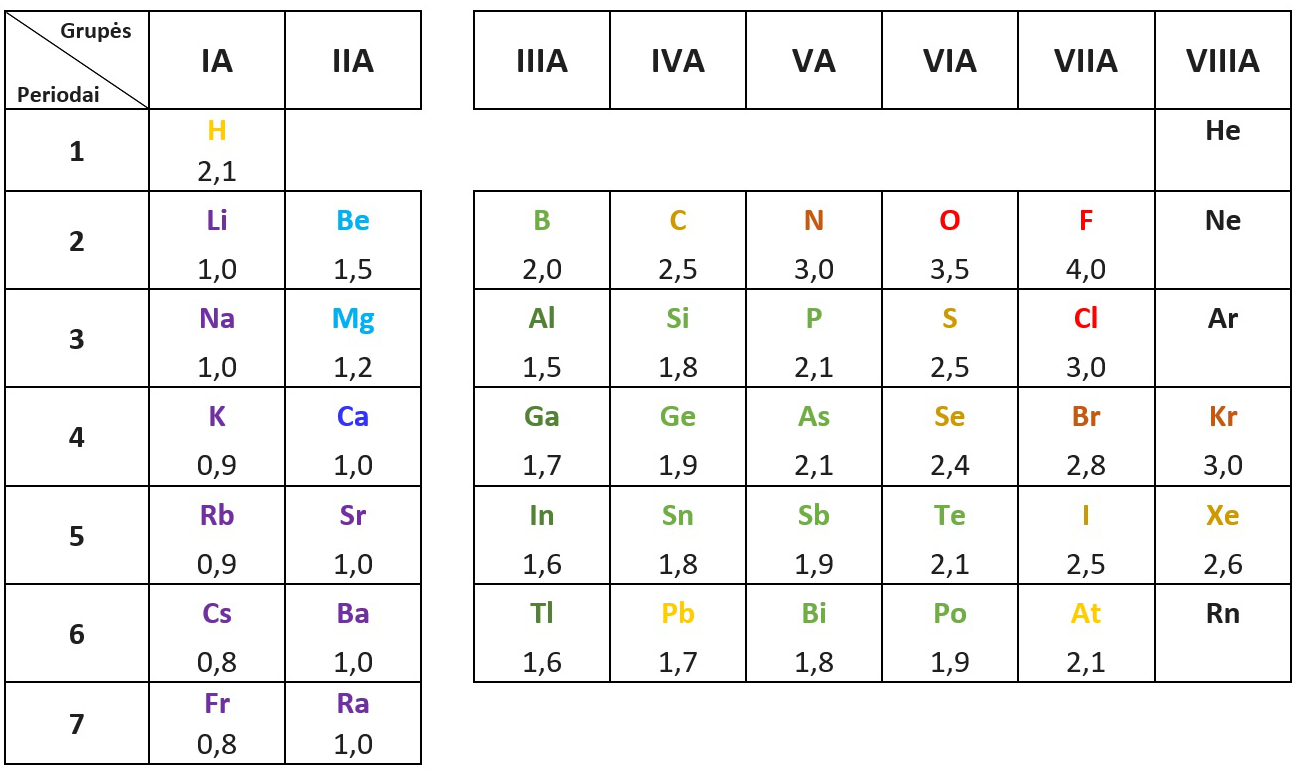
2.2.3. pav. Pagrindinių grupių cheminių elementų elektrinis neigiamumas santykiniais vienetais
2.2.3. Metalai, nemetalai ir pusmetaliai
Cheminiai elementai skirstomi į metalus, nemetalus ir pusmetalius.
Metalams būdinga aukšta lydymosi temperatūra, jie yra blizgus, kalūs, plastiški, laidūs elektrai ir šilumai. Visi metalai (išskyrus Hg, kuris yra skystas) kambario temperatūroje yra kieti. Chemiškai reaguodami metalai atiduoda elektronus ir virsta teigiamaisiais jonais (katijonais).
Nemetalai yra mažai laidūs elektrai ir šilumai, neblizgūs. Kambario temperatūroje nemetalai yra dujos (vandenilis, deguonis, azotas, floras, chloras), skysčiai (bromas) ar kietos medžiagos (anglis, jodas). Chemiškai reaguodami nemetalai prisijungia elektronus ir virsta neigiamaisiais jonais (anijonais).
Pusmetaliai – tai kristalinės medžiagos, pagal savitąjį elektroninį laidumą esančios tarp metalų ir puslaidininkių. Išvaizda pusmetaliai panašesni į metalus –tipiški pusmetaliai yra blizgūs. Jų cheminės savybės labiau panašios į nemetalų savybes.
Aktyviausi metalai yra kairiajame apatiniame periodinės lentelės kampe. Aktyvių metalų:
- dideli atomai;
- mažos jonizacijos energijos (lengvai atiduoda valentinius elektronus);
- maži elektriniai neigiamumai.
Aktyviausi nemetalai yra dešiniajame viršutiniame periodinės lentelės kampe. Aktyviausių nemetalų:
- maži atomai;
- didelės jonizacijos energijos (jie nelinkę atiduodi valentinių elektronų);
- dideli elektriniai neigiamumai (sudarydami cheminius ryšius, elektronus patraukia į save).
2.3. Cheminiai ryšiai
Cheminis ryšys – atomų savitarpio sąveika, dėl kurios susidaro molekulė arba kristalas.
Susidarant cheminiam ryšiui, persidengia atominės orbitalės, kuriose yra valentinių elektronų.
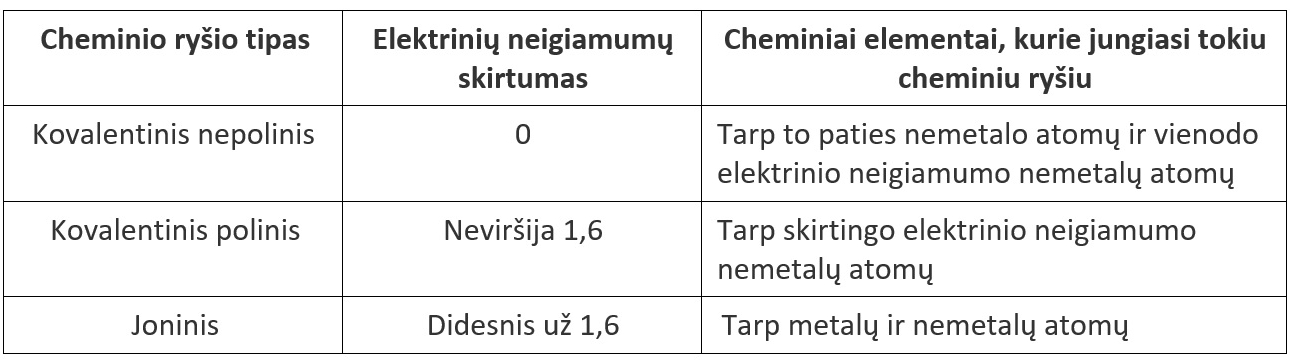
Cheminio ryšio tipas priklauso nuo cheminių elementų, sudarančių ryšį, elektrinio neigiamumo skirtumo (2.3.1. lentelė).
2.3.1. lentelė. Cheminio ryšio tipo priklausomybė nuo cheminių elementų, sudarančių ryšį, elektrinio neigiamumo skirtumo
Cheminis ryšys – atomų savitarpio sąveika, dėl kurios susidaro molekulė arba kristalas.
Susidarant cheminiam ryšiui, persidengia atominės orbitalės, kuriose yra valentinių elektronų.
Cheminio ryšio tipas priklauso nuo cheminių elementų, sudarančių ryšį, elektrinio neigiamumo skirtumo (2.3.1. lentelė).
2.3.1. lentelė. Cheminio ryšio tipo priklausomybė nuo cheminių elementų, sudarančių ryšį, elektrinio neigiamumo skirtumo

Cheminis ryšys – atomų savitarpio sąveika, dėl kurios susidaro molekulė arba kristalas.
Susidarant cheminiam ryšiui, persidengia atominės orbitalės, kuriose yra valentinių elektronų.
Cheminio ryšio tipas priklauso nuo cheminių elementų, sudarančių ryšį, elektrinio neigiamumo skirtumo (2.3.1. lentelė).
2.3.1. lentelė. Cheminio ryšio tipo priklausomybė nuo cheminių elementų, sudarančių ryšį, elektrinio neigiamumo skirtumo

Cheminis ryšys – atomų savitarpio sąveika, dėl kurios susidaro molekulė arba kristalas.
Susidarant cheminiam ryšiui, persidengia atominės orbitalės, kuriose yra valentinių elektronų.
Cheminio ryšio tipas priklauso nuo cheminių elementų, sudarančių ryšį, elektrinio neigiamumo skirtumo (2.3.1. lentelė).
2.3.1. lentelė. Cheminio ryšio tipo priklausomybė nuo cheminių elementų, sudarančių ryšį, elektrinio neigiamumo skirtumo

2.3.1. Joninis ryšys
Joninis ryšys – tai cheminis ryšys, kuris susidaro veikiant priešingo krūvio jonų elektrostatinėms traukos jėgoms.
Susidarant joniniam ryšiui, vienas atomas savo elektronus atiduoda kitam ir jie abu virsta jonais. Tokį ryšį gali sudaryti didelį elektrinių neigiamumų skirtumą turintys atomai, t.y. metalų (virsta katijonais) ir nemetalų (virsta anijonais) atomai.
Joninis ryšys – tai cheminis ryšys, kuris susidaro veikiant priešingo krūvio jonų elektrostatinėms traukos jėgoms.
Susidarant joniniam ryšiui, vienas atomas savo elektronus atiduoda kitam ir jie abu virsta jonais. Tokį ryšį gali sudaryti didelį elektrinių neigiamumų skirtumą turintys atomai, t.y. metalų (virsta katijonais) ir nemetalų (virsta anijonais) atomai.
Pavyzdžiui, natrio atomas atiduoda vieną valentinį elektroną chloro atomui ir virsta natrio jonu, o chloro atomas prisijungia vieną elektroną ir virsta chlorido jonu:
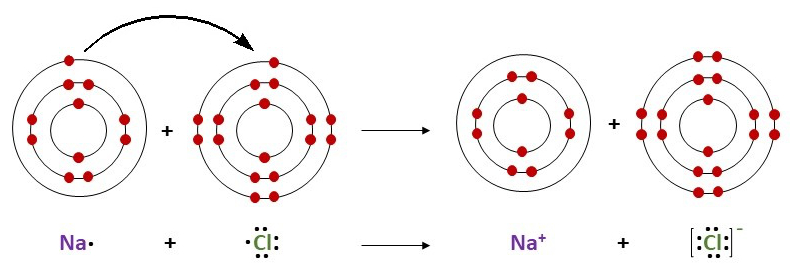
2.3.1. pav. Natrio ir chlorido jonų susidarymas
Abu jie įgyja stabiliąją energetinę būseną (oktetą) – artimiausių inertinių dujų atomo elektronų konfigūraciją.
Priešingo ženklo jonai traukia vieni kitus, o vienodo – stumia. Jonai išsidėsto tam tikra tvarka, vadinama joniniu kristalu, kad šios jėgos kompensuotų vienos kitas. Joniniuose junginiuose neįmanoma išskirti atskiros jonų grupės, kurią būtų galima pavadinti molekule, nes joniniame kristale jonai sąveikauja su visais juos supančiais jonais.
Junginiai, kuriuose elementų atomai yra sujungti joniniu ryšiu, vadinami joniniais junginiais.
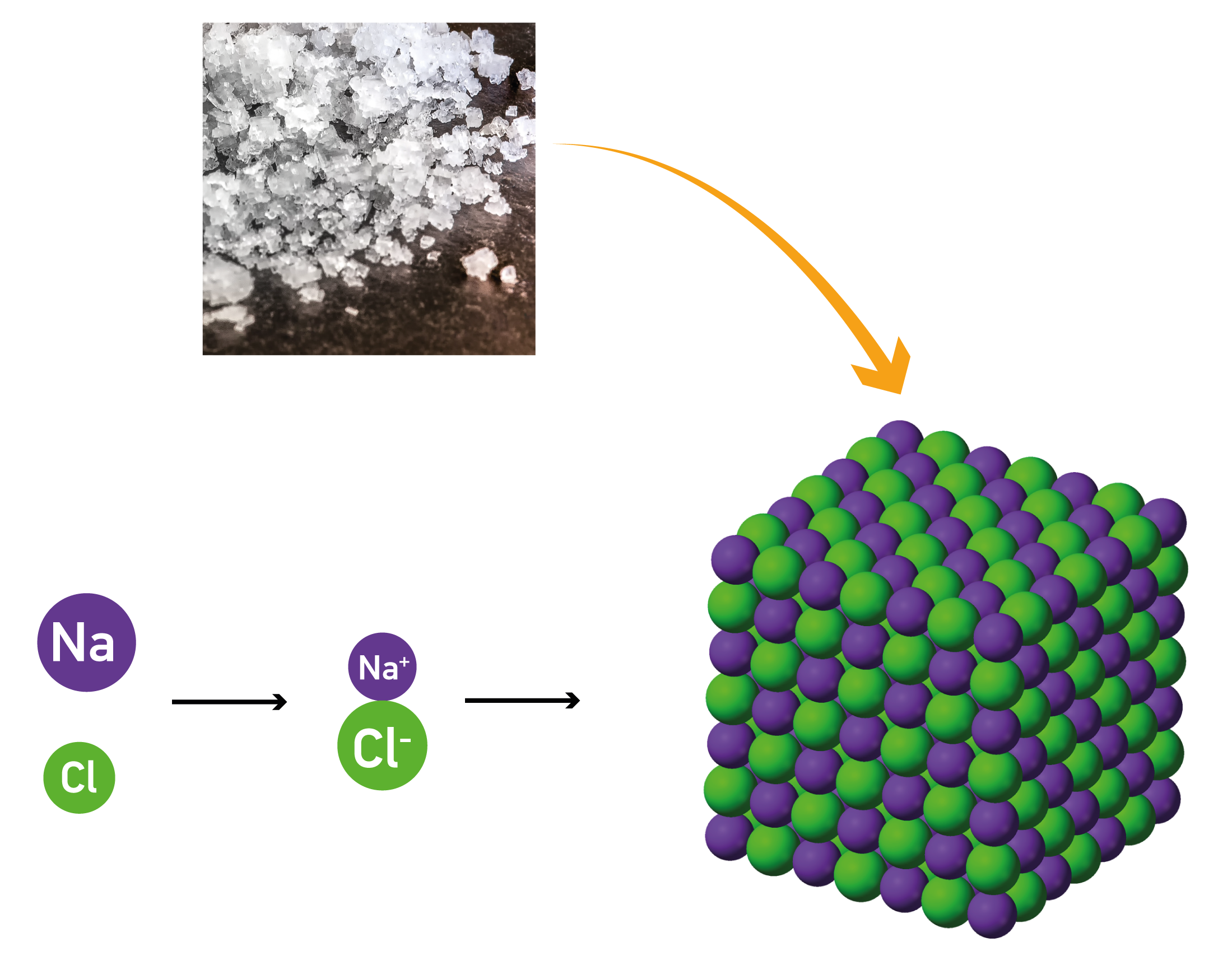
2.3.2. pav. NaCl susidarymas
NaCl kristale kiekvieną Na+ joną supa šeši Cl- jonai, o kiekvieną Cl- joną supa šeši Na+ jonai.
Joninį ryšį sudaro IA-IIIA grupių metalai su VA-VIIA grupių nemetalais, nes šių elementų atomai yra linkę sudaryti stabilią užpildytą elektroninę konfigūraciją. Pavyzdžiui, suartėjus tipinio metalo kalio (K) ir tipinio nemetalo fluoro (F) jonams, kalio atomas atiduoda elektroną ir virsta K+ jonu, o fluoras prisijungia elektroną ir virsta F- jonu. Dėl traukos jėgų šie priešingo krūvio jonai sudaro joninį ryšį.
Joninis ryšys būdingas druskoms, kai kuriems oksidams ir hidroksidams.
2.3.2. Kovalentinis ryšys
Kovalentinis ryšys – tai cheminis ryšys, kai elektronai tampa bendri abiems atomams, t.y. susidaro bendra valentinių elektronų pora. Susijungus atomams kovalentiniu ryšiu, jų išoriniuose energijos lygmenyse susidaro po 8 elektronus, įskaitant bendros poros elektronus. Kovalentinis ryšys dažniausiai jungia nemetalų (vienodo ar artimo elektrinio neigiamumo) atomus.
Junginiai, kuriuose elementų atomai yra susijungę kovalentiniais ryšiais, yra vadinami kovalentiniais junginiais. Kovalentiniai junginiai dažniausiai yra molekulinės sandaros junginiai. Šiuo atveju egzistuoja atskiros atomų grupės, turinčios visas chemines tos medžiagos savybes. Kovalentinis ryšys yra būdingas visiems organiniams ir daugeliui neorganinių junginių. Bendra elektronų pora, sudaranti kovalentinį ryšį, molekulės struktūrinėje formulėje yra žymima brūkšneliu.
Atomai kovalentiniu ryšiu gali būti susijungę vieninėse medžiagose, pavyzdžiui, H2. Kiekvienas vandenilio atomas gauna po antrą elektroną ir įgyja stabilią artimiausių inertinių dujų – helio – elektronų konfigūraciją:
![]()
Kovalentinio ryšio susidarymas tarp dviejų chloro atomų, susidarant Cl2 molekulei, gali būti pavaizduota panašiai:
![]()
Šiuo atveju kiekvienas chloro atomas turi 8 elektronus.
Sudėtinėse medžiagose atomai taip pat jungiasi kovalentiniu ryšiu, pavyzdžiui, HF, H2O, NH3:
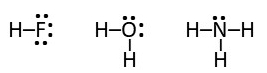
Jei atomai dalinasi viena elektronų pora, susidaro viengubas ryšys (žymimas vienu brūkšneliu). Tarp atomų gali susidaryti ir dvigubi (atomai dalinasi dviem elektronų poromis, žymima dvigubu brūkšniu) ar trigubi (atomai dalinasi trimis elektronų poromis, žymima trigubu brūkšniu) ryšiai:
![]()
![]()
Kovalentinis ryšys gali būti polinis ir nepolinis.
Kovalentinis nepolinis ryšys susidaro tada, kai ryšį sudaranti elektronų pora vienodai priklauso abiem ryšį sudarantiems atomams, t.y. yra simetriškai nutolusi nuo abiejų atomų branduolių. Kovalentinis nepolinis ryšys susidaro, kai jungiasi to paties cheminio elemento atomai (jų elektrinių neigiamumų reikšmės yra vienodos ir jų skirtumas lygus nuliui).

Kovalentinis polinis ryšys susidaro, kai ryšį sudaranti elektronų pora yra pasislinkusi arčiau to atomo, kurio elektrinis neigiamumas didesnis (žr. 2.2.2. sk.). Kovalentinis polinis ryšys susidaro, kai jungiasi skirtingo elektrinio neigi.amumo elementų atomai.

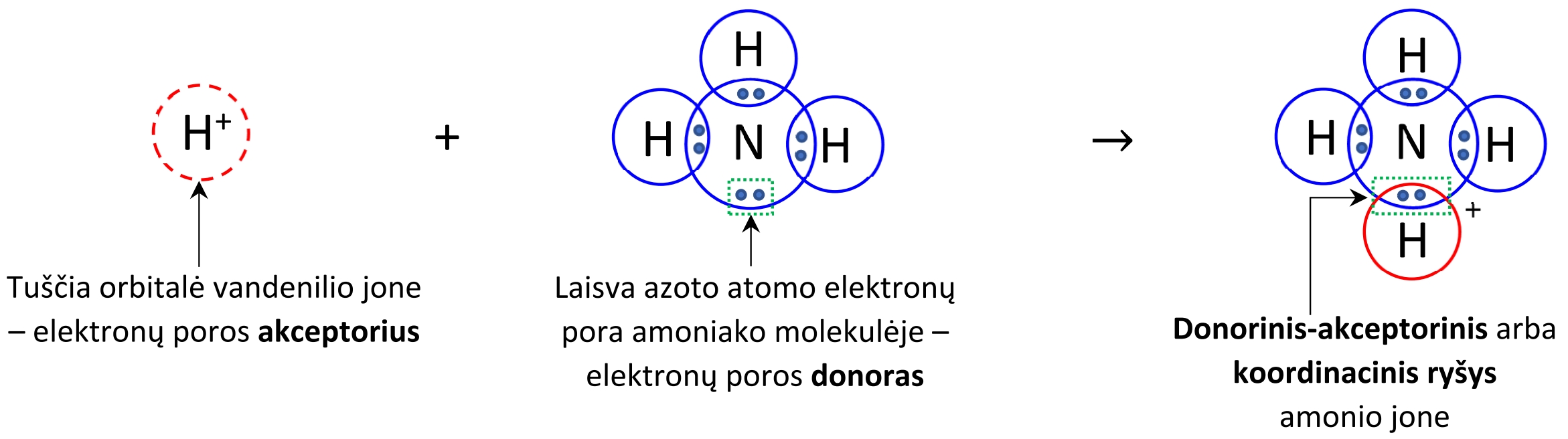
Koordinacinis ryšys, donorinis-akceptorinis ryšys - cheminis ryšys, kuris susidaro tada, kai ryšio elektronus duoda tik vienas iš ryšį sudarančių atomų. Atomas arba jonas, turintis išoriniame energiniame lygmenyje (sluoksnyje) laisvąją elektronų porą, sudarančią koordinacinį ryšį, vadinamas donoru, o atomas arba jonas, priimantis į savo išorinį energinį lygmenį (sluoksnį) šią porą, vadinamas akceptoriumi. Todėl koordinacinis ryšys dar vadinamas donoro-akceptoriniu ryšiu.
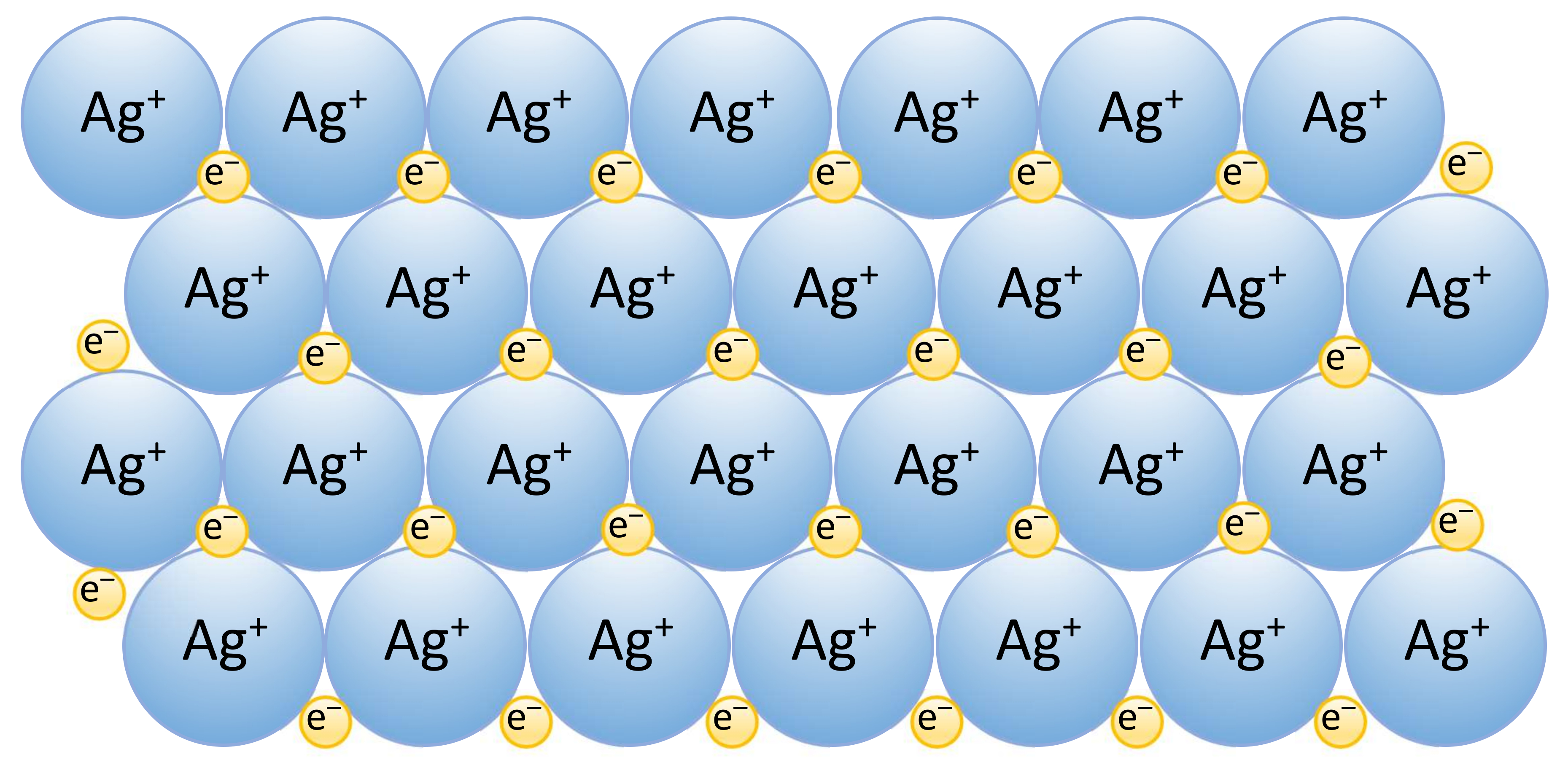
2.3.3. Metališkasis ryšys
Metališkasis ryšys pasireiškia tik tarp metalo atomų ir jonų. Šis ryšys jungia metalų jonus metalų kristaluose. Metalai yra geri šilumos ir elektros laidininkai, plastiški. Daugumos jų lydymosi ir virimo temperatūros yra aukštos arba labai aukštos. Dėl savo vidinės struktūros metalai, išskyrus Hg, įprastinėmis sąlygomis yra kietos kristalinės medžiagos. Jų gardelėse taisyklingai išsidėstę teigiamieji jonai, o tarp jų juda elektronai. Metalų atomuose yra daug laisvųjų orbitalių, kurios susinėrusios su gretimų atomų laisvosiomis orbitalėmis sudaro daugiacentrines atomines orbitales, apimančias visą metalo kristalą. Taigi kiekvieno metalo atomo valentiniai elektronai yra susiję ne su vienu branduoliu, o yra bendri visiems metalo atomams ir laisvai juda visame metalo tūryje (ne tik atskiruose kristaluose, bet ir tarp besiliečiančių kristalų!!!). Ši laisvųjų elektronų ir atomų teigiamųjų jonų elektrostatinė sąveika ir lemia stiprias ryšio jėgas tarp metalų atomų, būdingas metališkajam ryšiui. Metališkasis ryšys būdingas tik kietosios ir skystosios būsenos metalams. Dėl bendrų elektronų judėjimo metalų kristaluose jie yra kieti, tačiau lengvai plastiškai deformuojasi juos tempiant, gniuždant, lenkiant ar kitaip veikiant mechaniškai.
2.3.4. Cheminiai ryšiai daugiaatomiuose jonuose
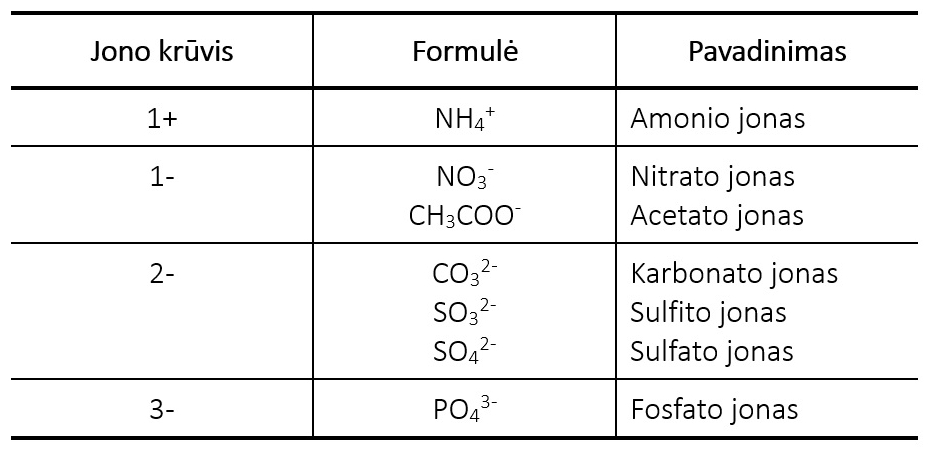
Keletas katijonų ir daugelis įprastų anijonų yra daugiaatomiai jonai. Pavyzdžiui, amonio jonas NH4+ arba nitrato (NO3-), karbonato (CO32-) ir fosfato jonai (PO43-).
Svarbu suprasti, kad šiuo atveju kovalentiniu ryšiu susijungusių atomų grupės sudaro stabilius krūvį turinčius jonus, kurie gali sudaryti joninį ryšį su kitais jonais.
2.3.2. lentelė. Daugiaatomiai jonai
2.3.5. Junginių formulių rašymas
Junginys, susidarantis jonams jungiantis tarpusavyje, yra neutralus. Taigi, teigiamą krūvį turinčių jonų ir neigiamą krūvį turinčių jonų krūvių suma turi būti lygi 0.
Junginių formulėse rašomi koeficientai, kurie nurodo konkrečių jonų skaičių junginyje. Daugiaatomiai jonai rašomi skliausteliuose, o koeficientas, nurodantis jų skaičių, – už skliaustelio. Rašant junginių formules, būtina įsitikinti, kad teigiamo krūvio suma yra lygi neigiamo krūvio sumai.
Pavyzdžiui, susidarant natrio karbonatui Na2CO3, turi susijungti du natrio jonai Na+ ir vienas karbonato jonas CO32- – tik tokiu atveju teigiamų krūvių ir neigiamų krūvių suma bus lygi 0. Kalcio nitrato Ca(NO3)2 formulėje daugiaatomis nitrato jonas NO3- rašomas skliausteliuose ir už jų esantis koeficientas 2 nurodo, kad du tokie jonai, kurių kiekvieno krūvis yra 1-, susijungia su vienu kalcio jonu Ca2+, kurio krūvis 2+.
2.4. Vandenilinis ryšys
Vandenilinis ryšys – ryšys tarp laisvąją elektronų porą turinčio labai elektriškai neigiamo atomo (N, O, F) ir vandenilio atomo, prisijungusio prie kito labai elektriškai neigiamo atomo (N, O, F).
Ryšiai N–H, O–H ir F–H yra labai poliški. Juose ryšį sudaranti bendroji elektronų pora yra ženkliai pasislinkusi link N, O ar F atomo, kuris įgyja dalinį neigiamą krūvį, o H atomas įgyja dalinį teigiamą krūvį (pasidaro panašus į H+ joną) ir gali sudaryti vandenilinį ryšį su kitoje molekulėje esančio N, O ar F atomo laisvąja elektronų pora. Dažniausiai vandenilinis ryšys susidaro tarp skirtingų molekulių. Todėl jis vadinamas tarpmolekuline sąveika.
Vandenilinis ryšys schemose žymimas punktyrine linija, taip parodant, kad jis yra silpnesnis nei ryšiai molekulės viduje.
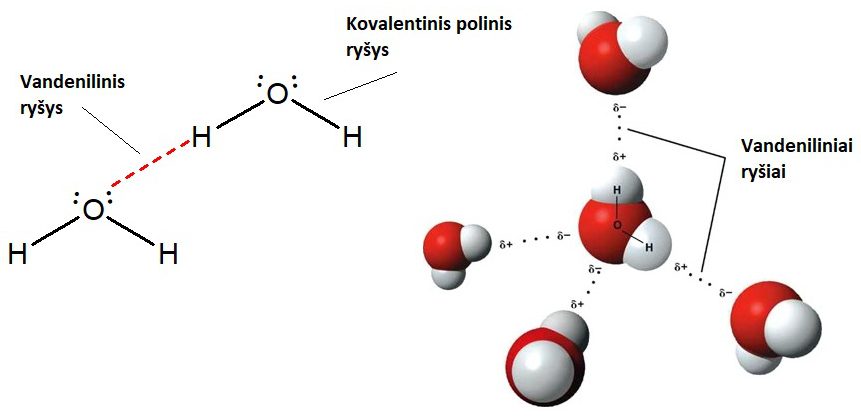
2.4.1. pav. Vandeniliniai ryšiai tarp vandens molekulių (paveikslas adaptuotas iš https://en.wikipedia.org/wiki/Hydrogen_bond)
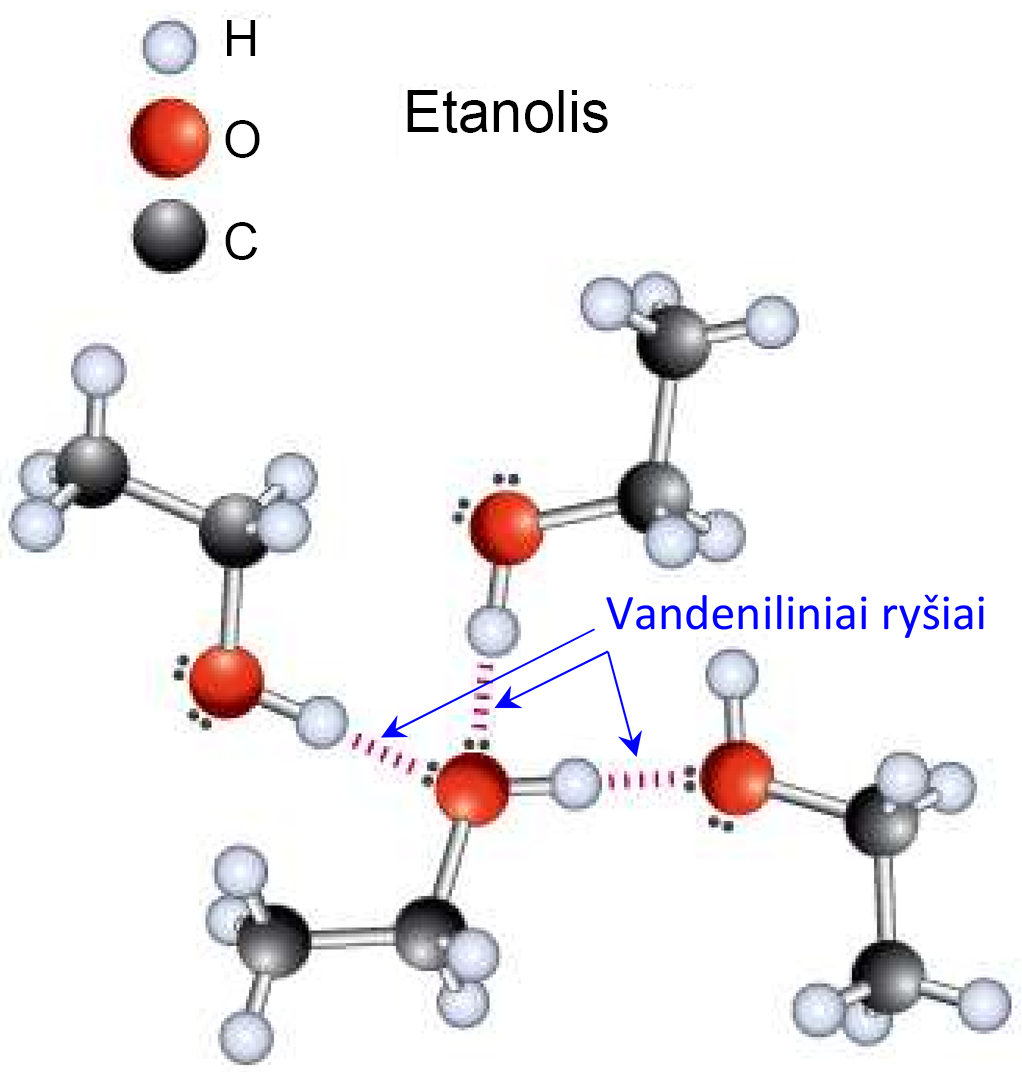
2.4.2. pav. Vandeniliniai ryšiai tarp etanolio molekulių
Kartais vandenilinis ryšys gali susidaryti ir toje pačioje molekulėje tarp skirtingų jos dalių (intramolekulinis vandenilinis ryšys)
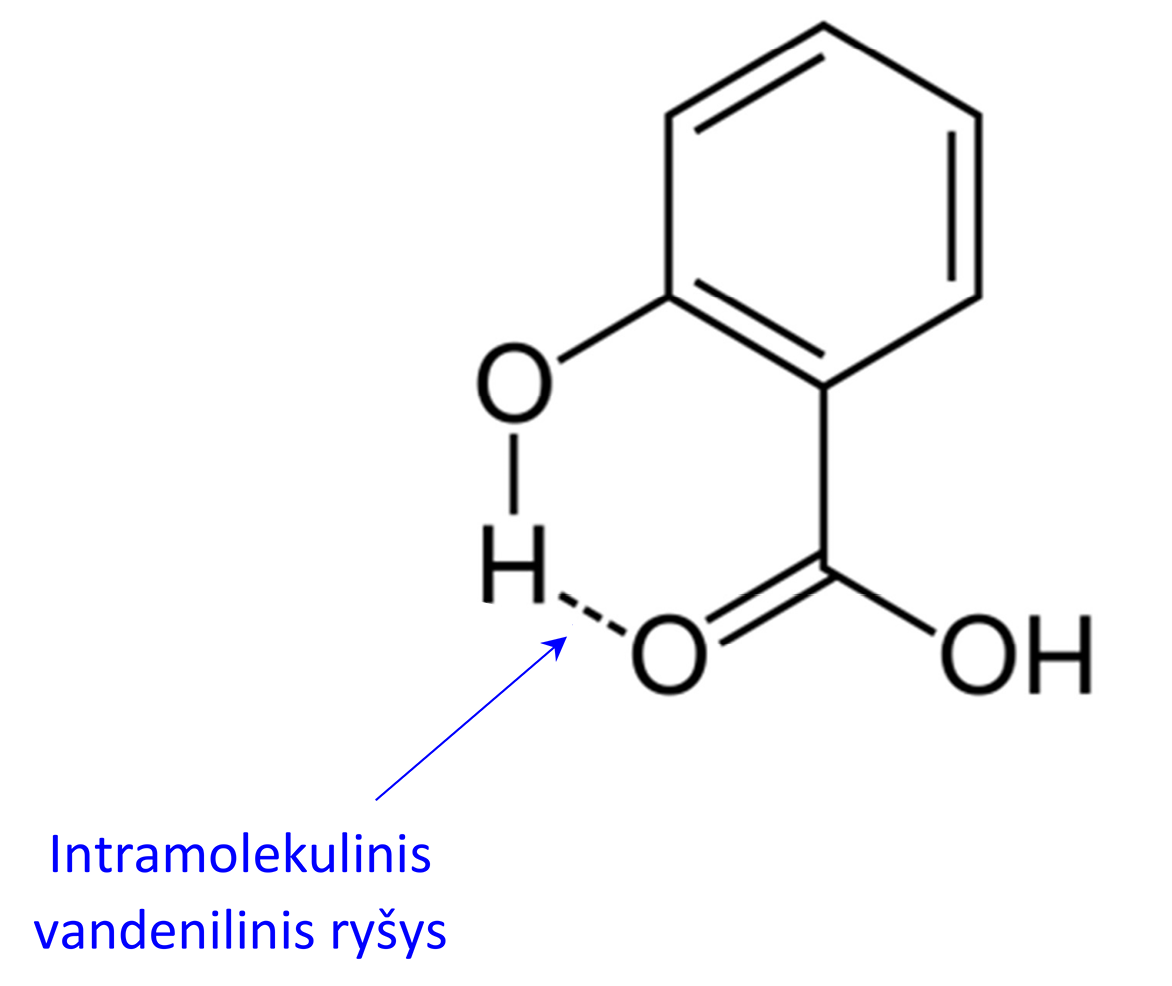
2.4.3. pav. Intramolekulinis vandenilinis ryšys 2-hidroksibenzenkarboksirūgšties (salicilo rūgšties) molekulėje
Jei nebūtų vandenilinių ryšių, nebūtų ir gyvybės žemėje. Standartinėmis sąlygomis (STP) vanduo būtų dujinėje būsenoje. Kuo mažesnė molekulių masė, tuo yra žemesnės iš jų sudarytų medžiagų lydymosi ir virimo temperatūros. Dėl vandenilinių ryšių hidridų NH3, H2O ir HF lydymosi ir virimo temperatūros yra neįprastai aukštos. Taigi, standartinėmis sąlygomis vanduo yra skystojoje būsenoje.
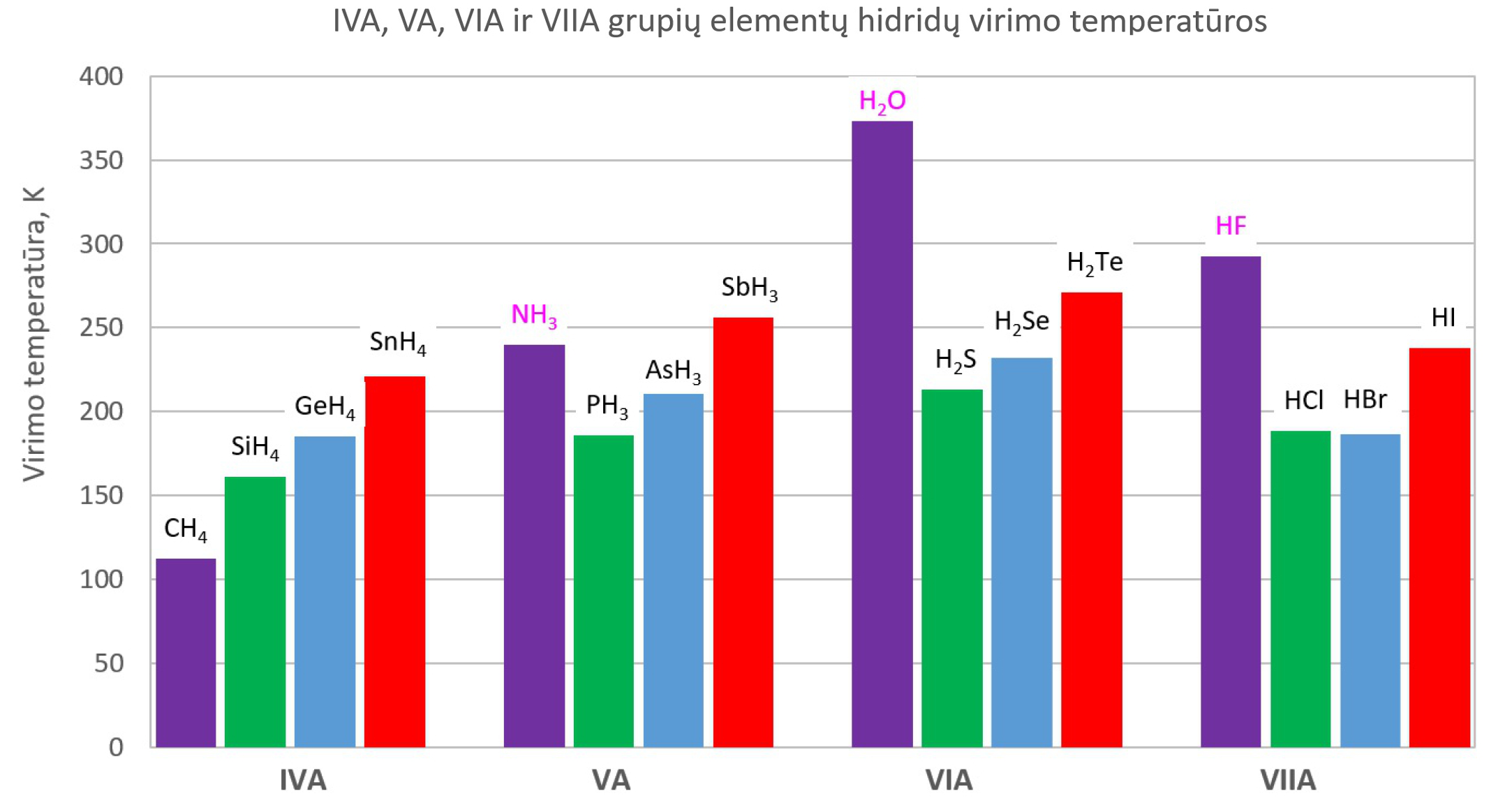
2.4.4. pav. IVA, VA, VIA ir VIIA grupių elementų hidridų virimo temperatūros
Vandenilinių ryšių dėka baltymai ir kitos didelės gyvybei svarbios molekulės išlaiko savo struktūrą ir gali atlikti svarbias funkcijas biochemijoje. Deoksiribonukleorūgšties (DNR), kurioje yra užkoduota visa genetinė informacija, molekulė yra sudaryta iš dviejų į spiralę susisukusių polinukleotidinių grandinių, kurias kartu laiko vandeniliniai ryšiai.