Teorinė medžiaga su pavyzdžiais
2.3. Cheminiai ryšiai
2.3.2. Kovalentinis ryšys
Kovalentinis ryšys – tai cheminis ryšys, kai elektronai tampa bendri abiems atomams, t.y. susidaro bendra valentinių elektronų pora. Susijungus atomams kovalentiniu ryšiu, jų išoriniuose energijos lygmenyse susidaro po 8 elektronus, įskaitant bendros poros elektronus. Kovalentinis ryšys dažniausiai jungia nemetalų (vienodo ar artimo elektrinio neigiamumo) atomus.
Junginiai, kuriuose elementų atomai yra susijungę kovalentiniais ryšiais, yra vadinami kovalentiniais junginiais. Kovalentiniai junginiai dažniausiai yra molekulinės sandaros junginiai. Šiuo atveju egzistuoja atskiros atomų grupės, turinčios visas chemines tos medžiagos savybes. Kovalentinis ryšys yra būdingas visiems organiniams ir daugeliui neorganinių junginių. Bendra elektronų pora, sudaranti kovalentinį ryšį, molekulės struktūrinėje formulėje yra žymima brūkšneliu.
Atomai kovalentiniu ryšiu gali būti susijungę vieninėse medžiagose, pavyzdžiui, H2. Kiekvienas vandenilio atomas gauna po antrą elektroną ir įgyja stabilią artimiausių inertinių dujų – helio – elektronų konfigūraciją:
![]()
Kovalentinio ryšio susidarymas tarp dviejų chloro atomų, susidarant Cl2 molekulei, gali būti pavaizduota panašiai:
![]()
Šiuo atveju kiekvienas chloro atomas turi 8 elektronus.
Sudėtinėse medžiagose atomai taip pat jungiasi kovalentiniu ryšiu, pavyzdžiui, HF, H2O, NH3:
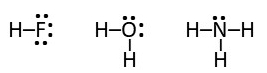
Jei atomai dalinasi viena elektronų pora, susidaro viengubas ryšys (žymimas vienu brūkšneliu). Tarp atomų gali susidaryti ir dvigubi (atomai dalinasi dviem elektronų poromis, žymima dvigubu brūkšniu) ar trigubi (atomai dalinasi trimis elektronų poromis, žymima trigubu brūkšniu) ryšiai:
![]()
![]()
Kovalentinis ryšys gali būti polinis ir nepolinis.
Kovalentinis nepolinis ryšys susidaro tada, kai ryšį sudaranti elektronų pora vienodai priklauso abiem ryšį sudarantiems atomams, t.y. yra simetriškai nutolusi nuo abiejų atomų branduolių. Kovalentinis nepolinis ryšys susidaro, kai jungiasi to paties cheminio elemento atomai (jų elektrinių neigiamumų reikšmės yra vienodos ir jų skirtumas lygus nuliui).

Kovalentinis polinis ryšys susidaro, kai ryšį sudaranti elektronų pora yra pasislinkusi arčiau to atomo, kurio elektrinis neigiamumas didesnis (žr. 2.2.2. sk.). Kovalentinis polinis ryšys susidaro, kai jungiasi skirtingo elektrinio neigi.amumo elementų atomai.

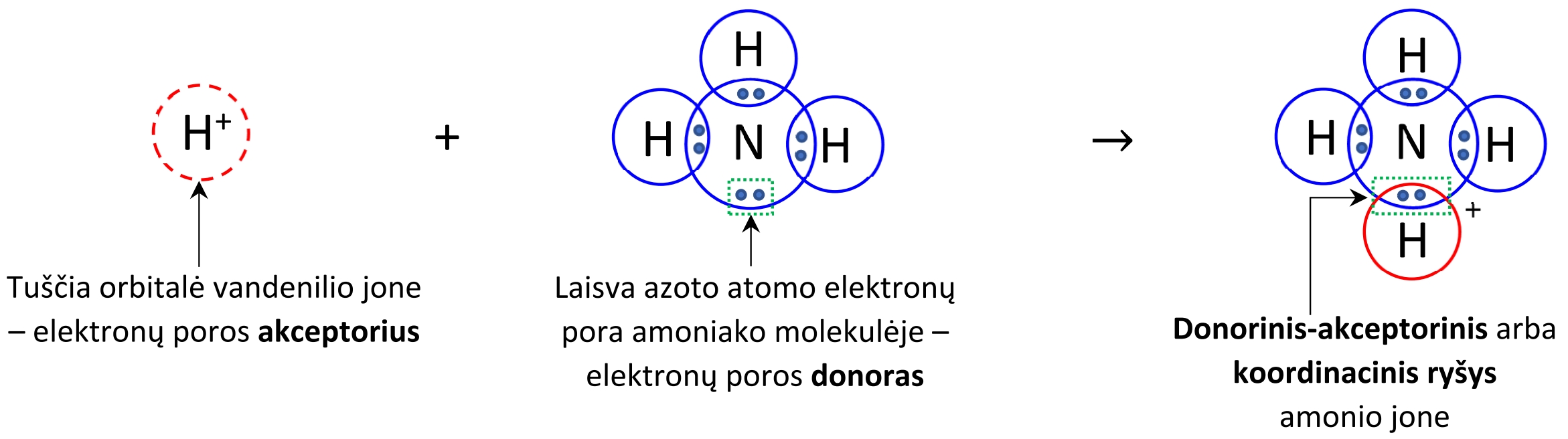
Koordinacinis ryšys, donorinis-akceptorinis ryšys - cheminis ryšys, kuris susidaro tada, kai ryšio elektronus duoda tik vienas iš ryšį sudarančių atomų. Atomas arba jonas, turintis išoriniame energiniame lygmenyje (sluoksnyje) laisvąją elektronų porą, sudarančią koordinacinį ryšį, vadinamas donoru, o atomas arba jonas, priimantis į savo išorinį energinį lygmenį (sluoksnį) šią porą, vadinamas akceptoriumi. Todėl koordinacinis ryšys dar vadinamas donoro-akceptoriniu ryšiu.