Uždavinių sprendimo pavyzdžiai
1. Iškaitinus 4,56 g magnio sulfato kristalohidrato MgSO4 · nH2O, gauta 2,4 g bevandenio magnio sulfato. Kokia šio kristalohidrato formulė?
M(MgSO4) = 24 + 32 + 16 ·2 = 120 g/mol
Apskaičiuojame kristalohidrato molio masę:
4,56 g kristalohidrato – 2,4 g bevandenio sulfato
x g – 120 g

M(MgSO4 · nH2O) = 228 g/mol
m(nH2O) = 228 g – 120 g = 108 g
M(H2O) = 18 g/mol
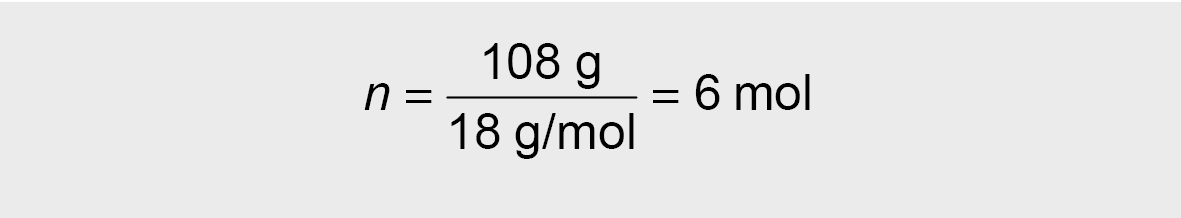
Ats.: kristalohidrato formulė yra MgSO4 · 6 H2O.
2. Kiek molių NaCl bus 500-se g valgomosios druskos?
M(NaCl) = 23 +35,5 = 58,5 g/mol

Ats.: bus 8,54 moliai NaCl
3. Kurią masės dalį korunde Al2O3 sudaro aliuminis?
Mr(Al2O3) = 27 · 2 + 16 ·2 = 102
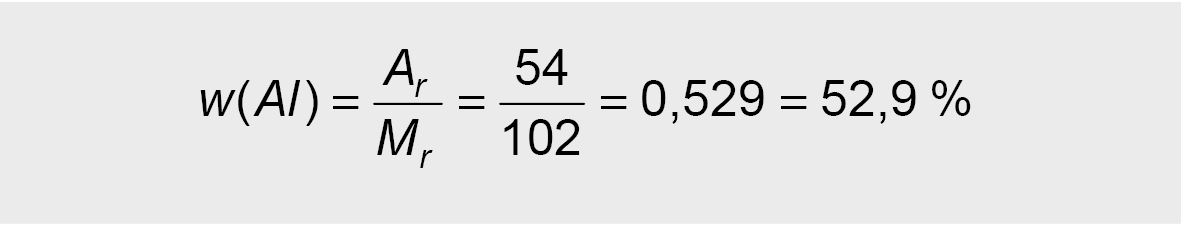
Ats.: aliuminio yra 52,9 %.
4. Viename litre vandens ištirpinome 0,3 kg cukraus. Apskaičiuokite, kurią masės dalį tirpale sudaro cukrus.
m(tirpalo) = 1 kg tirpiklio + 0,3 kg tirpinio = 1,3 kg

Ats.: cukrus tirpale sudaro 23,1 %.
