Pagrindinės chemijos sąvokos ir dėsniai
1.1. Pagrindinės sąvokos
CHEMIJA
MOKSLAS,
NAGRINĖJANTIS MEDŽIAGŲ SAVYBES, JŲ SUDĖTĮ BEI SANDARĄ IR VIENŲ MEDŽIAGŲ VIRTIMĄ
KITOMIS.
Atomas – mažiausia cheminio elemento dalelė, turinti visas jo chemines ir fizikines savybes. Jis yra elektriškai neutralus ir chemiškai nedalomas.
Atomas sudarytas iš branduolio (protonų bei neutronų) ir apie jį skriejančių elektronų (žr. temoje „Atomo sandara“).
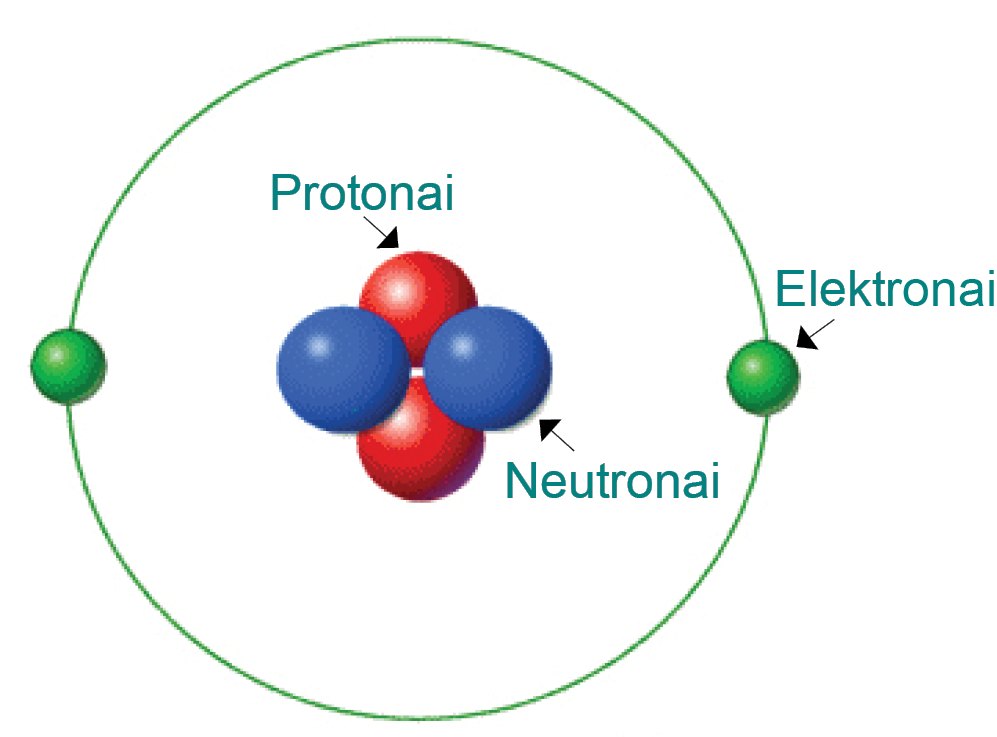
Helis
Molekulė – mažiausia medžiagos dalelė, turinti tos medžiagos chemines savybes. Molekulė susideda iš to paties atomo arba skirtingų cheminių elementų atomų ir egzistuoja kaip vientisa atomo branduolių ir elektronų sistema. Elektriškai neutrali.
Pvz.: 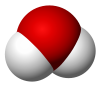

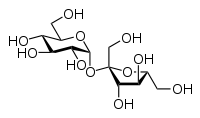
H2O NaCl C12H22O11
Medžiaga – materialus objektas, turintis rimties masę. Medžiagos susideda iš mažiausių dalelių: atomų ir molekulių. Medžiagos gali būti vieninės ir sudėtinės.
Vieninės medžiagos – tai iš vienos rūšies atomų sudarytos medžiagos. Jos gali būti:
- vienatomės: Ne, Ar, Hg, Na;
- dviatomės: O2, Cl2, Br2, N2;
- poliatomės: P4, S8.
Sudėtinės medžiagos – iš kelių skirtingų elementų atomų sudarytos medžiagos.
Pvz.:
vandenilio chloridas HCl, cukrus C12H22O11, polietenas (– CH2 = CH2 –)n.
S, H, Pb, Th ir kt.
Izotopai – to paties cheminio elemento atomai, turintys vienodą protonų skaičių, bet skirtingą masę (neutronų skaičių). (žr. 2.1.2. sk.)
Alotròpija – cheminio elemento gebėjimas egzistuoti dviejų ar kelių vieninių medžiagų (alotropinių atmainų pavidalu).
Alotropinė atmaina – to paties elemento skirtingos struktūros ir skirtingų savybių vieninės medžiagos.
Pvz.:
- deguonies alotropinės atmainos: deguonis O2 ir ozonas O3;
- fosforo alotropinės atmainos: baltasis, raudonasis, juodasis ir violetinis;
- anglies alotropinės atmainos: grafitas, deimantas, fulerenas ir kt.
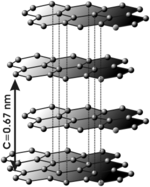
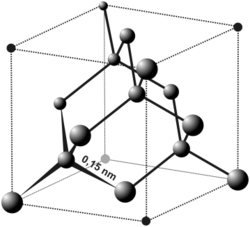
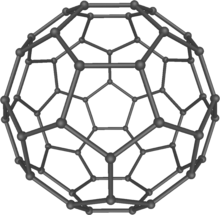
grafitas deimantas fulerenas
Cheminis ryšys (žr. 2.3 sk.) – atomų savitarpio sąveika, dėl kurios susidaro molekulė arba kristalas.
Cheminis ryšys gali būti joninis, kovalentinis, koordinacinis (donoro-akceptorinis), metališkasis ir vandenilinis.
Elektrinis neigiamumas – atomo branduolio savybė prisitraukti kito atomo, su kuriuo junginyje yra sudaręs ryšį (ryšius), elektronus.
Atominė masės vienetas (a.m.v.) – nesisteminis masės vienetas, naudojamas cheminių elementų atominei masei išreikšti. Atominės masės vienetas atitinka anglies izotopo 12C atomo masės 1/12 dalį. Jo dydis SI vienetais yra unitas (u). 1u = 1,66057·10–27 kg.
Elemento santykinė atominė masė (Ar) – vidutinės elementų atomų masės ir 1/12 anglies izotopo 12C atomo masės santykis. Vidutinė to paties elemento visų izotopų vidutinė santykinė atominė masė yra nurodoma periodinėje cheminių elementų lentelėje.
Pvz.:
Ar(Al) = 27
Ar(O) = 16
Ar(S) = 32
Santykinė molekulinė masė (Mr) – molekulę sudarančių atomų santykinių atominių masių suma, skaitine verte lygi vieno medžiagos molio masei.
Pvz.:
Mr(Na2SO4)
= 23 · 2 + 32 + 16 · 2 = 142
Mr(Na2SO4
·10H2O) = 142 + 10 · 18 = 322
Mr(C12H22O11)
= 12 · 12 +1 · 22 +16 · 11 = 342
Molis – medžiagos kiekio SI sistemos matavimo vienetas (n, mol), lygus medžiagos kiekiui, kuriame yra tiek struktūrinių vienetų (molekulių, jonų, atomų), kiek atomų yra 0,012 kg anglies 12C izotopo (6,02 · 1023).
Vieną molį bet kurios medžiagos sudaro 6,02 · 1023 struktūrinių vienetų. Šis skaičius vadinamas Avogadro konstanta (NA, mol–1).
Molinė masė – vieno medžiagos molio masė (M, g/mol). Molinės masės skaitinė vertė sutampa su santykinės atominės masės arba santykinės molinės masės skaitine verte.
M(Al) = 27 g/mol
M(O2) = 32 g/mol
M(Na2SO4) = 23 · 2 + 32 +16 · 2 = 142 g/mol
M(Na2SO4 ·10H2O) = 142 + 10 ·18 = 322 g/mol
M(C12H22O11) = 12 · 12 + 1 · 22 + 16 · 11 = 342 g/mol
Molinis tūris – medžiagos 1 molio užimamas tūris. Vienas molis bet kurių dujų normaliomis sąlygomis užima 22,4 litro tūrį. Jis žymimas Vm = 22,4 l/mol.
Normaliosios sąlygos (n.s.) – T = 273,15 K arba t = 0 ºC, p = 100 kPa (IUPAC) (angl. standard temperature and pressure – STP)
Valentingumas - cheminio elemento atomo sudaromų ryšių su kitais atomais, skaičius. Dažnai atomo valentingumas junginyje lygus periodinės elementų sistemos grupės, kurioje yra elementas, numeriui.
Vienų elementų valentingumas yra pastovus (pvz., Na, K, Al, Zn, Cd), kitų – kintamas (pvz., junginyje H2S siera yra dvivalentė, junginyje SO2 – keturvalentė, junginyje SO3 – šešiavalentis).
Oksidacijos laipsnis (OL) yra sąlyginis atomo krūvis junginyje, kurį jis turėtų, jeigu prisijungtų ar atiduotų valentinius elektronus.
Oksidacijos laipsnis gali būti teigiamas, neigiamas arba lygus nuliui.
Elementų OL rašomas virš cheminio elemento simbolio, nurodant krūvio ženklą ir vertę.
Pvz.: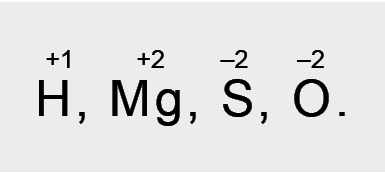
Cheminė formulė – vieninių ar sudėtinių medžiagų sandaros ir sudėties išraiška cheminiais ir kitais simboliais, skaitiniais indeksais.
Pvz.:
Vieninės medžiagos: helis – He; chloras – Cl2. Dešinėje apačioje indeksas 2 rodo, kad chloro molekulę sudaro du chloro atomai (dviatomė molekulė).
Sudėtinės medžiagos: vanduo – H2O. Ji rodo, kad vandens molekulę sudaro du vandenilio atomai ir vienas deguonies atomas; azoto(V) oksido – N2O5. Azoto(V) oksido molekulę sudaro du azoto atomai ir penki deguonies atomai; aliuminio sulfatas – Al2(SO4)3.
Cheminė formulė būna empirinė ir struktūrinė.
Empirinė formulė – formulė, rodanti junginio elementų paprasčiausią kiekybinį santykį molekulėje.
Pvz.:
Empirinė
formulė CH2O tinka ir etano rūgščiai CH3COOH, ir gliukozei
C6H12O6, ir metanaliui HCOH.
Struktūrinė formulė – molekulės atomų erdvinio išsidėstymo ir ryšių tarp jų pavaizdavimas plokštumoje.
Struktūrinėse formulėse vienu
brūkšniu (–) vaizduojami viengubieji ryšiai, dviem (=) – dvigubieji,
o trim (≡) – trigubieji ryšiai.
Pvz.:
H2O O2 N2
H – O – H O = O N ≡ N
Jonas – tai teigiamąjį arba neigiamąjį elektros krūvį turinčios dalelės, kuriomis virsta atomas ar atomų grupė, atidavusios arba prisijungusios elektronus.
Katijonas – atomas arba atomų grupė, turinti teigiamąjį krūvį (Na+, NH4+).
Anijonas – atomas arba atomų grupė, turinti neigiamąjį krūvį (Cl–, SO42–, CH3COO–).
Disociacija – molekulių ar sudėtinių jonų skilimas į kelias mažesnės molekulinės masės daleles (žr. 5.2.3 sk.).
Jonizacija – elektringųjų dalelių – jonų – susidarymas iš neutraliųjų atomų ir molekulių.
Cheminė reakcija – procesas, kai vienos medžiagos virsta kitomis, vienuose cheminiuose junginiuose nutrūkstant cheminiams ryšiams, persitvarkant juose atomams bei susidarant naujiems ryšiams.
Vykstant cheminėms reakcijoms susidaro naujos medžiagos su kitomis fizikinėmis ir cheminėmis savybėmis (žr. 4.1 sk.).
Cheminė lygtis – cheminės reakcijos raiška (aprašymas) cheminėmis formulėmis.
Termocheminė lygtis – cheminė lygtis, kurioje nurodytas šiluminis reakcijos efektas. (žr. 3.xx sk.).
Tankis – tai medžiagos vienetinio tūrio masė (ρ, g/cm3; kg/m3 ).
Pvz.:
Aliuminio ρ = 2,7 g/cm3 arba 2700 kg/m3
Mišinys – medžiaga, susidedanti mažiausiai iš dviejų sudedamųjų dalių. Mišiniai gali būti vienalyčiai ir nevienalyčiai.
Vienalytis mišinys – mišinys, sudarytas iš vienos būsenos medžiagų (tirpalai, lydiniai, dujų mišiniai).
Nevienalytis mišinys – mišinys, sudarytas iš skirtingų medžiagų, kurių daleles matome plika akimi (dūmai – kietos medžiagos dujose, aliejus vandenyje – dviejų skysčių mišinys).
Medžiagos masės dalis mišinyje (tirpale) yra lygi tos medžiagos ir mišinio (tirpalo) masių santykiui.
Mišinio sudėtis procentais rodo, kiek kiekvienos medžiagos masės dalių yra 100 masės dalių mišinio.
Tirpiklis – medžiaga, kurios kiekis tirpale yra didžiausias. Dažniausiai tirpiklis yra skystis.
Tirpinys – ištirpusi medžiaga tirpiklyje.
Tirpumas – dydis, nusakomas didžiausia tirpinio mase (arba tūriu dujinėms medžiagoms), kuri gali ištirpti 100 g tirpiklio tam tikroje temperatūroje, susidarant sočiajam tirpalui.
Sotusis tirpalas – tirpalas, kuriame yra didžiausia tirpinio masė esant tam tikrai temperatūrai.
Nesotusis tirpalas – tirpalas, kuriame dar gali ištirpti tirpinio, susidarant sočiajam tirpalui, esant tam tikrai temperatūrai.
Persotintasis tirpalas – tirpalas, kuriame tirpinio masė yra didesnė, nei tos pačios temperatūros sočiajame tirpale.
