Teorinė medžiaga su pavyzdžiais
| Wydrukowane przez użytkownika: | Gość |
| Data: | sobota, 30 maja 2026, 16:18 |
8.1. Teorija: grafikų braižymas ir lentelių sudarymas
1. Ašių pasirinkimas ir įvardijimas
Ant horizontaliosios (abscisių) ašies žymimos argumento vertės, ant vertikaliosios (ordinačių) ašies − funkcijos vertės. Pavyzdžiui, nubrėžkite grafiką, vaizduojantį monohidroksilių alkoholių virimo temperatūros priklausomybę nuo C atomų skaičiaus. Vadinasi, virimo temperatūros vertės bus žymimos ant vertikaliosios ašies, o C atomų skaičius − ant horizontaliosios ašies (1 pav.). Abi ašys turi būti įvardytos − nurodomas parametras ir matavimo vienetai.
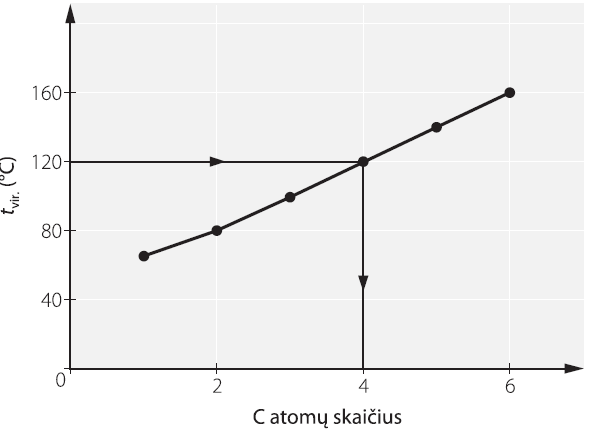
1 pav. Tinkamai panaudotas duotasis graduotas plotas
Jei pateikiamas klausimas: „Alkoholio virimo temperatūra 120 °C. Kiek C atomų yra alkoholyje?“, rodyklių kryptimi, pasitelkus liniuotę, nubrėžiamos linijos iki susikirtimo su abscisių ašimi. Atsakymas: alkoholį sudaro 4 C atomai.
2. Mastelio pasirinkimas
Ašių padalos žymimos ir mastelis pasirenkamas taip, kad būtų kuo geriau panaudotas duotasis plotas (1 pav.). Jei jis panaudotas ne visas (pavyzdžiui, pasirinktas toks mastelis, kad jį padvigubinus kreivė telpa į duotąjį plotą), vertinimas mažinamas 1 tašku.
Atsižvelgiant į konkrečius duomenis, koordinačių pradžia nebūtinai turi būti nulinė parametro vertė. Jei duomenų intervalas labai didelis, ašyse reikia daryti „trūkį“ − žymėti jį atitinkamu ženklu (dažniausiai ≈) (2 pav.).
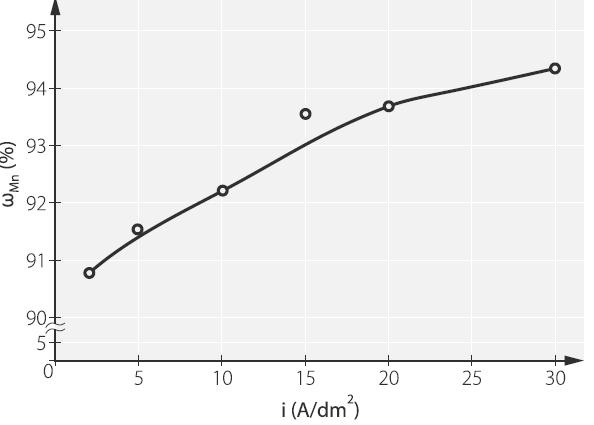
2 pav. Trūkio žymėjimas graduotame plote
Nepatartina rinktis mastelio, kai pateikto grafiko sudarymui ploto 1 cm lygus nelyginiams parametro vienetams (pavyzdžiui, 1 cm = 3 arba 6, arba 9 parametro dydžiams). Tada žymint grafiko taškus dažnai klystama.
3. Verčių žymėjimo tikslumas ir kreivės kokybė
Visos grafiko vertės, laikantis mastelio, žymimos tašku, trikampiu ar kitu panašiu nedideliu ženklu, kurio centras sutampa su konkrečia verte. Grafiko kreivė tolygiai brėžiama ranka, kad kuo mažiau būtų nutolusi nuo pažymėtos vertės. Atsižvelgiant į rezultatų tikslumą, ne visos vertės gali būti sujungiamos kreive (2 pav.). Jei kuri nors vertė akivaizdžiai skiriasi nuo bendros duomenų kitimo tendencijos, yra atmetama kaip eksperimento klaida. Brėžiant kreivę, į šią vertę neatsižvelgiama.
4. Lentelių sudarymas
Labai svarbu mokėti tyrimų rezultatus surašyti į pasirinktos struktūros lenteles, kuriose eilutes ir stulpelius galima sukeisti.
8.2. Pavyzdžiai: grafikų sudarymas/skaitymas ir lentelių sudarymas
1 pavyzdys
Lentelėje pateiktos VIA grupės cheminių elementų hidridų fizikinės charakteristikos, nustatytos esant STP:
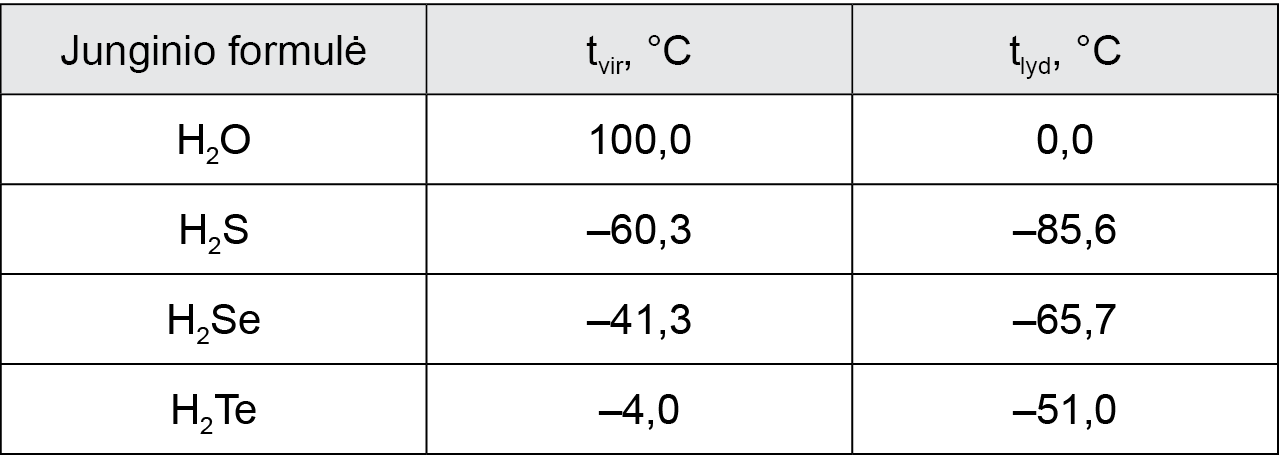
1. Naudodamiesi lentelėje pateikta informacija nubraižykite grafiką, vaizduojantį hidridų virimo temperatūros priklausomybę nuo nemetalo, esančio VIA grupės hidrido formulėje, atominio skaičiaus.
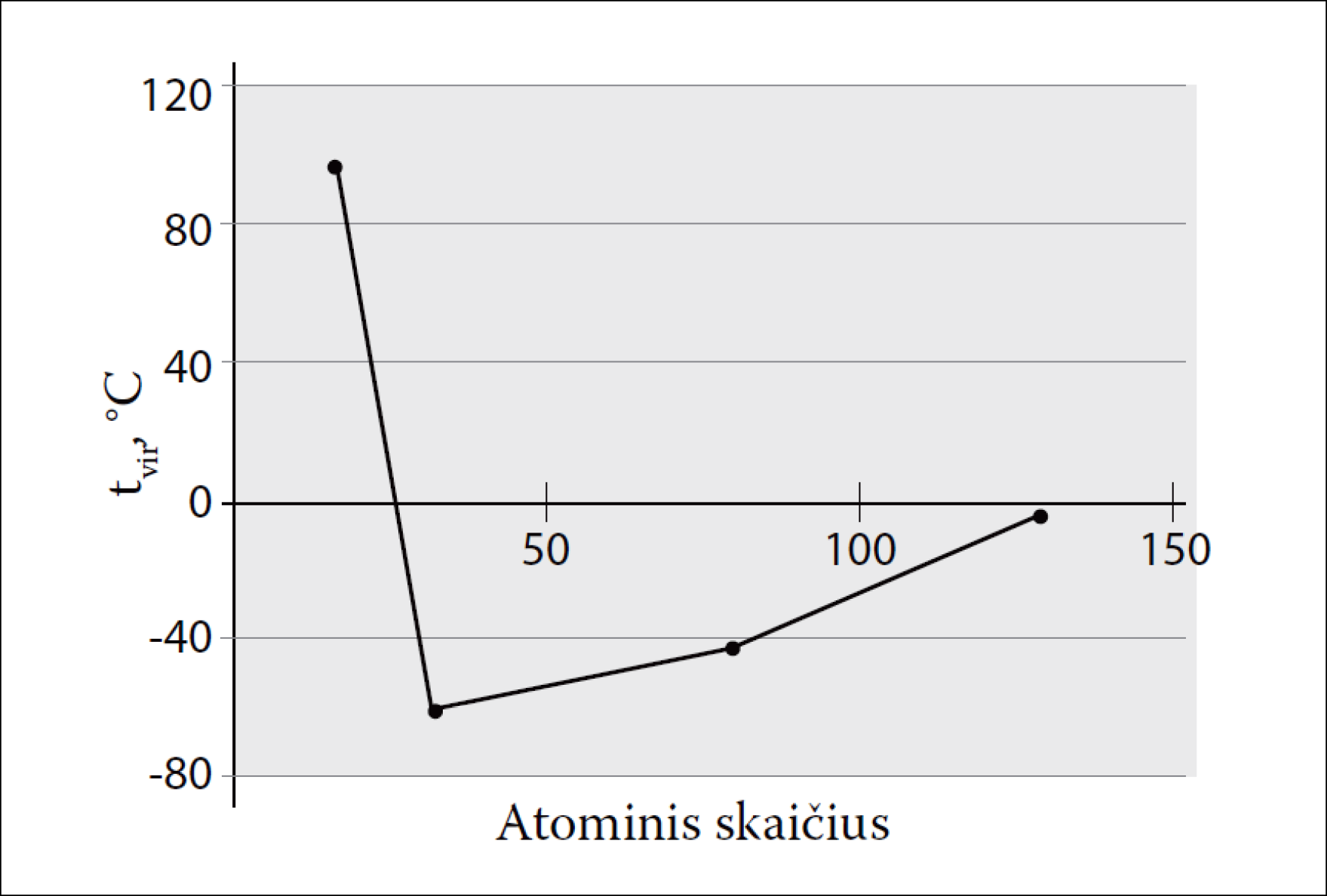
Nubrėžto grafiko vertinimas:
- Teisingai pasirinktos ir įvardytos ašys bei pažymėti matavimo vienetai
- Ašyse sužymėtos padalos pasirinkus tinkamą mastelį, kai grafikas užima daugiau negu pusę duotojo ploto
- Pažymėti taškai ir nubraižyta kreivė
Agregatinė būsena Junginio formulė
kieta H2O
Agregatinė būsena Junginio formulė
dujos H2S arba H2Se arba H2Te
2 pavyzdys
Grafikas vaizduoja, kaip paplitę kai kurie cheminiai elementai Visatoje.
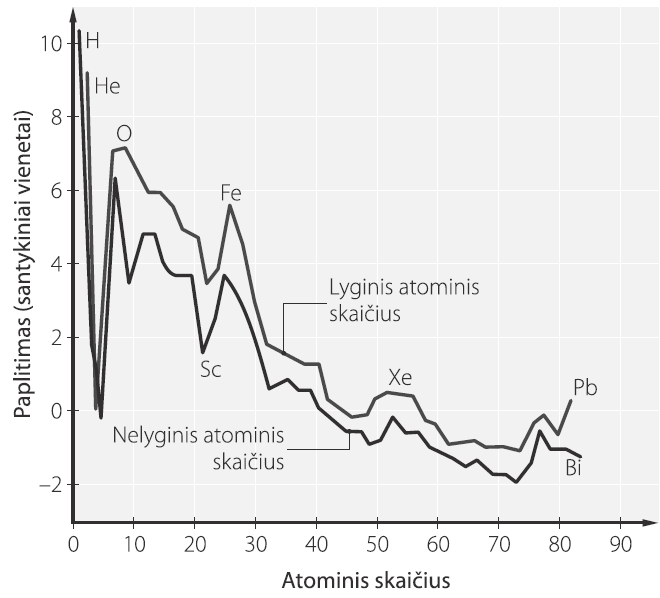
Pagal grafiką išsamiai apibūdinkite šių cheminių elementų paplitimo Visatoje priklausomybę nuo jų atominio skaičiaus.
Remiantis pateiktu grafiku galima daryti tokias išvadas:
- Didėjant atominiam skaičiui, cheminių elementų paplitimas netolygiai mažėja.
- Lyginio atominio skaičiaus cheminiai elementai daugiau paplitę negu nelyginio atominio skaičiaus.
- Netikslus būtų toks atsakymas: „Didėjant atominiam skaičiui, cheminių elementų paplitimas mažėja.“
Lentelių sudarymas
Mokinys tyrė tirpimo reakcijos
Zn(k) + 2HCl(aq) → ZnCl2(aq) + H2(d)
reakcijos greičio v (mol/(l×s)) priklausomybę nuo įvairių šių veiksnių: temperatūros, skiedimo vandeniu bei cinko gabalėlių smulkinimo.
Nubraižykite lentelę, kurioje, įvardinę eilutes ir stulpelius, galėtumėte surašyti ir apibendrinti visus bandymų rezultatus.
Tyrimo rezultatus galima pateikti tokioje lentelėje:

Lentelės sudarymo įvertinimas:
- Lentelės eilutės ir stulpeliai gali būti sukeisti
- Parašyti matavimo vienetai
8.3. Tyrimų duomenų tikslumas ir paklaidos. Apvalinimas
Tyrimo duomenų tikslumas ir paklaidos. Apvalinimas
Sprendžiant chemijos uždavinius vartojami dydžiai, nurodyti uždavinio sąlygoje arba pateikti įvairiose lentelėse. Šie dydžiai skirstomi į tiksliuosius ir apytikslius.
Tikslieji dydžiai:
- objektų kiekiai (11 Al gabalėlių, 4 trikampės prizmės sienos ir t. t.);
- koeficientai ir laipsnio rodikliai;
- indeksai ar sutartiniai dydžiai (metano formulėje CH4 4 yra tikslus vandenilio atomų skaičius).
Taigi tikslieji dydžiai nėra matavimų rezultatai, todėl jie rašomi be jokių paklaidų.
Apytiksliai dydžiai – kokių nors matavimų ar jų pagrindu atliktų skaičiavimų rezultatai. Pavyzdžiui, tirpalo temperatūros nustatymas (1 pav.).

1 pav. Tirpalo temperatūros nustatymas spiritiniu termometru
Išmatuotos ir tikrosios fizikinio dydžio vertės skirtumas yra vadinamas matavimų paklaida. Kadangi per bandymą matuojama kelis kartus, tai apskaičiuojama vidutinė matuojamo dydžio vertė. Pavyzdžiui, atlikti keturi neutralizavimo reakcijos matavimai: titravimui suvartota 10,5 ml, 11,2 ml, 10,9 ir 10,6 ml tirpalo. Taigi vidutinė dydžio vertė:
(10,7 + 11,2 + 10,9 + 10,6) : 4 = 10,85 ml
Matavimų rezultatas pateikiamas dviem reikšminiais skaitmenimis, todėl vidutinė dydžio vertė yra 10,9 ml.
Įprasta, kad paskutinis skaičius rašomas su mažiausiai vieno skaitmens paklaida.
Reikšminių skaitmenų kiekis leidžia įvertinti matavimų ar skaičiavimų tikslumą.
- Visos „nenulinės“ vertės yra reikšminiai skaitmenys. Pavyzdžiui, skaičius 5248 turi keturis, o 6,12 − tris reikšminius skaitmenis.
- Nuliai, rašomi tarp skaičių 1...9, yra reikšminiai. Pavyzdžiui, skaičius 6,0095 turi penkis, o 8,18 − tris reikšminius skaitmenis.
- Į kairę nuo skaičių 1...9 rašomi nuliai nėra reikšminiai. Pavyzdžiui, du reikšminius skaitmenis turi skaičius 0,45 ir 0,000045.
Skaičiuojant apytiksliais skaičiais, galutinis rezultatas irgi yra apytikslis skaičius.
Kad skaičiavimų rezultatai parodytų gautų dydžių tikslumą, reikia laikytis tam tikrų taisyklių:
1. Pirmiausia nustatoma, kurie skaičiai yra tikslūs, o kurie – apytiksliai.
2. Daugybos ir dalybos veiksmų atsakyme rašoma tiek reikšminių skaitmenų, kiek jų yra skaičiuje, kuris tokių skaitmenų turi mažiausiai. Pavyzdžiui, reikia apskaičiuoti 11-os cukraus gabalėlių, kurių vieno masė 0,35 g, bendrąją masę. Čia 11 yra tikslus, o 0,15 – apytikslis skaičius, turintis du reikšminius skaitmenis. Todėl 0,35 g × 11 = 3,85 g ≈ ~3,9 g.
Atsakyme irgi turi būti du reikšminiai skaitmenys. Tarpinis atsakymas apvalinamas.
mb = 0,650 g + 0,655 g + 0,54 g = 1,845 g ≈ ~1,85 g.
Mažiausias skaičius 0,52, todėl bendroji masė apvalinama iki dviejų skaitmenų po kablelio tikslumu.
4. Tarpinius rezultatus atitinkantis skaičius visada turi vienu reikšminiu skaitmeniu daugiau negu netiksliausias skaičius. Galutiniame atsakyme šis skaičius turi būti apvalinamas.
Sprendžiant chemijos uždavinius dažniausiai vartojami apytiksliai skaičiai: molinis tūris 22,4 l/mol; Avogadro konstanta 6,02 × 1023 mol−1; santykinės atominės ir molekulinės masės (paprastai apvalinamos iki 3 reikšminių skaitmenų), todėl atlikus matematinius veiksmus atsakyme irgi turėtų būti tik 3 reikšminiai skaitmenys.
Skaičių apvalinimo (≈) iki 3 reikšminių skaitmenų pavyzdys:
5,250 ≈ ~5,25
5,251 ≈ ~5,25
5,252 ≈ ~5,25
5,253 ≈ ~5,25
5,254 ≈ ~5,25
5,255 ≈ ~5,26
5,256 ≈ ~5,26
5,257 ≈ ~5,26
5,258 ≈ ~5,26
5,259 ≈ ~5,26
Dažnai skaičiuojant kiekio vienetais atliekama daug matematinių veiksmų ir daug kartų apvalinama.
Pavyzdys
Didelio oktaninio skaičiaus benzinas pramonėje gaminamas krekingo proceso metu, kuomet vyksta panašaus pobūdžio reakcija:
C20H42 ![]() C6H14 + C14H28
C6H14 + C14H28
nafta
Krekingo metu alkenai sudaro 75 % visų produktų kiekio. Iš jų 90 % tenka alkenams su dvigubuoju ryšiu grandinės gale, kurie naudojami paviršiaus aktyvių medžiagų sintezei. Apskaičiuokite, kiek tokių alkenų galima gauti iš 1 tonos naftos, jei reakcijos išeiga 85 %. Atsakymą užrašykite standartine išraiška.
Sprendimas
Apskaičiuojame iš naftos gaunamo alkeno masę:
282 g/mol C20H42 – 196 g/mol C14H28
1 t C20H42 – x t C14H28
x = 0,695 t
Įvertiname alkenų masės dalį naftoje:
m(C14H28) = 0,695 t × 0,75 × 0,9 = 0,4691 t
Apskaičiuojame alkenų masę įvertinant reakcijos išeigą:
m = 0,4691 t × 0,85 = 0,3987 t
Užrašome atsakymą standartine išraiška:
m = 3,987 × 10-1 t arba m = 3,987 × 102 kg
8.4. Cheminiai indai
Paprasčiausias indas bandymams nedideliais tūriais atlikti yra mėgintuvėlis, t.y. vamzdelis užlydytu galu:

Cheminė stiklinė − laboratorinis indas skysčiams laikyti, šildyti ir reakcijoms atlikti:

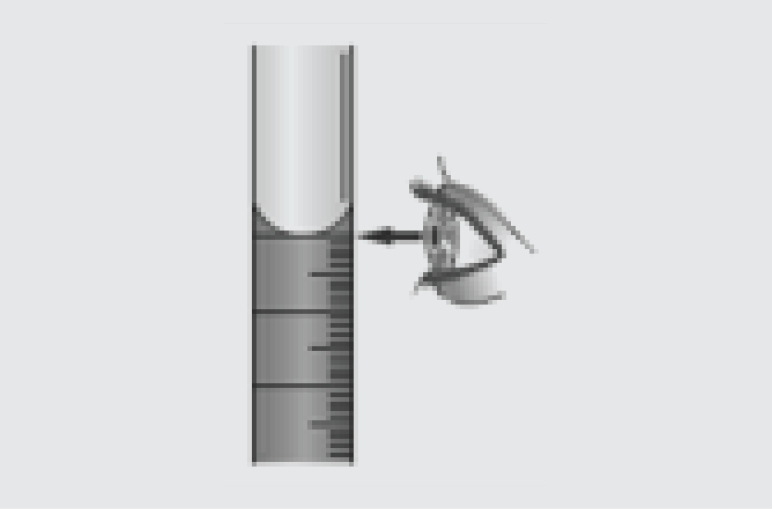
Matavimo cilindras − cilindras su padalomis skysčių tūriui matuoti:

Skysčių stulpelio aukštis nustatomas pagal meniską. Meniskas − iškilas (nustatant Hg aukštį) arba įgaubtas skysčio paviršius siaurame vamzdelyje:
Pipetė − indas arba vamzdelio pavidalo įtaisas skysčiams įsiurbti, lašinti, matuoti:

Įsiurbti skystį pipete galima burna, kriauše ar specialiu įtaisu:

Iš pipetės skystis ne pučiamas, o laukiama, kol ištekės.
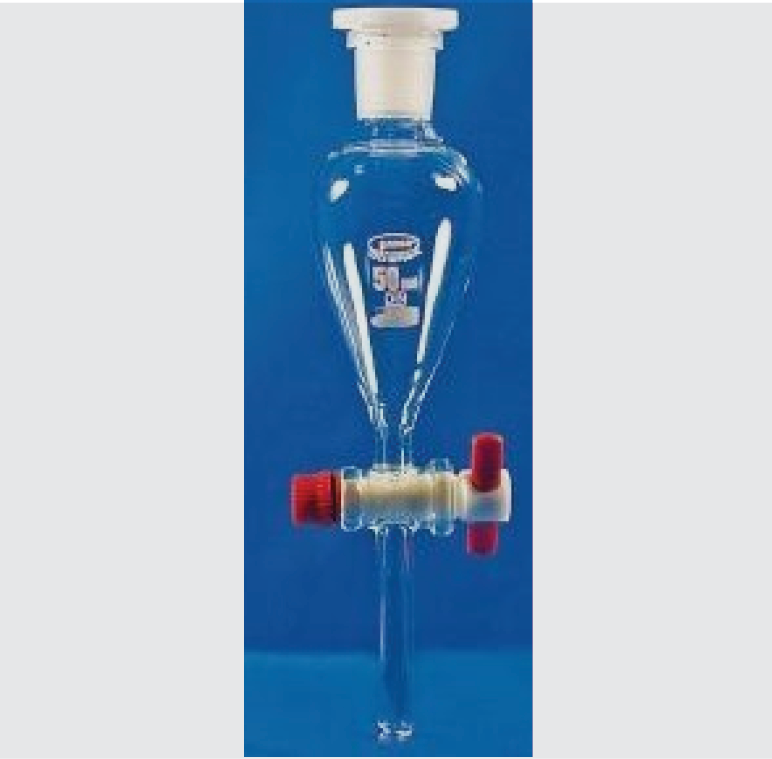
Dalijamasis piltuvas − indas nesimaišantiems skysčiams perskirti:
Norint garinimu iš tirpalo išskirti kietąjį tirpinį, naudojama garinimo lėkštelė:

Spiritinė lemputė − laboratorinis šildymo įtaisas, kuriame deginamas etanolis:

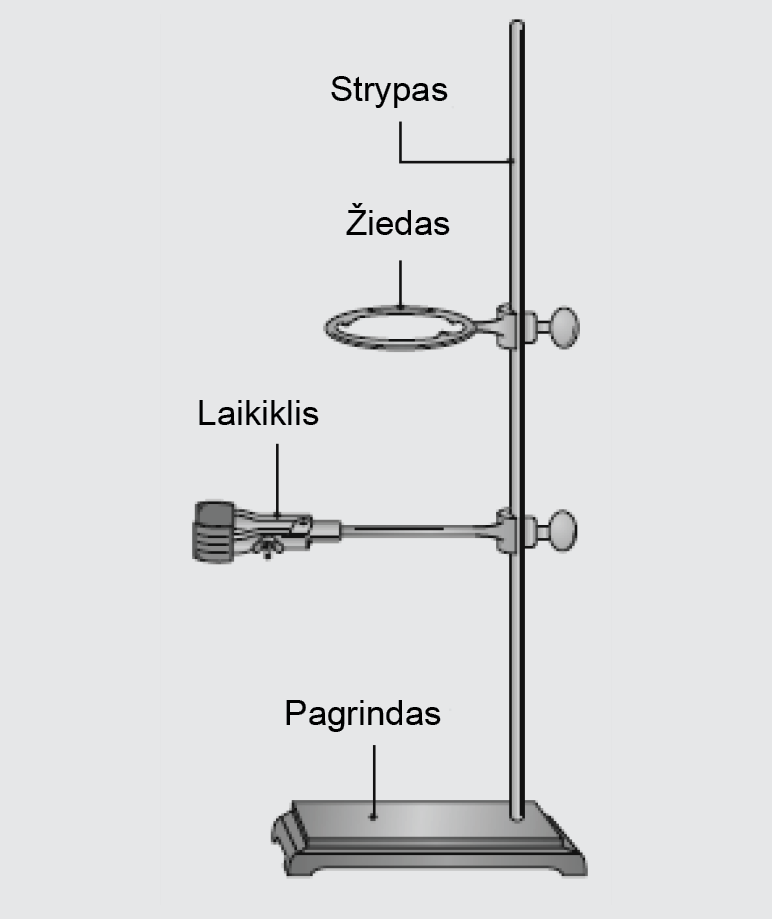
Laboratorinis stovas − metalinis stiebas ant trikojės arba keturkampės plokštės, naudojamas indams ar laboratorijos prietaisams įtvirtinti:
Atliekant įvairius bandymus, pavyzdžiui, titravimą, naudojama kūginė (Erlenmejerio) kolba:

Plokščiadugnė kolba − apvali kolba plokščiu dugnu:

Ji naudojama ruošiant tirpalus.
Norint kolboje esantį tirpalą kaitinti, naudojama apvaliadugnė kolba:

Viurco kolba − apvaliadugnė kolba su kaklo atšaka:

Joje distiliuojami skysčiai.
Matavimo kolba − plokščiadugnė, ilgakaklė kolba su žyme tūriui matuoti:

Joje ruošiami molinės koncentracijos tirpalai.
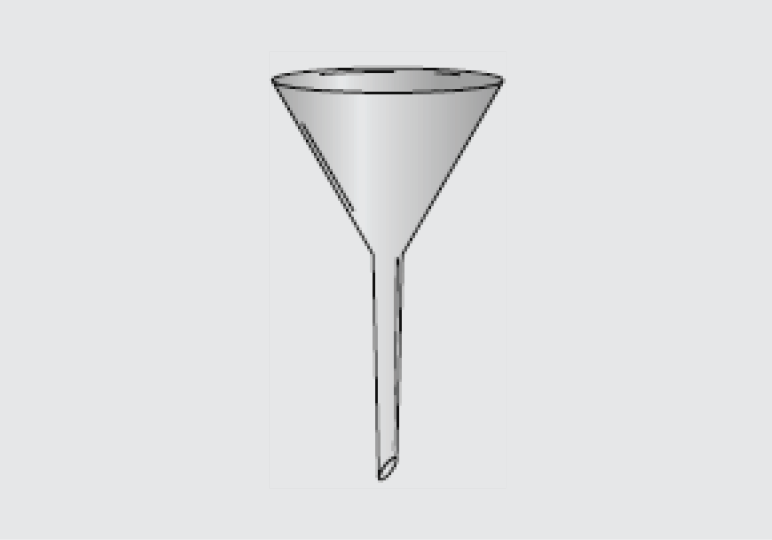
Piltuvas − kūgio pavidalo indas su kakleliu skysčiams pilti, filtruoti pro filtravimo popierių:
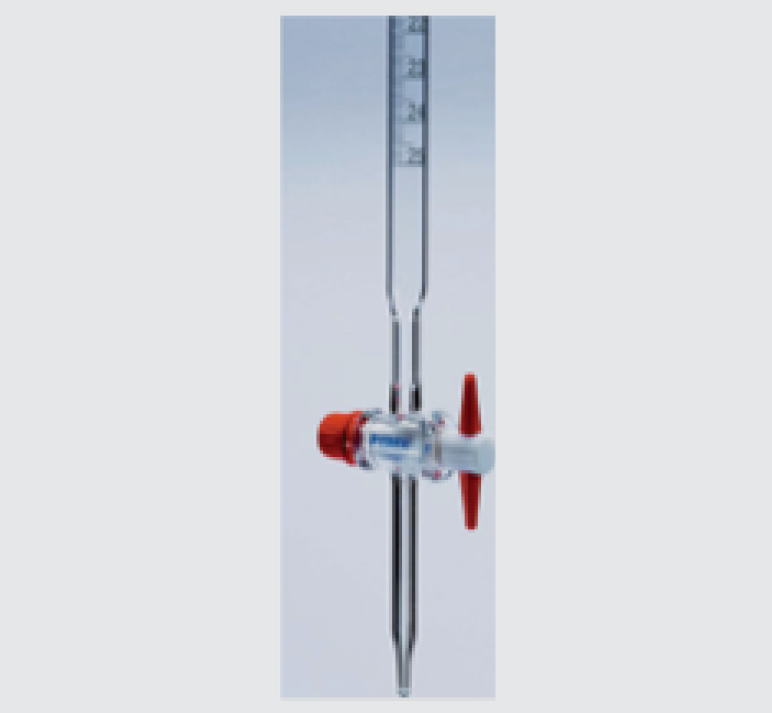
Biuretė − stiklinis vamzdelis su padalomis skysčių ar dujų tūriui matuoti, skysčiui lašinti.
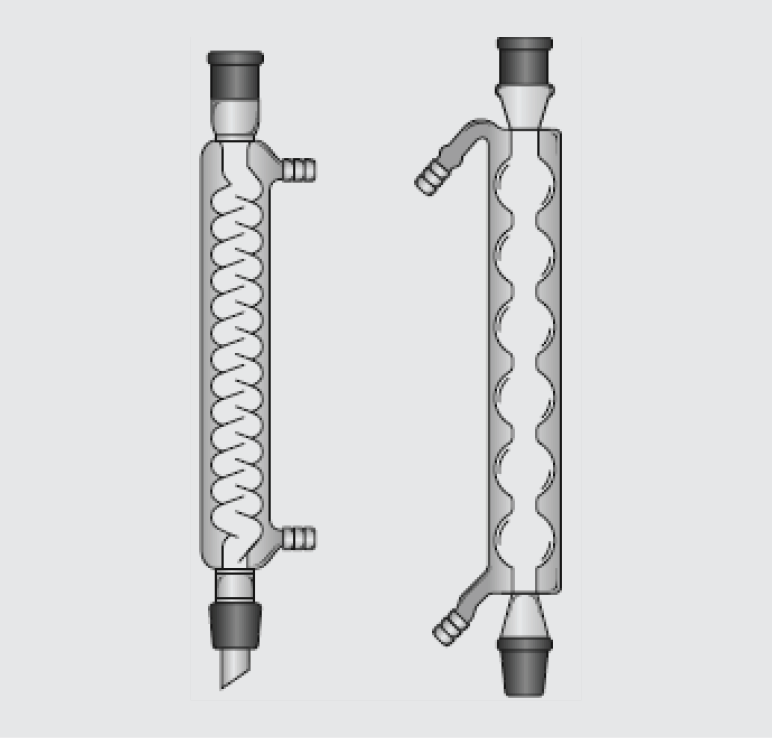
Kondensatoriuje (šaldytuve) aušinami ir kondensuojami garai.
Stikliniai laboratoriniai kondensatoriai naudojami dujoms ir garams kondensuoti ir aušinti:
8.5. Saugus darbas laboratorijoje
Dirbant chemijos laboratorijoje būtina laikytis tam tikrų reikalavimų:
- apsipylus cheminėmis medžiagomis ar sudaužius indus to negalima slėpti. Apsipylus cheminėmis medžiagomis, nedelsiant jas nuplaukite vandeniu ir apie tai pasakykite laborantui ar dėstytojui;
- laboratorijoje negalima valgyti ir gerti. Neragaukite jokių cheminių medžiagų;
- siekiant apsaugoti akis, naudokite apsauginius akinius. Medžiagoms patekus į akis, plaukite jas vandeniu ir pasakykite laborantui ar dėstytojui. Esant galimybei, naudokite chalatus;

- neuostykite jokių cheminių medžiagų, nekiškite nosies tiesiai prie indo angos, nes galite įkvėpti pavojingų ir nuodingų medžiagų. Kvapui pajusti pakanka labai nedidelio kiekio medžiagos. Norint nustatyti medžiagos kvapą, indą laikykite priešais save ir mosuokite ranka virš indo su medžiaga link savęs:
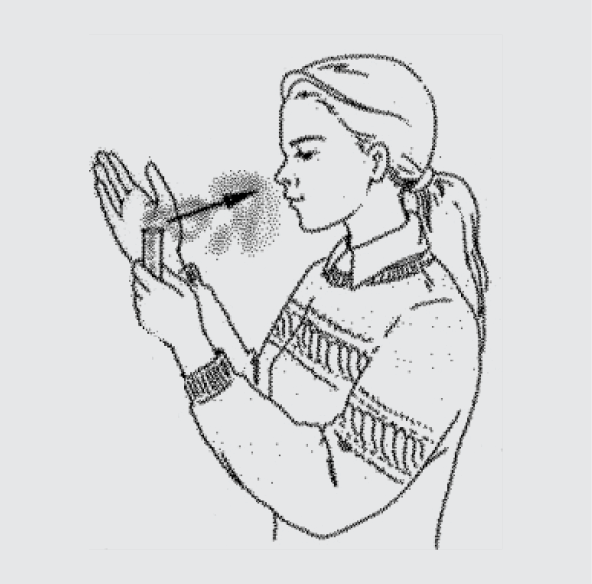
Norint išmokti uostyti, namuose pabandykite uostyti actą ar kvepalus;
- nelieskite cheminių medžiagų rankomis, jei tai nenurodyta eksperimento aprašyme, nes kai kurios medžiagos gali pažeisti odą ir įsiskverbti per ją į žmogaus organizmą. Esant galimybei, naudokite apsaugines pirštines;

- nemaišykite chemines medžiagas viena su kita, jei tai nėra nurodyta eksperimento aprašyme, nes sumaišius jas gali įvykti sprogimas ar išsiskirti nuodingos medžiagos;
- atliekant eksperimentus laikykitės tvarkos. Indai su cheminėmis medžiagomis ir prietaisai turi būti laikomi tvarkingai. Nedėkite juos arti laboratorinio stalo krašto, nes netyčia galite užkliudyti ranka ir numesti;
- eksperimentai su koncentruotomis rūgštimis ar šarmais, bei bandymų metu išsiskiriant nuodingoms dujoms, atliekami traukos spintose:

- taupykite chemines medžiagas ir bandymus atlikite su nedideliais jų kiekiais. Vieną medžiagą paėmus cheminiu šaukšteliu, jo nenuplovę ar nenuvalę kitai medžiagai paimti nenaudokite, nes užteršite kitą reagentą. Medžiagų ar skysčių likučių negalima pilti atgal į indą, nes į jį gali patekti priemaišų ir užteršite inde esančią medžiagą;
- likučiai supilami į indus atliekoms, kurie dažniausiai laikomi traukos spintose;
- baigus eksperimentus, sutvarkykite darbo vietą ir nusiplaukite rankas.
8.6. Cheminių medžiagų pavojingumo ženklai
Cheminės medžiagos yra klasifikuojamos pagal tris kategorijas:
- Pavojingumą sveikatai: 1) labai toksiška; 2) toksiška; 3) kenksminga; 4) ardanti; 5) dirginanti; 6) jautrinanti; 7) kancerogeninė; 8) mutageninė; 9) toksiška reprodukcijai;
- dėl jų fizikinių cheminių savybių: 1) sprogstamoji; 2) oksiduojanti; 3) ypač degi; 4) labai degi; 5) degi;
- pavojingumą aplinkai: 1) aplinkai pavojinga; 2) nepavojinga.
Kiekviena pavojingumo kategorija ženklinama simbolio raide, pavojingumo simboliu ir pavojingumo
nuoroda. Visos naudojamos cheminės medžiagos turi turėti įspėjamąją etiketę ir saugos lapą.
Bendrajam išsilavinimui būtina žinoti šias piktogramas:

Parengtos etiketės, esančios ant cheminio reagento indo, pavyzdys:
