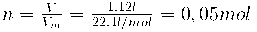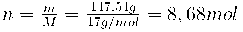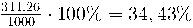Uždaviniai ir jų sprendimas
1. Kai nebūtina reakcijos lygtis
1.1. Kai reikia įvertinti dujų tirpumą
Kai kurių dujų tirpumo vandenyje priklausomybės nuo temperatūros (kai p=101,325 kPa)
Dažniausiai įvairių dujų tirpumo vandenyje priklausomybės nuo temperatūros yra atvaizduojamos grafiškai. Tačiau tikslias dujų tirpumo vertes galima rasti žinynų lentelės.Atkreipkite dėmesį: didėjant temperatūrai daugumos dujų tirpumas vandenyje mažėja!!! Ypač menkai tirpių dujų tirpumas vandenyje beveik nekinta didėjant temperatūrai.
Pagrindinių orą sudarančių dujų (N2, O2) tirpumas vandenyje yra gan mažas. Vandenilio bei visų inertinių dujų tirpumas vandenyje yra ypač mažas.
CO2 ir H2S tirpumas yra gerokai didesnis nei pagrindinių orą sudarančių dujų.
Tačiau tokių dujų, kurios ištirpę vandenyje gana gerai jonizuojasi (NH3, SO2, HCl), tirpumas vandenyje yra ypač didelis.
1 pav. Azoto (N2), deguonies (O2) ir vandenilio (H2) dujų tirpumo vandenyje priklausomybė nuo temperatūros (kai p=101,325 kPa)
2 pav. CO2 ir H2S dujų tirpumo vandenyje priklausomybė nuo temperatūros (kai p=101,325 kPa)
3 pav. NH3, SO2 ir HCl dujų tirpumo vandenyje priklausomybė nuo temperatūros (kai p = 101,325 kPa)
Uždavinys Nr.1
Kiek litrų reikia paimti 50 ºC temperatūros vandens, norint ištirpinti 1,12 l deguonies dujų?
Uždavinio sprendimas:
1. Iš 1 pav. pavaizduotų tirpumo kreivių surandame deguonies dujų tirpumą 50 ºC temperatūros vandenyje.
50 ºC temperatūros vandenyje gali ištirpti 3 mg deguonies dujų 100 g vandens.
2. Apskaičiuojame, kiek molių sudaro 1,12 l deguonies dujų:
3. Apskaičiuojame deguonies dujų masę:
m = n · M = 0,05 mol · 32 g/mol = 1,6 g
4. Apskaičiuojame, kiek litrų reikia paimti vandens, norint ištirpinti 1,6 g deguonies dujų:
3 mg – 100 g (vandens)
1600 mg – x g (vandens)
x = 53333 g = 53,333 kg
V = m / ρ = 53333 / 1 g/ml = 53333 ml = 53,333 l
Atsakymas: reikia 53,333 litrų vandens.
Uždavinys Nr.2
Apskaičiuokite, koks tūris amoniako dujų išsiskirs šildant 1 kg sotųjį amoniako tirpalą nuo 20 ºC iki 40 ºC temperatūros. Kokia bus amoniako masės dalis 20 ºC ir 40 ºC temperatūros tirpaluose?Uždavinio sprendimas:
1. Iš 3 pav. pavaizduotų tirpumo kreivių surandame amoniako dujų tirpumą 20 ºC ir 40 ºC temperatūros vandenyje.
20 ºC temperatūros vandenyje gali ištirpti 52,5 g amoniako dujų 100 g vandens.
40 ºC temperatūros vandenyje gali ištirpti 30 g amoniako dujų 100 g vandens.2. Apskaičiuojame, kiek gramų amoniako ir vandens (tirpiklio) yra 20 ºC temperatūros 1 kg sotaus tirpalo:
m(tirpalo) = 100 g (vandens) + 52,5 g (NH3) = 152,5 g
152,5 g (tirpalo) – 52,5 g (NH3)
1000 g (tirpalo) – x g (NH3)
x = 344,26 g (NH3)
m (H2O) = 1000 g – 344,26 g = 655,74 g
3. Apskaičiuojame kiek gramų amoniako gali ištirpti 40 ºC temperatūros vandenyje (655,4 g):
100 g (vandens) – 30 g (NH3)
655,4 g (vandens) - x g (NH3)
x = 196,72 g
4. Apskaičiuojame koks tūris amoniako dujų išsiskirs šildant tirpalą nuo 20 ºC iki 40 ºC:
m(NH3)išsiskirs = 344,26 g – 196,72 g = 147,54 g
Norint masę paversti į tūrį, reikia susirasti molius:
V = n · Vm = 8,68 mol · 22,4 l/mol = 194,4 l100 g (tirpalo) – x g (NH3)
x = 34,43 %
6. Apskaičiuojame 40 ºC temperatūros amoniako masės dalį tirpale:
m(tirpalo) = 655,74 g + 196,72 g = 852,46 g
852,46 g (tirpalo) – 196,72 g (NH3)
100 g (tirpalo) – x g (NH3)
x = 23,08 %