Teorinė medžiaga
5.1. Neorganinių junginių tipai
5.1.3. Rūgštys
Rūgštys – tai junginiai, kuriems skylant (jonizuojantis) vandenyje susidaro teigiamieji vandenilio jonai (protonai) H+. Rūgštys yra skirstomos į:
1) deguonines (H2SO4, HNO3, H2CO3, CH3COOH ir kt.);
2) nedeguones (H2S, HCl, HI, HBr ir kt.).
Pagal vandenilio atominį skaičių rūgštys skirstomos į:
1) vienprotones (HCl, HNO3 ir kt.);
2) poliprotones (H2S, H2SO4, H3PO4).
Bendroji deguoninių rūgščių formulė A(OH)mOn. Jei n = 0, tai tokia deguoninė rūgštis laikoma silpnąja (H3BO3, HClO); jei n = 1, tai deguoninė rūgštis yra silpnoji (H2CO3) arba vidutinio stiprumo (H3PO4); jei n = 2, tai rūgštis yra stiprioji (H2SO4, HNO3) (1 pav.).
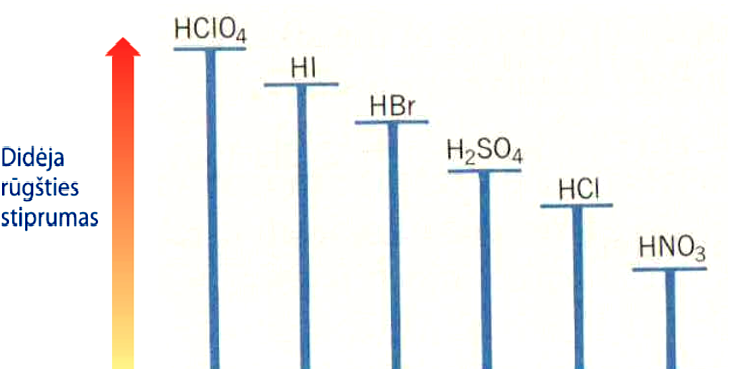
1 pav. Stipriųjų rūgščių stiprumo tarpusavio sąsaja
Kai kurių rūgščių pavadinimai
|
Formulė |
Nesisteminis pavadinimas |
Sisteminis (IUPAC) pavadinimas |
|
HCl |
Druskos rūgštis |
Vandenilio chloridas (1−) |
|
H2CO3 |
Anglies rūgštis, karbonato rūgštis |
Divandenilio trioksokarbonatas (2−) |
|
HNO3 |
Azoto rūgštis, nitrato rūgštis |
Vandenilio trioksonitratas (1−) |
|
H3PO4 |
Fosforo rūgštis, ortofosfato rūgštis |
Trivandenilio tetraoksofosfatas (3−) |
|
H2SO4 |
Sieros rūgštis, sulfato rūgštis |
Divandenilio tetraoksosulfatas (2−) |
|
H2SO3 |
Sulfito rūgštis |
Divandenilio trioksosulfatas (2−) |
|
HClO4 |
Perchlorato rūgštis |
Vandenilio tetraoksochloratas (1−) |
|
HClO |
Hipochlorito rūgštis |
Vandenilio monooksochloratas (1-) |
Chemijos laboratorijose dažnai naudojamos organinės rūgštys: metano arba skruzdžių HCOOH ir etano arba acto CH3COOH (daugiau žr. temos „Organiniai junginiai“ skyriuje „Karboksirūgštys“).
Pagrindiniai rūgščių gavimo būdai
1. Vykstant tiesioginei elementų sintezei:
Cl2(d) + H2(d) → 2HCl(d) (tirpinant vandenyje HCl(aq);
S(k) + H2(d) → H2S(d) (tirpinant vandenyje H2S(aq).
2. Tirpinant vandenyje rūgštinius oksidus (anhidridus):
SO2(d) + H2O(s) → H2SO3(aq);
N2O5 (d)+ H2O(s) → 2HNO3(aq).
3. Druskoms reaguojant su stipriosiomis rūgštimis:
NaCl(k) + H2SO4(s) → HCl(aq) + NaHSO4(aq);
NaNO3(k) + H2SO4(s) ![]() HNO3(aq) + NaHSO4(aq).
HNO3(aq) + NaHSO4(aq).
Pagal agregatinę būseną rūgštys yra skysčiai (H2SO4, HClO4) ir kietosios medžiagos (H3PO4, H2SiO3). Kai kurių rūgščių gali būti tik tirpaluose, pavyzdžiui, H2CO3, H2SO3.
Rūgštys reaguoja:
1) su bazėmis (vykstant neutralizacijos reakcijoms; (daugiau apie neutralizavimą žr. 5.2.8 skyrelį):
|
Stiprioji rūgštis ir stiprioji bazė | |
|
Visiška neutralizacija |
2NaOH(aq) + H2SO4(aq) → Na2SO4(aq) + 2H2O(s) OH−(aq) + H+(aq) → H2O(s) |
|
Nevisiška neutralizacija |
KOH(aq) + H2SO4(aq) → KHSO4(aq) + H2O(s) OH−(aq) + 2H+(aq) + SO42−(aq) → HSO4−(aq) + H2O(s) |
|
Silpnoji rūgštis ir stiprioji bazė | |
|
Visiška neutralizacija |
KOH(aq) + CH3COOH(aq) → KCH3COO(aq) + H2O(s) OH−(aq) + CH3COOH(aq) → CH3COO− (aq) + H2O(s) |
2) su baziniais oksidais:
Fe2O3(k) + 6HNO3(aq) → 2Fe(NO3)3(aq) + 3H2O(s);
Fe2O3(k) + 6H+(aq) → 2Fe3+(aq) + 3H2O(s);
3) su druskomis, jei susidaro mažai tirpus, lakus ar silpnai disocijuojantis junginys:
H2SO4(aq) + BaCl2(aq) → BaSO4(k) + 2HCl(aq);
SO42- (aq) + Ba2+(aq) → BaSO4(k);
2HCl(aq) + Na2CO3(aq) → 2NaCl(aq) + H2O(s) + CO2(d);
2H+(aq) + CO32- (aq) → H2O(s) + CO2(d);
4) kaitinamos deguonies turinčios rūgštys skyla:
H2SiO3(k) ![]() SiO2(k) + H2O(s);
SiO2(k) + H2O(s);
H2SO4(s) ![]() SO3(d) + H2O(s);
SO3(d) + H2O(s);
5) su metalais:
Zn(k) + 2HCl(aq) → ZnCl2(aq) + H2(d);
3Cu(k) + 8HNO3(aq) ![]() 3Cu(NO3)2(aq) + 2NO(d) + 4H2O(s).
3Cu(NO3)2(aq) + 2NO(d) + 4H2O(s).
Rūgštyse kinta indikatorių spalvos (žr. 5.2.8 skyrelį).