Teorinė medžiaga
5.2. Tirpalai
5.2.6. Elektrolitų pH
Vanduo yra silpnasis elektrolitas ir šiek tiek jonizuojasi į H+ ir OH- jonus:
![]()
Parašome šios grįžtamosios reakcijos (jonizacijos) pusiausvyros konstantos formulę:
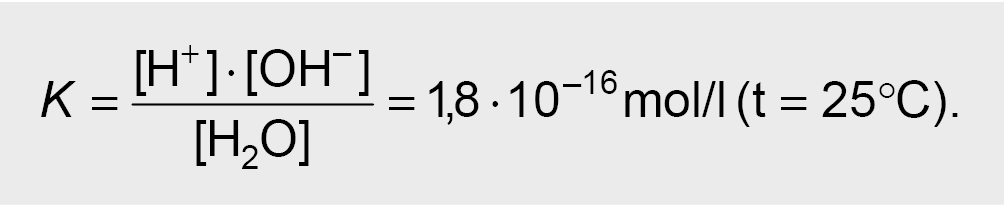
Pertvarkę formulę gauname:
[H+] · [OH–] = K · [H2O].
Kadangi vandens jonizacijos laipsnis labai mažas, tai nedisocijavusių vandens molekulių koncentraciją galima laikyti pastoviu dydžiu:

čia 1000 g yra 1 litro vandens masė.
Pažymėję [H+] ・ [OH-] = KH2O, gauname:
KH2O = K ・ [H2O] = 1,8 ・ 10-16 mol/l・55,55 mol/l = 10-16 mol2/l2
Kai temperatūra pastovi (t = 25 °C), vandens ir praskiestų vandeninių tirpalų vandenilio ir hidroksido jonų koncentracijų sandauga yra pastovus dydis, vadinamas vandens jonų koncentracijų sandauga ir lygus 10-14 mol2/l2 .
Tirpalai, kurių:
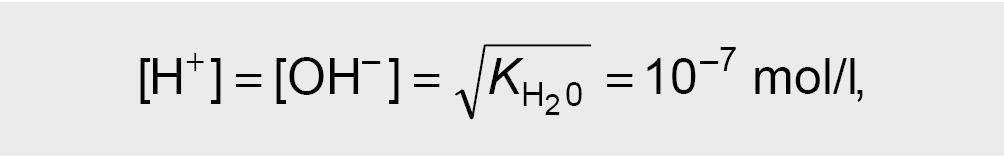
vadinami neutraliaisiais tirpalais.
Žinant vandenilio jonų koncentraciją, apskaičiuojama hidroksido jonų koncentracija, ir atvirkščiai:
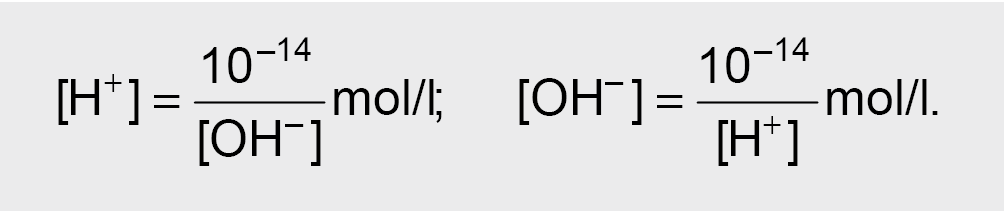
Pavyzdžiui, jei [H+] = 10–3 mol/l, tai
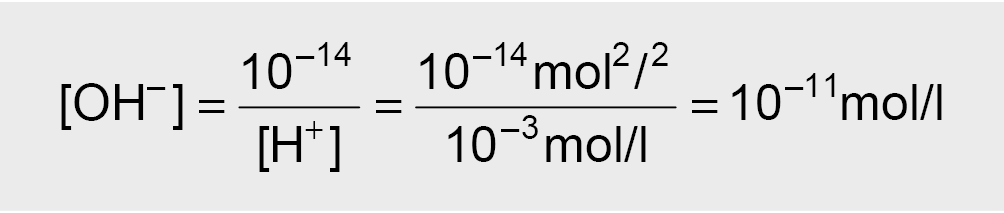 (tirpalas rūgštus);
(tirpalas rūgštus);
jei [H+] = 10–6 mol/l, tai
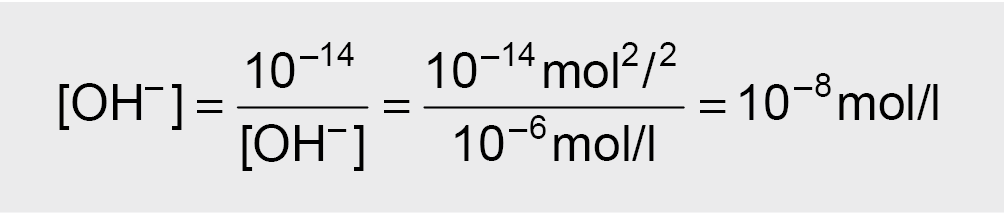 (tirpalas šarminis).
(tirpalas šarminis).
Vandenilio jonų koncentracijos vertė labai maža, todėl, kad būtų patogiau skaičiuoti, vandenilio jonų koncentracija reiškiama vandenilio jonų rodikliu, kuris žymimas pH.
pH yra lygus vandenilio jonų koncentracijos neigiamo ženklo dešimtainiam logaritmui:
pH = –lg[H+].
Kadangi [H+] · [OH-] = 10-14 mol2/l2, tai logaritmuodami gauname:
−lg[H+] · [OH-]) = −lg(10-14 ) Þ −lg[H+] + (−lg[OH-])= −lg10-14 .
pH + pOH = 14
Rūgščiojo tirpalo pH < 7, neutraliojo – pH = 7, šarminio – pH > 7.
Vandenilio jonų koncentracijos ir pH kitimas ir ryšys parodytas 6 ir 7 pav.
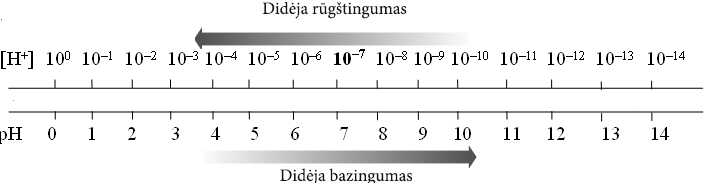
6 pav. Vandenilio jonų koncentracijos ir pH kitimas

7 pav. Vandenilio jonų koncentracijos ir pH ryšys
Tirpalų ir kai kurių maisto produktų pH vertės parodytos 8 pav.
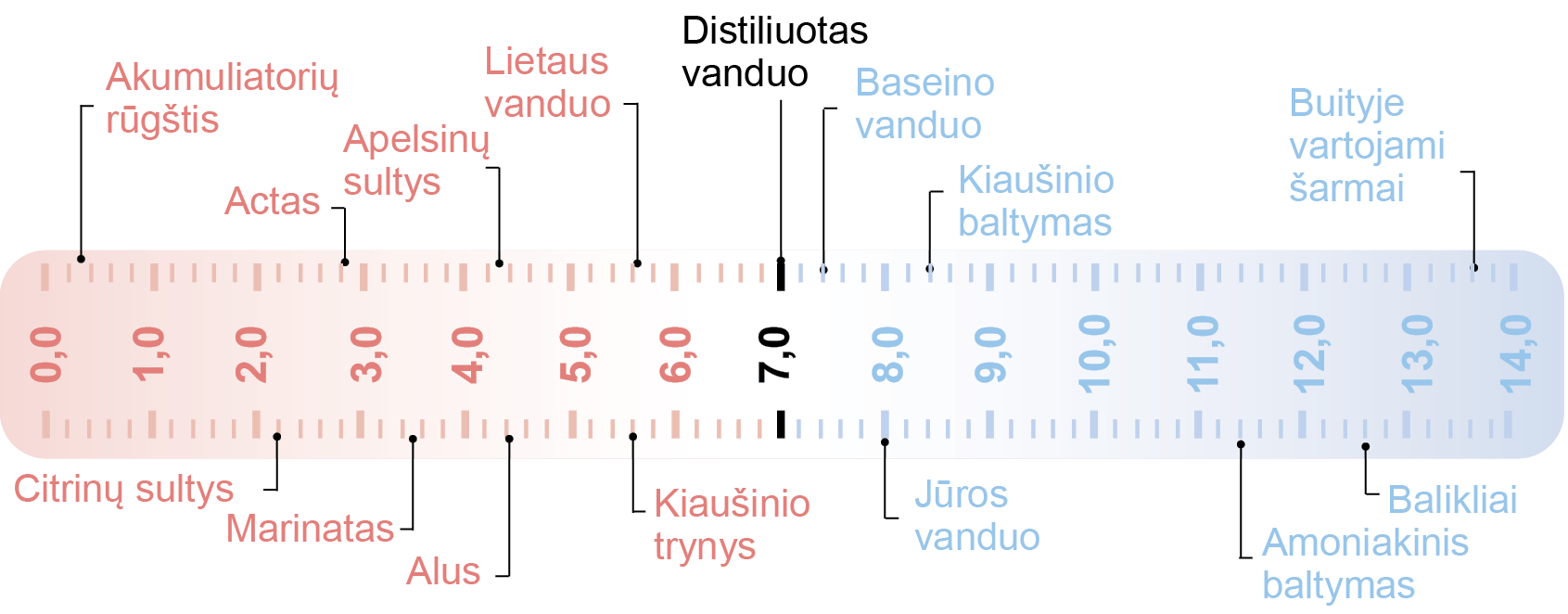
8 pav. Buityje naudojamų tirpalų ir kai kurių maisto produktų pH vertės