Teorinė medžiaga
5.2. Tirpalai
5.2.3. Elektrolitų jonizacija ar disociacija
Tirpinamų ar lydomų joninių junginių skaidymasis į jonus vadinamas disociacija (5 pav.).
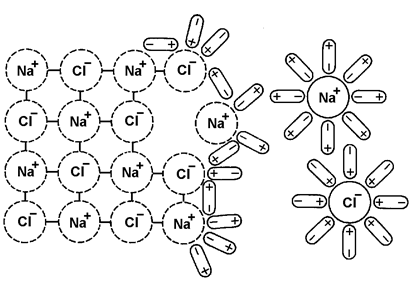
5 pav. Valgomosios druskos NaCl disociacija ir jonų hidratacija (vandens prijungimas)
NaCl disociaciją galima užrašyti taip:
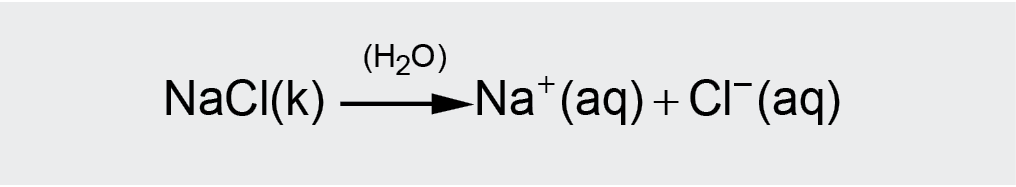
Stiprieji elektrolitai: visos tirpios druskos, dauguma neorganinių rūgščių (H2SO4, HNO3, HCl, HBr, HI, HMnO4, HClO3), šarminių ir šarminių žemių metalų hidroksidai (NaOH, KOH, Ba(OH)2).
Silpnieji elektrolitai: HF, sulfito rūgštis H2SO3, Ca(OH)2, beveik visos organinės rūgštys (pvz., HCOOH ir CH3COOH) ir kai kurios neorganinės rūgštys (H2CO3, H2S, HCN, HClO), daugelio metalų hidroksidai (išskyrus šarminių ir šarminių žemių metalų), amoniakinis vanduo NH3 · H 2O(aq), aminai R-NH2, R-NH-R1 ir kt. (apie aminus žr. temoje „Organiniai junginiai“)
Kadangi absoliučiai netirpių medžiagų nėra, ištirpusi netirpiųjų medžiagų dalis yra laikoma stipriuoju elektrolitu. Pavyzdžiui, 30 °C temperatūroje ištirpsta 10–12 mg/l CaCO3. Vadinasi, ištirpęs CaCO3 disocijuoja:
CaCO3 → Ca2+ + CO32- (žr. 5.2.7 skyriaus 5 uždavinio sprendimą)
Jonizacija yra neutralių molekulių virtimas jonais.
Elektrolitų disociacijos ar jonizacijos laipsnis α rodo, kuri ištirpusios medžiagos dalis suskilo į jonus.

Disociacijos laipsnio vertė kinta nuo 0 iki 1. Neelektrolitų tirpalų α = 0. Jeigu visa medžiaga disocijuoja į jonus, tai α = 1 arba α = 100 %.
Egzaminų lentelėse pateikiamos rūgščių ir bazių disociacijos ar jonizacijos konstantos: rūgštingumo Ka ir bazingumo Kb.
Jonizacijos/disociacijos konstantų vertės, leidžiančios atskirti stipriuosius ir silpnuosius elektrolitus, yra šios:
stipriųjų elektrolitų – kai K ≥ 10-2, vidutinio stiprumo – kai K ~10-2–10-4, silpnųjų – kai K ~10-4–10-10.