Teorinė medžiaga su pavyzdžiais
2.1. Atomo sandara
2.1.2. Izotopai
Izotopai – tai to paties cheminio elemento atomai, turintys vienodą branduolio krūvį, bet skirtingą masės skaičių. Jų branduoliuose yra vienodas protonų, bet skirtingas neutronų skaičius.
Daugumos vandenilio atomų branduoliuose yra 1 protonas ir 0 neutronų. Tačiau gamtoje egzistuoja ir tokie vandenilio atomai, kurių branduoliuose yra neutronų. Trys vandenilio izotopai yra protis (jo branduolyje yra tik 1 protonas), deuteris (jo branduolį sudaro 1 protonas ir 1 neutronas; kartais jis žymimas simboliu D) ir tritis (jo branduolį sudaro 1 protonas ir 2 neutronai; kartais jis žymimas simboliu T). Visų šių atomų branduoliuose yra tik po 1 protoną – visi jie yra to paties cheminio elemento atomai. Cheminės izotopų savybės yra vienodos.
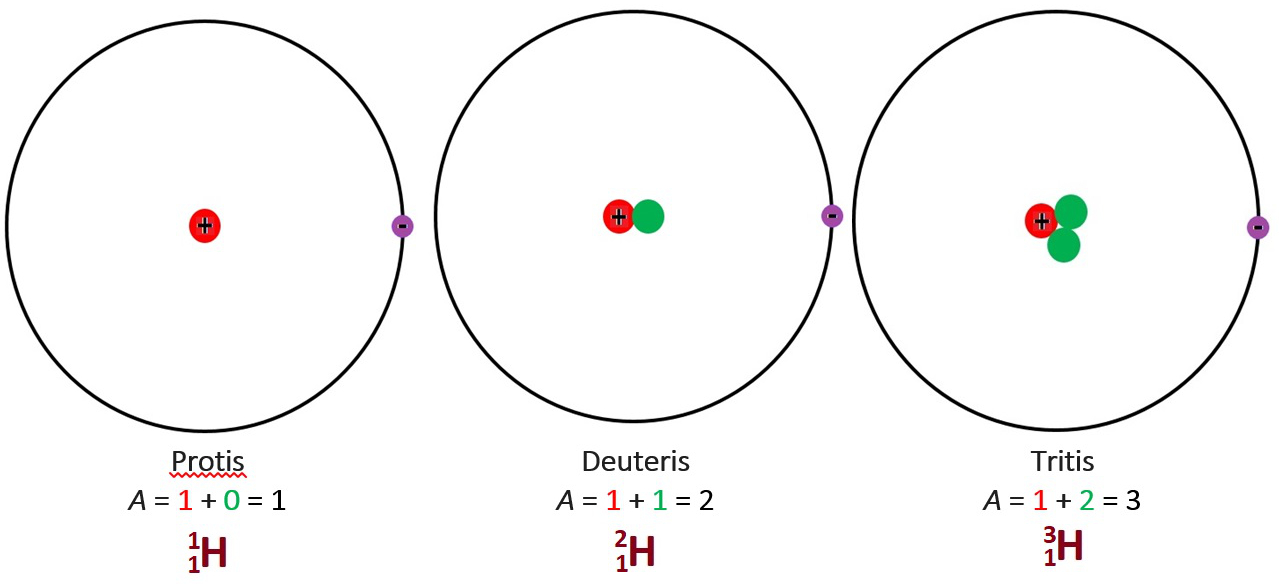
2.1.2. pav. Vandenilio (Z = 1) izotopai
Dauguma cheminių elementų gamtoje egzistuoja kaip izotopų mišiniai. Periodinėje elementų lentelėje yra nurodytos gamtinių izotopų mišinių vidutinės santykinės atominės masės. Jos apskaičiuojamos, įvertinant kiekvieno izotopo masės skaičių ir santykinį paplitimą gamtoje. Egzistuoja du anglies izotopai

Anglies vidutinė santykinė atominė masė yra
![]()
Jei cheminis elementas neegzistuoja gamtoje, periodinėje elementų lentelėje nurodoma jo stabiliausio izotopo santykinė atominė masė, kuri rašoma skliausteliuose.