Teorinė medžiaga su pavyzdžiais
2.3. Cheminiai ryšiai
2.3.1. Joninis ryšys
Joninis ryšys – tai cheminis ryšys, kuris susidaro veikiant priešingo krūvio jonų elektrostatinėms traukos jėgoms.
Susidarant joniniam ryšiui, vienas atomas savo elektronus atiduoda kitam ir jie abu virsta jonais. Tokį ryšį gali sudaryti didelį elektrinių neigiamumų skirtumą turintys atomai, t.y. metalų (virsta katijonais) ir nemetalų (virsta anijonais) atomai.
Joninis ryšys – tai cheminis ryšys, kuris susidaro veikiant priešingo krūvio jonų elektrostatinėms traukos jėgoms.
Susidarant joniniam ryšiui, vienas atomas savo elektronus atiduoda kitam ir jie abu virsta jonais. Tokį ryšį gali sudaryti didelį elektrinių neigiamumų skirtumą turintys atomai, t.y. metalų (virsta katijonais) ir nemetalų (virsta anijonais) atomai.
Pavyzdžiui, natrio atomas atiduoda vieną valentinį elektroną chloro atomui ir virsta natrio jonu, o chloro atomas prisijungia vieną elektroną ir virsta chlorido jonu:
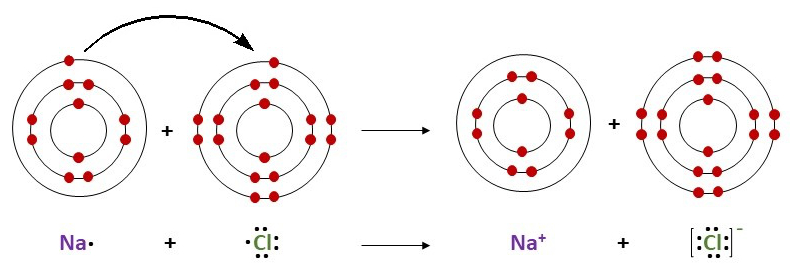
2.3.1. pav. Natrio ir chlorido jonų susidarymas
Abu jie įgyja stabiliąją energetinę būseną (oktetą) – artimiausių inertinių dujų atomo elektronų konfigūraciją.
Priešingo ženklo jonai traukia vieni kitus, o vienodo – stumia. Jonai išsidėsto tam tikra tvarka, vadinama joniniu kristalu, kad šios jėgos kompensuotų vienos kitas. Joniniuose junginiuose neįmanoma išskirti atskiros jonų grupės, kurią būtų galima pavadinti molekule, nes joniniame kristale jonai sąveikauja su visais juos supančiais jonais.
Junginiai, kuriuose elementų atomai yra sujungti joniniu ryšiu, vadinami joniniais junginiais.
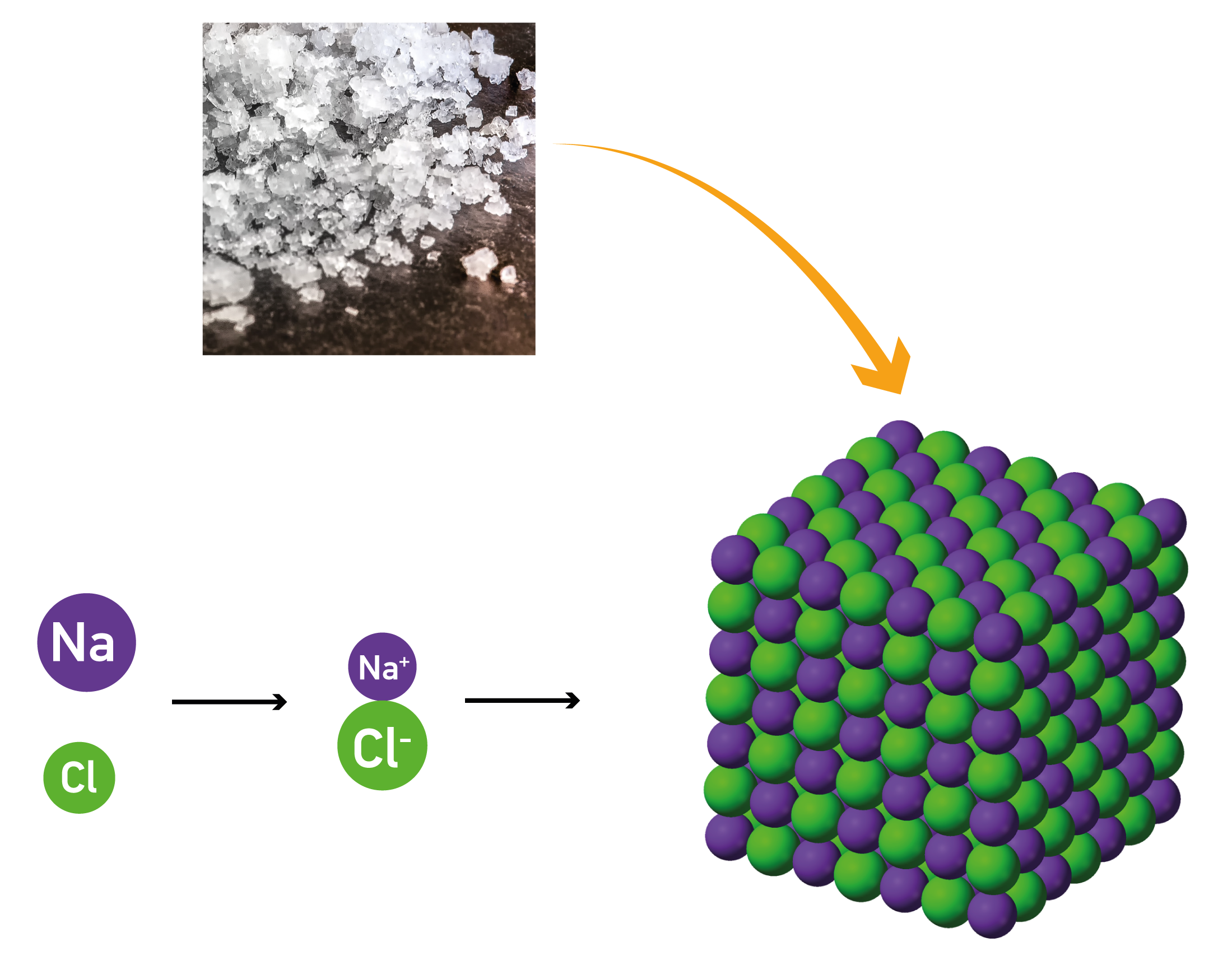
2.3.2. pav. NaCl susidarymas
NaCl kristale kiekvieną Na+ joną supa šeši Cl- jonai, o kiekvieną Cl- joną supa šeši Na+ jonai.
Joninį ryšį sudaro IA-IIIA grupių metalai su VA-VIIA grupių nemetalais, nes šių elementų atomai yra linkę sudaryti stabilią užpildytą elektroninę konfigūraciją. Pavyzdžiui, suartėjus tipinio metalo kalio (K) ir tipinio nemetalo fluoro (F) jonams, kalio atomas atiduoda elektroną ir virsta K+ jonu, o fluoras prisijungia elektroną ir virsta F- jonu. Dėl traukos jėgų šie priešingo krūvio jonai sudaro joninį ryšį.
Joninis ryšys būdingas druskoms, kai kuriems oksidams ir hidroksidams.