Teorinė medžiaga su pavyzdžiais
2.2. Periodinis dėsnis ir periodinė elementų lentelė
2.2.1. Periodiškai kintančios cheminių elementų savybės periodinėje lentelėje
Periodinėje elementų lentelėje cheminiai elementai išdėstyti jų atominio skaičiaus didėjimo tvarka. Periodinės elementų lentelės horizontaliosios eilės vadinamos periodais, o vertikalūs stulpeliai – grupėmis.
Periodas prasideda šarminiu metalu ir baigiasi inertinėmis dujomis. Visi vieno periodo elementai turi tokį pat elektronų energijos lygmenų skaičių. Didėjant periodo numeriui, elementų atomai įgyja vienu energijos lygmeniu daugiau negu prieš tai esančio periodo elementų atomai. Kiekvieno periodo elemento atomai, einant iš kairės į dešinę, išoriniame energijos lygmenyje turi vienu elektronu daugiau negu prieš tai esančio elemento atomai.
Periode iš kairės į dešinę silpnėja metališkosios ir stiprėja nemetališkosios savybės. Kiekvieno periodo pradžioje esantys elementai pasižymi metališkosiomis savybėmis, o esantys periodo gale arti inertinių dujų – nemetališkosiomis savybėmis. Kiekviename periode, didėjant atomo elektronų skaičiui, atomo spindulys trumpėja.
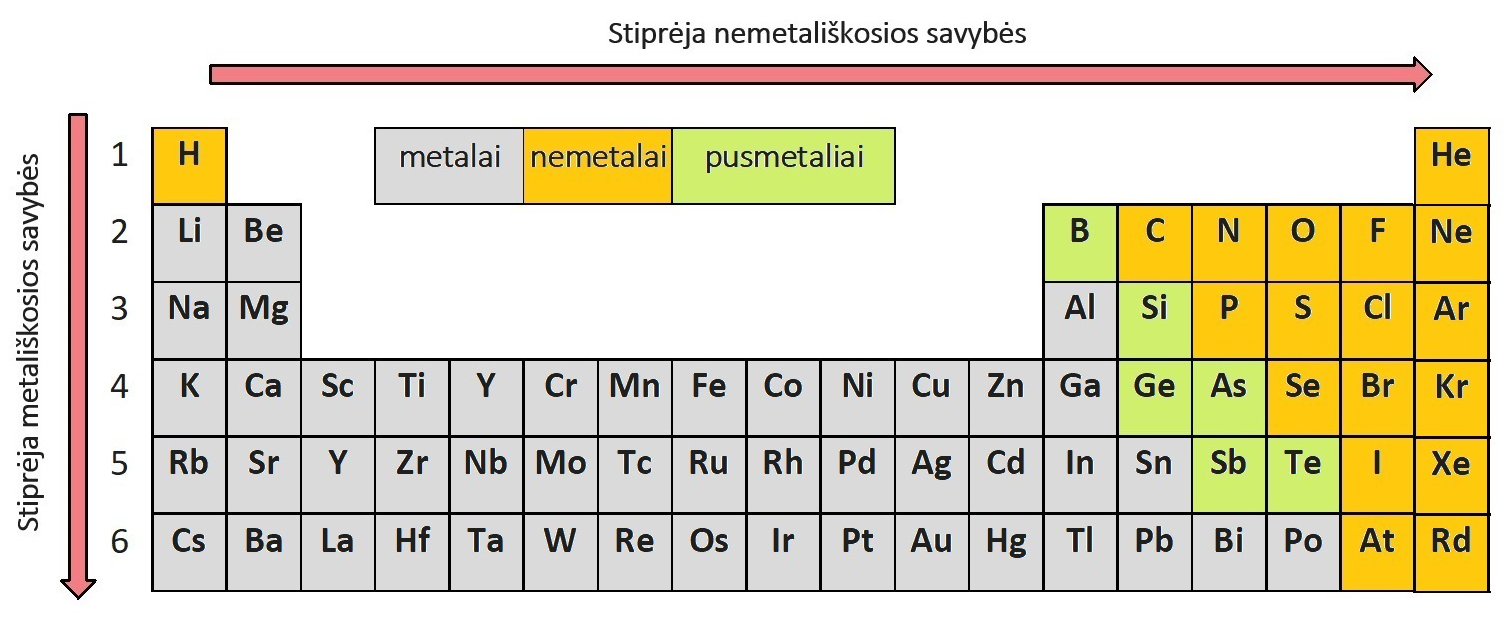
2.2.1. pav. Elementų metališkųjų ir nemetališkųjų savybių kitimas grupėse ir perioduose
Grupėse visi tos pačios grupės elementai išoriniame energijos lygmenyje turi vienodą skaičių elektronų, todėl jų cheminės savybės panašios. Grupės numeris rodo elektronų, galinčių sudaryti cheminius ryšius, skaičių.
Grupėse iš viršaus į apačią stiprėja metališkosios savybės ir silpnėja nemetališkosios savybės. Grupėse iš viršaus į apačią didėjant atomo branduolio krūviui ir elektronų lygmenų skaičiui, A grupių elementų atomų spinduliai ilgėja sparčiau negu B grupių elementų.
Grupės gali būti žymimos romėniškaisiais (nuo I iki VIII, prie kurių rašoma A arba B raidė) ar arabiškaisiais (nuo 1 iki 18) skaitmenimis. A raide žymimos pagrindinės grupės – tos, į kurias įeina 1-7 periodo elementai. Šalutines grupes sudaro tik 4–7 periodo elementai.
IA grupės elementai (išskyrus H) vadinami šarminiais metalais. IIA grupės metalai (išskyrus Be ir Mg) vadinami šarminių žemių metalais. VIIA grupės elementai – halogenais, o VIIIA grupės elementai – inertinėmis dujomis.

2.2.2.pav. Elementų atomų spindulių kitimas cheminių elementų sistemoje.
Metalų atomai yra didesni už nemetalų atomus. Kuo didesnis atomas, tuo toliau nuo branduolio yra valentiniai elektronai ir tuo lengviau atomas gali jų netekti. Visų cheminių elementų atomai, susidarant junginiams, stengiasi savo išoriniame energetiniame lygmenyje įgyti tokį elektronų skaičių, kokį turi arčiausiai jų periodinėje sistemoje esančios inertinės dujos.
Cheminiai elementai skirstomi į metalus, nemetalus ir pusmetalius.
Metalams būdinga aukšta lydymosi temperatūra, jie yra blizgus, kalūs, plastiški, laidūs elektrai ir šilumai. Visi metalai (išskyrus Hg, kuris yra skystas) kambario temperatūroje yra kieti. Chemiškai reaguodami metalai atiduoda elektronus ir virsta teigiamaisiais jonais (katijonais).
Nemetalai yra mažai laidūs elektrai ir šilumai, neblizgūs. Kambario temperatūroje nemetalai yra dujos (vandenilis, deguonis, azotas, floras, chloras), skysčiai (bromas) ar kietos medžiagos (anglis, jodas). Chemiškai reaguodami nemetalai prisijungia elektronus ir virsta neigiamaisiais jonais (anijonais).
Pusmetaliai – tai kristalinės medžiagos, pagal savitąjį elektroninį laidumą esančios tarp metalų ir puslaidininkių. Išvaizda pusmetaliai panašesni į metalus – tipiški pusmetaliai yra blizgūs. Jų cheminės savybės labiau panašios į nemetalų savybes.