Teorinė medžiaga su pavyzdžiais
2.1. Atomo sandara
2.1.3. Elektronai atome
Elektronai, esantys aplink branduolį, sudaro elektronų apvalkalą. Jame elektronai išsidėsto sluoksniais, atitinkančiais atstumus, kuriais elektronai yra nutolę nuo branduolio. Kiekvienas toks sluoksnis, supantis atomo branduolį su jam priklausančiais elektronais, vadinamas energijos lygmeniu.
Erdvė, kur yra didžiausia tikimybė būti elektronui, vadinama orbitale. Orbitalėje gali būti ne daugiau nei du elektronai, turintys priešingus sukinius. Elektrono sukinys vaizduojamas kaip į viršų (↑) arba į apačią (↓) nukreipta rodyklė. Aplink besisukantį elektros krūvį susidarančio magnetinio lauko kryptis priklauso nuo krūvio sukimosi krypties. Elektronas įsivaizduojamas kaip besisukantis aplink savo ašį rutuliukas, t. y. mažas magnetas. Orbitalėje priešingų sukinių elektronai traukia vienas kitą ir taip susidaro elektronų pora. Dėl šios priežasties vienoje orbitalėje gali būti tik du elektronai.
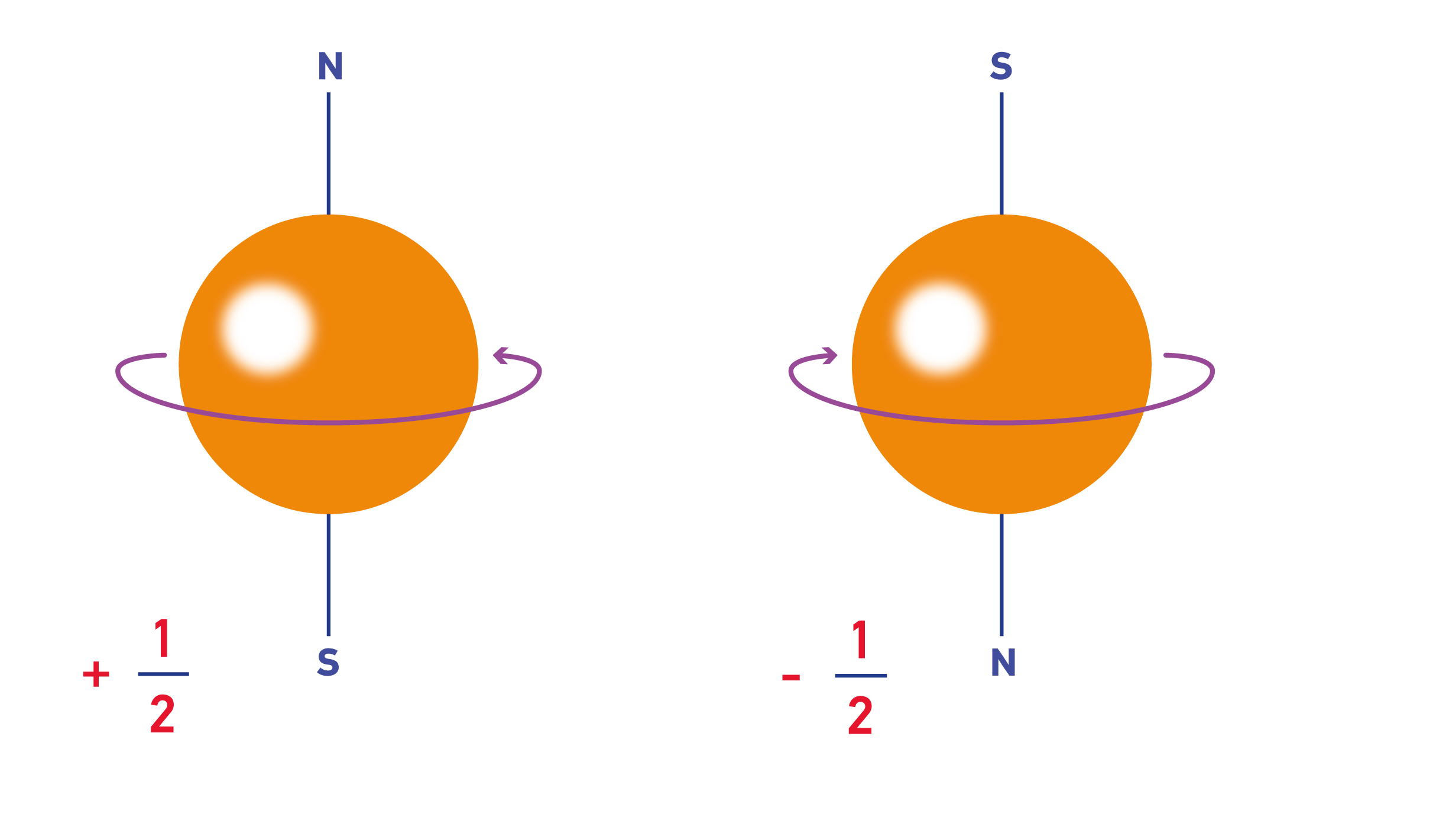
2.1.3. pav. Elektrono sukiniai
Du paprasčiausi orbitalių tipai yra s ir p.
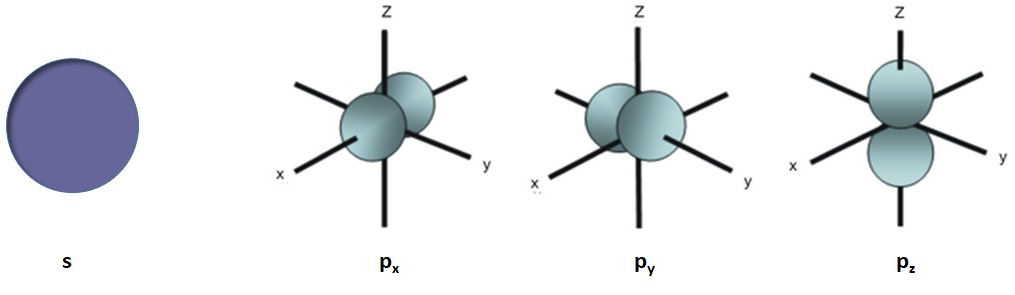
2.1.4. pav. s ir p orbitalės
Tame pačiame energetiniame lygmenyje yra viena s orbitalė,
kuri dviem elektronais yra užpildoma pirmiausiai, ir trys p orbitalės (px, py,
pz), kurios iš pradžių užpildomos po vieną elektroną, o po to jau ir po antrą.
Pirmame energijos lygmenyje yra tik viena s orbitalė, antrame energijos lygmenyje yra dviejų tipų orbitalės – s ir p. Supaprastintai orbitales galima vaizduoti kaip polygmenis.

2.1.5. pav. Energijos lygmuo ir polygmeniai
Vandenilio (H) atomo branduolyje yra 1 protonas ir atitinkamai aplink branduolį skrieja 1 elektronas. Antrasis elementas pirmajame energijos lygmenyje yra helis (He), kurio atomo branduolyje yra 2 protonai ir aplink branduolį yra 2 elektronai s orbitalėje (2.1.6. pav.).

2.1.6. pav. Vandenilio ir helio elektronų išsidėstymas atomų energijos lygmenyje
Didėjant elementų atominiam skaičiui (protonų skaičiui branduolyje), elektronai užpildo vis naujas orbitales. Užsipildžius orbitalėms viename energijos lygmenyje (sluoksnyje), elektronai pildo orbitales didesnės energijos lygmenyje (toliau nuo branduolio nutolusiame sluoksnyje). Atomai, turintys pilnai užpildytus energijos lygmenis, yra stabiliausi.
Ličio (Li), kurio atominis skaičius Z = 3, du elektronai užpildo pirmojo energijos lygmens s orbitalę, o trečiasis elektronas pradeda pildyti antrojo energijos lygmens s orbitalę (2.1.7. pav.). Berilio (Be) ketvirtasis elektronas tampa antruoju elektronu toje pačioje antrojo energijos lygmens s orbitalėje. Boro (B) penktasis elektronas pradeda pildyti antrojo energijos lygmens p orbitales (antrąjį polygmenį). Anglies (C) ir azoto (N) atitinkamai šeštasis ir septintasis elektronai pildo vis kitą p orbitalę, o deguonies (Z=8) atomo aštuntasis elektronas tampa antruoju elektronu pirmoje p orbtalėje, nes daugiau laisvų orbitalių nėra. Atitinkamai fluoro (F) ir neono (Ne) devintasis ir dešimtasis elektronai užpildo kitas dvi p orbitales. Neono elektrono konfigūracija yra stabiliausia, nes užpildytos visos elektronų orbitalės.
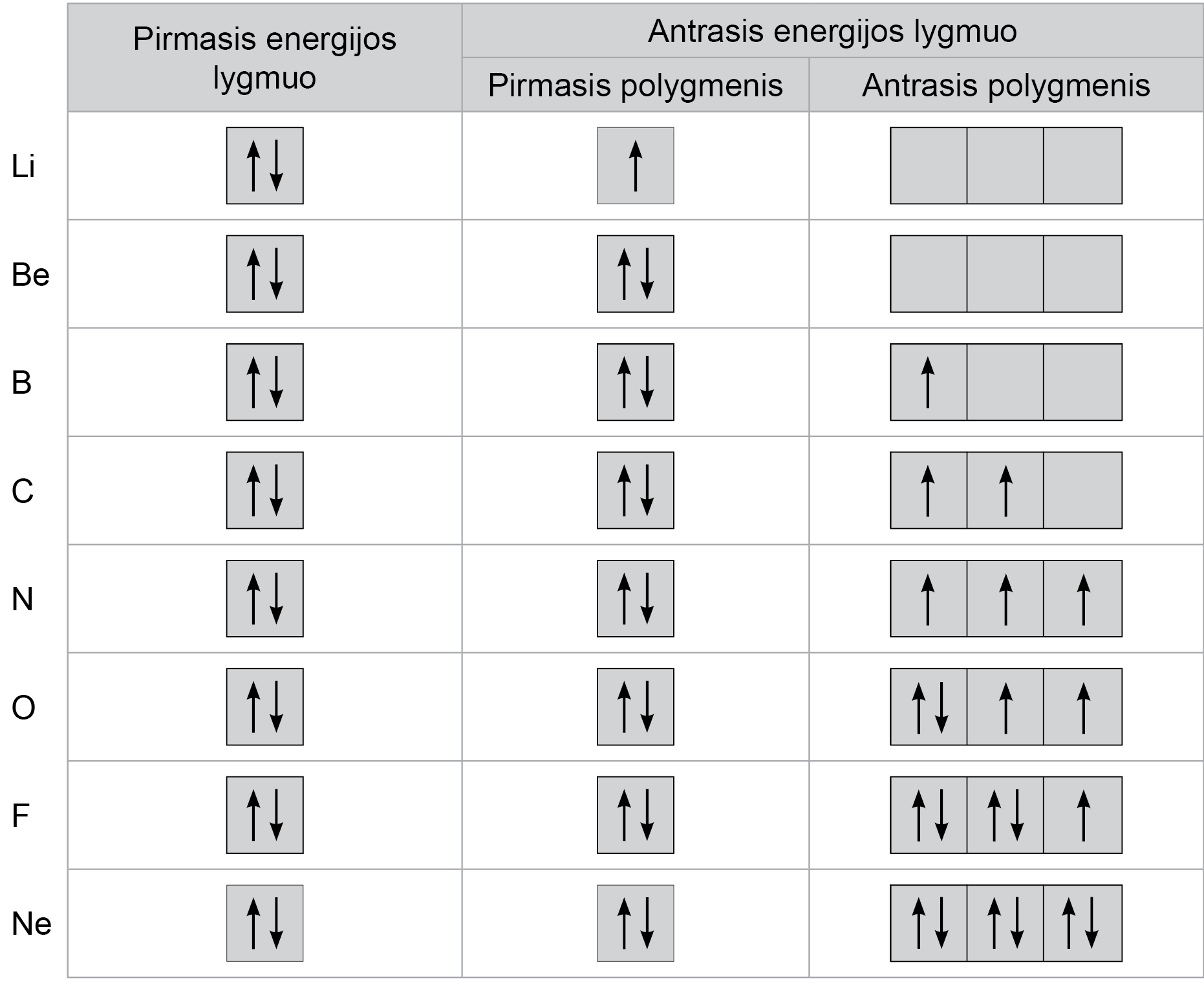
2.1.7. pav. Elementų nuo ličio iki neono elektronų išsidėstymas atomų energijos lygmenyse ir polygmeniuose
Atomai gali jungtis tarpusavyje tik pasikeitus jų elektroninei sandarai. Arčiau branduolio esančių ir jo stipriau traukiamų vidinių energijos lygmenų elektronai negali dalyvauti susidarant cheminiams ryšiams. Labai svarbūs yra valentiniai elektronai, kuriems priskiriami didžiausios energijos orbitalėse esantys elektronai.